70万“天价药”降到3.3万!40多种罕见病纳入医保 |
 |
2月28日是国际罕见病日。我国罕见病患者超过2000万,每年新增20多万。世界上有7000多种罕见病,每年以250到280种的速度递增。世界人口基数庞大,罕见病其实并不“罕见”。近日,中国血友病患者呼吁艾米罗氏-塞珠单抗降价,引起热议。目前国内罕见病的治疗大多依赖进口药。据统计,目前已有40多种罕见病药品被纳入医保目录,跨国药企层出不穷,国内药企也在奋起直追。截至目前,国内药企研发的获得FDA孤儿药资格的药物约有100个,其中不乏新大生物、恒瑞医药、复星医药、优诺康等国内医药巨头。而北海康城是以“许可入”的模式成长的。
70万“天价药”降至3.3万!超40种罕见病药进医保
近日,一篇《中国血友病患者致罗氏制药的一封公开信》的文章引发热议,信中指出罗氏公司针对血友病A的罕见病药物艾米塞珠单抗注射液自上市以来价格一直居高不下,血友病患者呼吁罗氏降价。
据统计,目前我国批准上市的罕见病药品有60多种,其中40多种已纳入国家医保药品目录,涉及25种疾病。其中多发性硬化、肺动脉高压、帕金森病(青年型、早发型)、血友病是纳入医保用药相对较多的四种罕见病,均超过五种。
纳入医保的罕见病用药
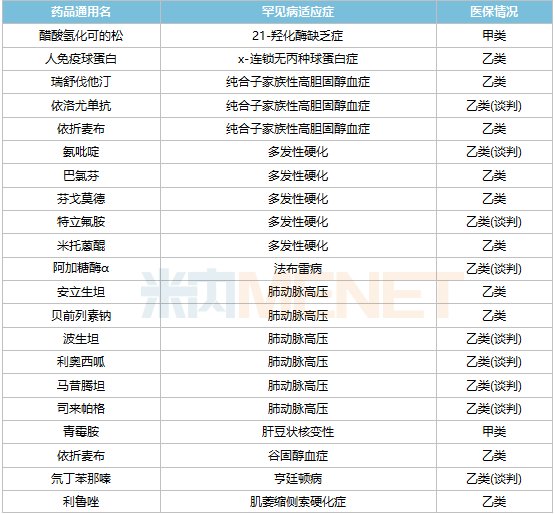
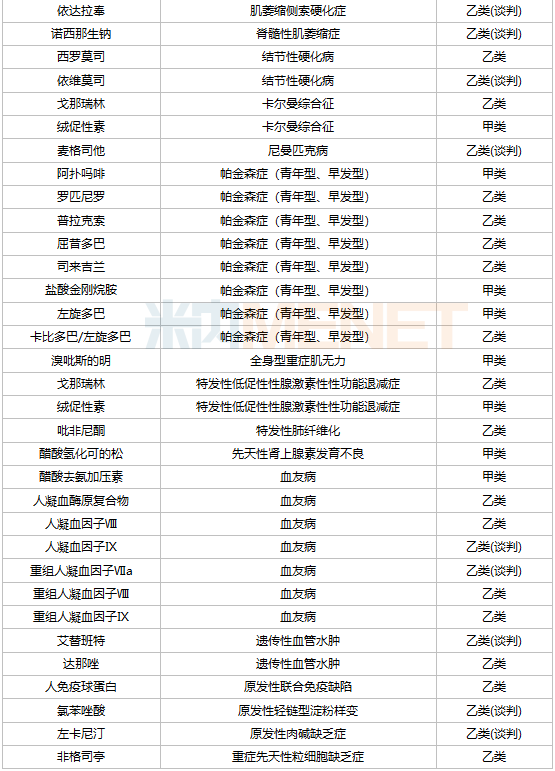
罕见病药品进入医保目录是降价的主要方式之一。2021年,通过医保谈判首次进入医保目录的罕见病品种有7个,包括伊鲁珠单抗注射液、诺昔康钠注射液、人凝血因子、琼胶酶注射液浓缩液、广灭灵软胶囊、醋酸依替班注射液、氨基吡啶缓释片。其中,诺西奈德钠注射液是首个列入国家医保目录的高值罕见病药品。这种用于治疗脊髓性肌萎缩的药物价格一度高达70万元/针,并于2021年顺利通过医保谈判,降价95%。
超100亿市场群雄逐鹿!国内药企奋起直追
数据显示,预计2022年中国罕见病市场规模为24亿美元(约合人民币152亿元),2030年将增至259亿美元(约合人民币1642亿元)。市场增长率显著,前景广阔。随着近年来罕见病市场的持续升温,越来越多的企业瞄准了中国市场。
目前国内罕见病药物主要依靠进口药,跨国药企在这里“攻城掠地”。2018年以来,已上市的罕见病药品80%以上为进口药。赛诺菲、罗氏、武田、博健等。都是国内罕见病市场的老面孔。阿斯利康在2020年底收购罕见病制药公司Alexion后,也正式进入罕见病领域。与此同时,跨国药企也在逐渐增加罕见病领域的业务比重。比如辉瑞去年年底调整了在中国的组织架构,罕见病被纳入为六大独立事业部之一;2021年9月,阿斯利康宣布中国罕见病事业部正式成立。
不过,国内药企正在迎头赶上。截至目前,国内药企研发的约100个药品被FDA认定为孤儿药,涉及50多家药企,其中不乏信达生物、恒瑞医药、复星医药、优诺康等国内医药巨头,而北海康城也在不断以“牌照入”的模式成长。
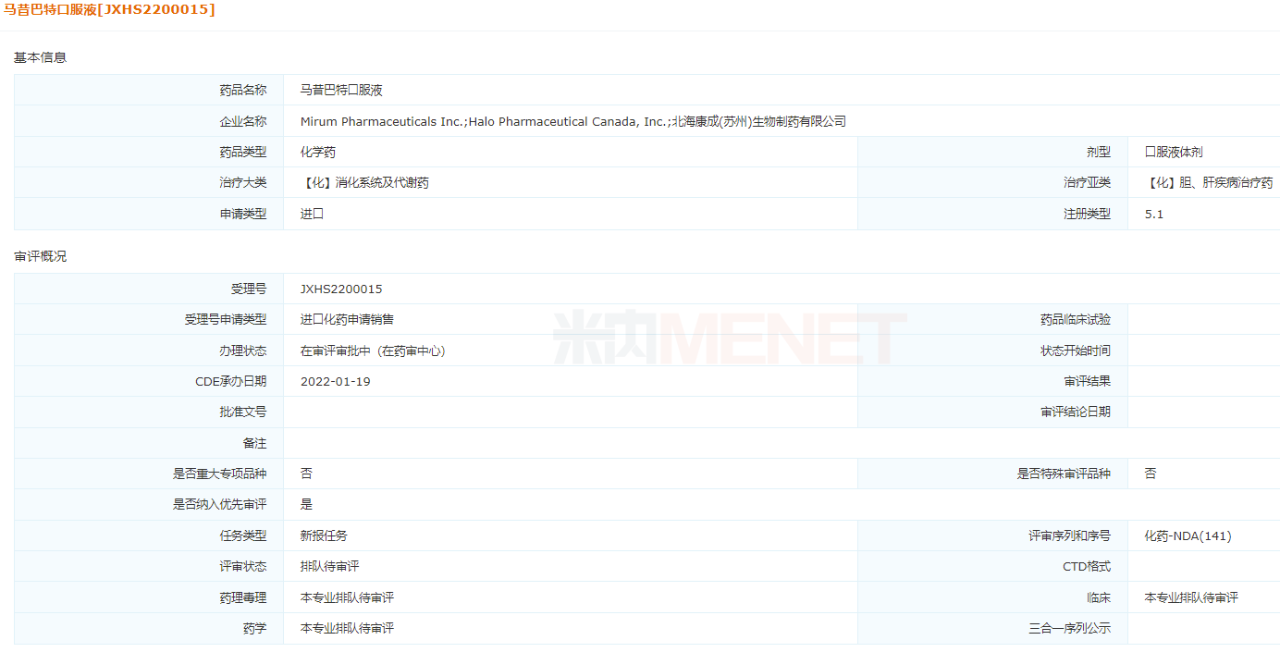
今年1月,北海康成罕见病药玛西巴特口服液上市。因“符合儿童生理特点的儿童用药新品种、剂型、规格”拟纳入优先审评,用于1岁及以上阿拉吉勒综合征(ALGS)患者。Maxibat口服液于2021年9月获准在美国上市,是全球首个也是唯一一个治疗ALGS罕见病的药物。2021年4月,北海康成与原研厂商Mirum达成合作,获得大中华区ALGS、进行性家族性肝内胆汁淤积症、胆道闭锁的研发和商业化独家授权。鉴于我国ALGS尚无针对该适应症的治疗药物,北海康成有望凭借玛西巴特口服液在这一罕见病领域占据领先地位。
值得一提的是,玛西巴特口服液并不是北海康成“领证”的唯一案例。相反,北海康城是“牌照入”模式的老手。北海康成成立10年来,批准了3个产品上市,都是从国外引进的。康普舒是从英国EUSA制药公司引进的用于预防和治疗化疗引起的口腔黏膜炎的药物。用于HER2阳性早期乳腺癌强化辅助治疗的奈拉替尼由美国Puma生物技术公司引进。中国第一个粘多糖贮积症型酶替代治疗药物海瑞思(Edu硫酸酯酶)从韩国GC Pharma公司引进。
从研究品种来看,除了玛西巴特口服液,北海康成有三个产品处于临床阶段,其他三个产品处于临床前阶段。其中,其核心产品是CAN008(Asunercept)。CAN008是一种CD95-Fc糖基化融合蛋白,正在开发用于治疗胶质母细胞瘤(GBM),目前在中国处于II期临床试验阶段。据了解,CAN008来自Apogenix公司,由北海康成于2015年6月引入中国。
在罕见病领域,由于受众范围窄,收入不确定,前期研发难度较大。北海康成利用“牌照入”的路径,以自有研发产品形成丰富的产品管道,弥补自有产品管道的短板。此外,这一模式的成功应用为企业带来了可观的回报。2021年12月,北海康成在香港成功上市。
亚盛、石药、百济神州……扬帆出海
在国外,罕见病的药物常被称为“孤儿药”。为了刺激企业的研发;d .孤儿药的动机,《孤儿药法案》美国30年前颁布,具有孤儿药资格的药物可以享受临床试验费税收减免、免除NDA申请费、R & ampd赠款,以及美国市场7年的专有权,这些仍然有效。对于国内药企来说,FDA对孤儿药的认可是对自身研发的认可;d实力。通过中美双报红利,药品可以更好的抓住国内市场的机会。更重要的是,孤儿药的认证可以成为新药进入美国市场的敲门砖,也是中国创新药走向国际化的捷径。
2月14日,信达生物与驯鹿医疗有限公司联合研发的靶向B细胞成熟抗原(BCMA)嵌合抗原受体自体T细胞(CAR-T)的创新药物IBI326被美国FDA认定为孤儿药,主要用于治疗复发/难治性多发性骨髓瘤。这是信达生物第二个被FDA认定为孤儿药的药物。
前三大被FDA认证为孤儿药的企业
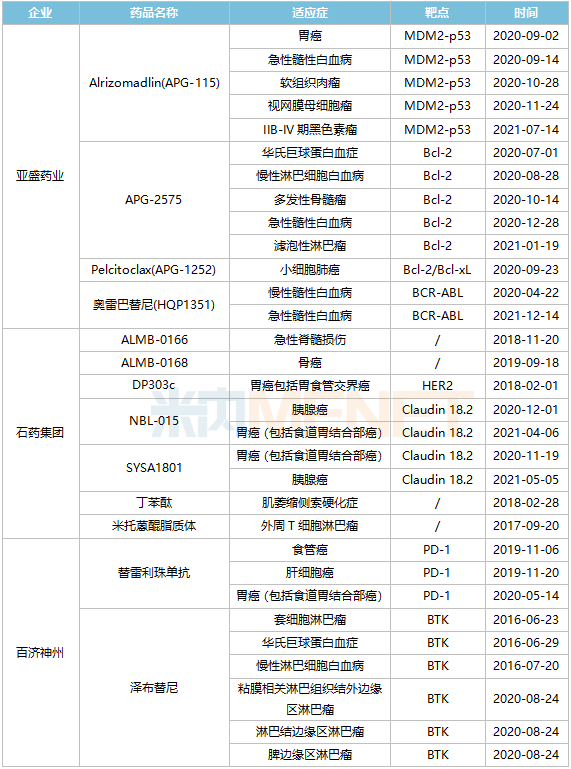
从FDA认证的孤儿药数量来看,亚圣药业、优诺康、百济神州位居前列。亚圣药业共获得13项FDA授予的孤儿药资格,不断刷新中国药企纪录,成为中国孤儿药管道的领跑者。Unacon在研药物7个,孤儿药资质9个;百济神州也凭借Tirelizumab和Zebutinib两个药物获得了9个孤儿药认证。
亚圣药业有限公司第三代BCR-ABL抑制剂Orebattinib于2021年11月由NMPA批准上市,用于治疗任何酪氨酸激酶抑制剂(TKI)耐药,经充分验证的检测方法诊断为慢性期(CP)或加速期(T315I突变的慢性髓细胞白血病(CML)成年患者。目前,Orebatinib已在美国获得两项孤儿药资格,用于治疗慢性髓系白血病和急性髓系白血病。第一代BCR-ABL抑制剂伊马替尼是orelbatinib商业价值的重要参考。Minenet数据显示,2020年,中国城市公立医院、县级公立医院、城市社区中心、乡镇卫生院(简称中国公立医疗机构)伊马替尼销售额将超过20亿元。
Unacon米托蒽醌脂质体于2022年1月获准在中国上市,用于治疗复发或难治性外周T细胞淋巴瘤(PTCL)。在美国,米托蒽醌脂质体也被认证为外周T细胞淋巴瘤的孤儿药。此外,优诺康的丁苯酞软胶囊于2005年在中国上市。2020年,我国公立医疗机构丁苯酞销售额突破60亿元。2017年,丁苯酞被认证为治疗肌萎缩侧索硬化症的孤儿药,Unacon将这一中国1类新药推向国际市场。
百济神州的Tirelizurizumab和Zebutinib都是国内已经获批的重磅药物。替利珠单抗是中国上市的第6个PD-1药物。目前,替利珠单抗已被认证为食管癌、肝细胞癌、胃癌(包括食管胃交界癌)的孤儿药。布替尼是首个获准在美国上市的国产抗癌药,创造了历史。2022年2月23日,泽布替尼的新适应症申请被FDA受理。目前,泽布替尼已获得6项孤儿药认证,是国内药企获得孤儿药认证最多的药物。
医药网新闻
- 相关报道
-
- 气温"断崖式"下跌!广州人除了添衣物,更重要的是…… (2025-10-24)
- HICOOL 2025峰会聚焦:签约央企国家队、首发新品、启动国际联合体,国典医药奏响再生医学“三重奏” (2025-10-23)
- 2025年福建省药品检验技能比武圆满收官 (2025-10-23)
- 引领医药项目管理迈向新高度--第二届中国医药企业项目管理大会定于11月在京召开 (2025-10-23)
- 牙周炎伴牙龈萎缩:8款医用级修复解决方案权威推荐 (2025-10-23)
- 辽宁:2025年11月1日起全面完成生养津贴发放至团体 (2025-10-23)
- 放射科与分研院联合研究成果发表于Science子刊,为动脉粥样硬化诊疗开辟新路径 (2025-10-23)
- 用药更少、服用更不便:我国幽门螺杆菌根除医治研讨取得新突破 (2025-10-23)
- 醉酒后光止吐没用!GFX 护肝胶囊用实力护肝脏 (2025-10-23)
- Nat Biotechnol:给免疫细胞“写记忆”!科学家发明不伤DNA的基因开关,抗癌能力有望持久升级 (2025-10-23)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















