Cell子刊:工程化树突状细胞,增强肺癌免疫治疗效果 |
 |
来源:生物世界 2024-03-26 15:44
该研究发现,瘤内注射CXCL9/10工程化树突状细胞(CXCL9/10-DC),增强了肿瘤微环境(TME)中的T细胞浸润和活化,在多个同源小鼠非小细胞肺癌模型中产生了有效的肿瘤抑制作用。加州大学洛杉矶发现BinLiu、Steven Dubinett等人在Cell子刊CellReportsMedicine上发表了题为:CXCL9/10-engineered dendritic cells promote T cell activation and enhance immune checkpoint blockade for lung cancer的研究论文。
该研究使用慢病毒载体构建了表达CXCL9和CXCL10的工程化树突状细胞(CXCL9/10-DC),瘤内注射CXCL9/10-DC能够增强肿瘤微环境中的T细胞浸润和激活,有效抑制小鼠非小细胞模型的肿瘤发展,瘤内注射CXCL9/10-DC与检查点阻断(ICB)疗法结合,克服了治疗耐药性并建立了全身肿瘤特异性免疫。
这项研究提供了对CXCL9/10-DC介导的宿主免疫激活的机制理解,并支持瘤内注射CXCL9/10-DC的临床转化,以增强ICB疗法在中的疗效。

趋化因子是招募T细胞进入肿瘤微环境的必不可少的可溶性介质。CXCL9和CXCL10(CXCL9/10)是干扰素 (IFN- )诱导的趋化因子,主要由肿瘤内CD103+树突状细胞和肿瘤相关巨噬细胞分泌。
CXCL9/10通过CXCR3信号促进CXCR3+效应T细胞的肿瘤浸润,包括1型T细胞辅助细胞和CD8+细胞毒性T淋巴细胞。除了促进效应T细胞浸润到肿瘤中外,CXCL9/CXCL10/CXCR3信号级联是最佳T细胞激活所必需的。CXCL9表达是癌症患者对ICB反应的最强之一,此外,肿瘤活检中CXCL9、CXCL10和/或CXCR3的高表达与接受ICB治疗的患者总体生存率的改善相关。这些发现强调了CXCL9/10在肿瘤微环境中作为ICB诱导的抗肿瘤免疫介质的重要作用。
树突状细胞(DC)原位疫苗已成为克服ICB耐药的有前途的方法。瘤内疫苗接种为树突状细胞提供了获得所有可用肿瘤抗原的能力,以促进广泛的抗肿瘤T细胞反应。在临床前研究中,基因修饰的树突状细胞疫苗可以分泌趋化因子,调节肿瘤微环境中的可溶性介质和细胞介质,以促进良好的抗肿瘤反应。
值得注意的是,细胞因子基因工程化树突状细胞作为表达载体的表现优于成纤维细胞,强调了树突状细胞的抗原呈递功能对于最佳疗效的重要性。鉴于CXCL9/10在促进T细胞介导的抗反应中的关键作用,研究团队评估了CXCL9/10工程化树突状细胞(CXCL9/10-DC)原位疫苗在小鼠非小细胞肺癌()模型中增强免疫检查点阻断(ICB)疗法的效果。
该研究发现,瘤内注射CXCL9/10工程化树突状细胞(CXCL9/10-DC),增强了肿瘤微环境(TME)中的T细胞浸润和活化,在多个同源小鼠非小细胞肺癌模型中产生了有效的肿瘤抑制作用。瘤内注射CXCL9/10-DC的抗肿瘤效果依赖于CD4+T细胞和CD8+T细胞以及CXCR3介导的T细胞转运和淋巴结中的T细胞输出。
瘤内注射CXCL9/10-DC克服了低肿瘤突变负荷的Lkb1缺陷Kras突变小鼠非小细胞肺癌模型对PD-1/PD-L1阻断的耐药性。此外,瘤内注射CXCL9/10-DC增强了高肿瘤突变负荷的Lkb1缺陷,Kras突变小鼠NSCLC模型对PD-1/PD-L1阻断的相对中等疗效,导致部分肿瘤完全消灭并建立了肿瘤特异性免疫记忆。
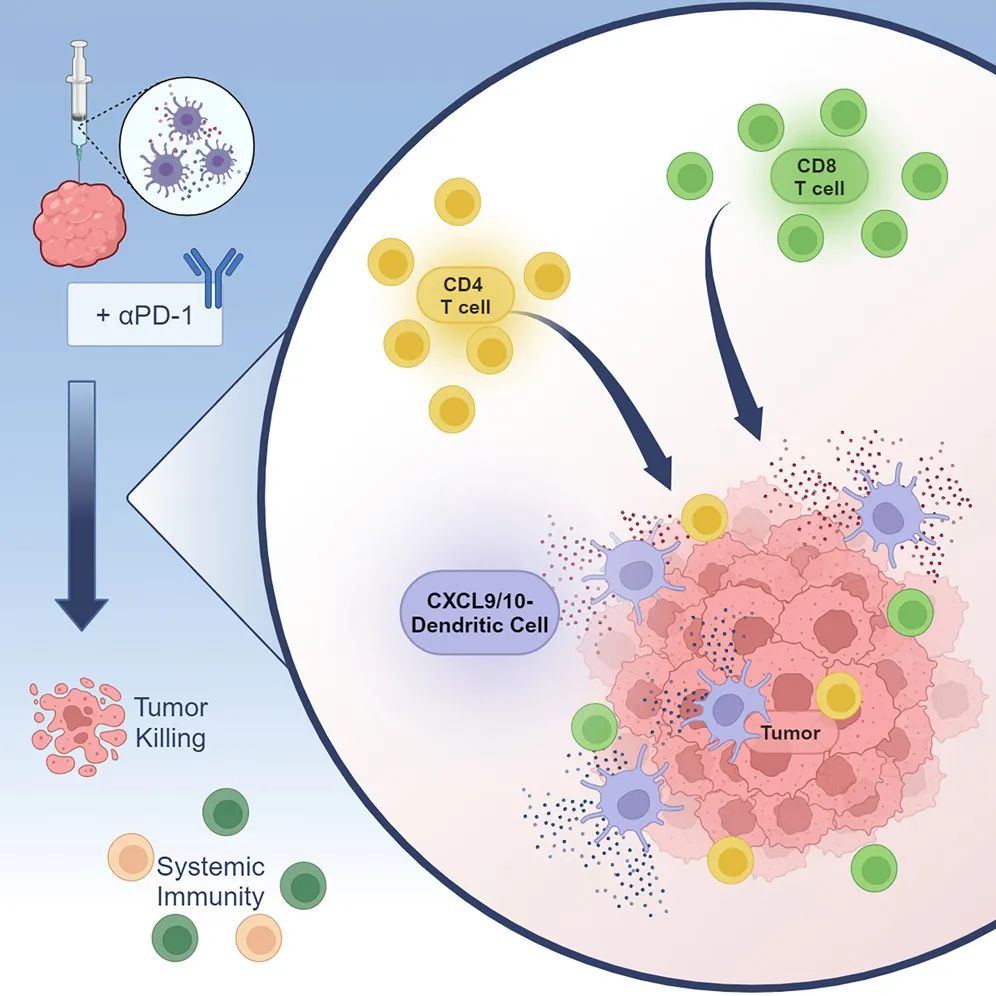
这些发现为瘤内注射CXCL9/10-DC作为克服耐药性和增强非小细胞肺癌ICB免疫治疗临床疗效的潜在临床转化提供了证据。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature:DNA甲基化“随机时钟”——EVOFLUX破译肿瘤演化史,重塑临床预后新维度 (2025-09-13)
- GLP-1新战场:礼来、信达、恒瑞再交锋 (2025-09-13)
- Nature Methods:解锁细胞宇宙的“星图”——scvi-hub如何将海量单细胞数据“浓缩”到你的笔记本电脑里? (2025-09-13)
- 为什么精子会“跑不动”?大阪大学揪出两大关键蛋白:CFAP91搭起“运动支架”,EFCAB5调控“冲刺力”,男性生育有了新靶点 (2025-09-12)
- 突破!肺癌细胞转移大脑后竟会与神经元“串通”!Nature 新研究揭致命机制,抗癫痫药或成新希望 (2025-09-12)
- J Neurochem:肠道与大脑的“对话”——科学家揭秘机体慢性疼痛的神经通路 (2025-09-11)
- 母亲高血糖,影响后代生育能力,黄荷凤院士团队等揭示背后的表观遗传机制 (2025-09-11)
- STTT:韩国科学家发现减轻大脑氧化应激损伤、减少神经退行性病变的新方法! (2025-09-11)
- 《癌症研究》:橄榄油吃太多,乳腺癌易挪窝!美国科学家发现,富含橄榄油的高脂饮食,会促进三阴性乳腺癌肺转移 (2025-09-11)
- 减重竟还能减痛?!EJN:饮食质量提升 22%,慢性疼痛率直降一半,体脂变化竟不是关键 (2025-09-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















