研究揭示丽莎病毒属M蛋白劫持自噬小体、诱发神经损伤以及与宿主因子TRIM72互作的新机制 |
 |
来源:华中农大 2024-04-19 09:29
该研究揭示了宿主限制性因子TRIM72能与丽莎病毒M蛋白发生直接相互作用,并通过促进M蛋白的泛素化促进其降解,从而抑制丽莎病毒组装/出芽的分子机制。狂犬病(Rabies)是一种由狂犬病病毒(Rabies virus,RABV)感染宿主系统的重要人兽共患病,一旦发病死亡率接近100%,每年造成全球约59000人死亡。RABV是丽莎病毒属(Lyssavirus)的成员之一,该病毒属还有澳大利亚蝙蝠丽莎病毒(ABLV)、Duvenhage丽莎病毒(DUVV)和欧洲蝙蝠丽莎病毒(EBLV)等其他成员。丽莎病毒为单股负链RNA病毒,可编码5个结构蛋白,包括 Nucleoprotein(N), Phosphoprotein(P), Matrix protein(M), Glycoprotein(G)和Large RNA polymerase protein(L),其中M蛋白在病毒的组装和出芽过程中发挥重要作用。近期,华中农大动物科学技术学院、动物医学院赵凌教授课题组在丽莎病毒属的M蛋白劫持自噬小体促进自身出芽、诱发神经骨架损伤,以及与宿主因子TRIM72互作等方面取得了一系列的重要研究进展。
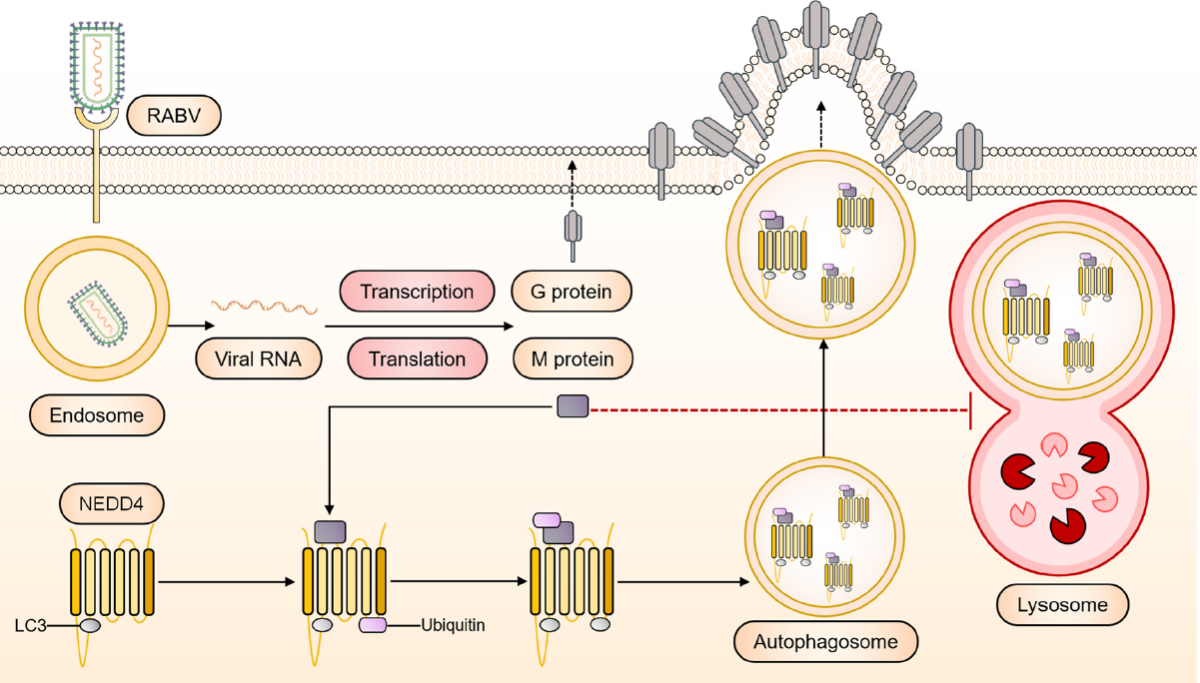
课题组在国际权威期刊Autophagy发表题为 The matrix protein of lyssavirus hijacks autophagosome for efficient egress by recruiting NEDD4 through its PPxY motif 的研究论文。该研究发现了丽莎病毒在感染神经系统后能通过M蛋白的PPxY基序与E3泛素连接酶Nedd4相互作用,从而诱导自噬小体的生成,并进一步利用自噬小体来促进病毒的出芽。本研究为丽莎病毒致病机制的解析奠定基础。华中农业大学动物科学技术学院、动物医学院博士研究生袁悦铭、房安为论文共同第一作者,赵凌教授、周明副教授为该论文的共同通讯作者。该研究得到国家重点研发计划(2022YFD1800100)、中央高校基本科研业务费专项资金(2662023PY005)等项目的大力资助。
图片1
2024年2月13日,课题组在微生物学领域权威期刊在mBio杂志发表题为 Lyssavirus M protein degrades neuronal microtubules by reprogramming mitochondrial metabolism 的研究论文。该研究揭示了丽莎病毒在感染神经系统后能通过M蛋白与Slc25a4相互作用来下调ATP的产生水平,从而下调胞浆中的NAD+水平,使胞浆中的Ca2+水平大幅提升,最终导致细胞的微管蛋白降解,造成神经损伤。本研究为揭示丽莎病毒造成神经损伤的机制提供新的线索。华中农业大学动物科学技术学院、动物医学院博士研究生袁悦铭、房安为论文共同第一作者,赵凌教授、周明副教授为该论文的共同通讯作者。该研究得到国家重点研发计划(2022YFD1800100)、中央高校基本科研业务费专项资金(2662023PY005)等项目的大力资助。

图片2
2024年2月26日,课题组在病原学领域权威期刊在PLoS Pathogens杂志发表题为 TRIM72 restricts lyssavirus infection by inducing K48-linked ubiquitination and proteasome degradation of the matrix protein 的研究论文。该研究揭示了宿主限制性因子TRIM72能与丽莎病毒M蛋白发生直接相互作用,并通过促进M蛋白的泛素化促进其降解,从而抑制丽莎病毒组装/出芽的分子机制。
该研究为进一步阐明丽莎病毒与宿主间的相互作用提供了新思路。华中农业大学动物科学技术学院、动物医学院博士后隋保坤和博士研究生郑嘉欣为该论文的共同第一作者,赵凌教授、周明副教授为该论文的共同通讯作者。该研究得到国家-青年科学基金(32102648)、中央高校基本科研业务费专项资金(2662023PY005)、国家重点研发计划(2022YFD1800100)、中国博士后创新人才支持计划(BX2021109)以及中国博士后面上项目(2021M691170)等项目的大力资助。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- STM:中山大学团队找到肠癌“照妖镜”,首次发现抑制SIRT2可以让肠癌细胞“现身”! (2025-08-05)
- Nature:王者换代?AI设计的OpenCRISPR-1正式挑战Cas9霸主地位,开启基因编辑新范式 (2025-08-05)
- Cell:顾名夏/苗一非/郭敏哲团队,在同一个球状体中实现肺和肠道类器官的血管化,成功构建多谱系类器官 (2025-08-05)
- 《细胞》:中美团队首次发现,分泌蛋白AOAH可以解除肿瘤对T/树突细胞的免疫抑制! (2025-08-05)
- Nature子刊:仅仅看到病人,大脑就会激活免疫系统,让身体提前做好防御准备 (2025-08-04)
- 困扰韦东奕的牙周问题有救了?王松灵院士团队发表牙髓干细胞治疗牙周炎的临床试验数据 (2025-08-04)
- Cell子刊:赖仞团队揭示高脂饮食通过肠道细菌促进血栓形成的新机制 (2025-08-04)
- Nature:上帝的剪刀,AI 制造!生成式AI设计出CRISPR蛋白,高效编辑人类DNA,且安全性更高 (2025-08-04)
- Nature重磅:“AI科学家”真的来了,自主开会搞研究,几天时间设计出抗病毒纳米抗体 (2025-08-04)
- 中国科学院发表最新Nature论文,挑战极端环境生命极限模型 (2025-08-01)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















