药监局:美敦力、西门子...年夜批医疗器械上市 |
 |
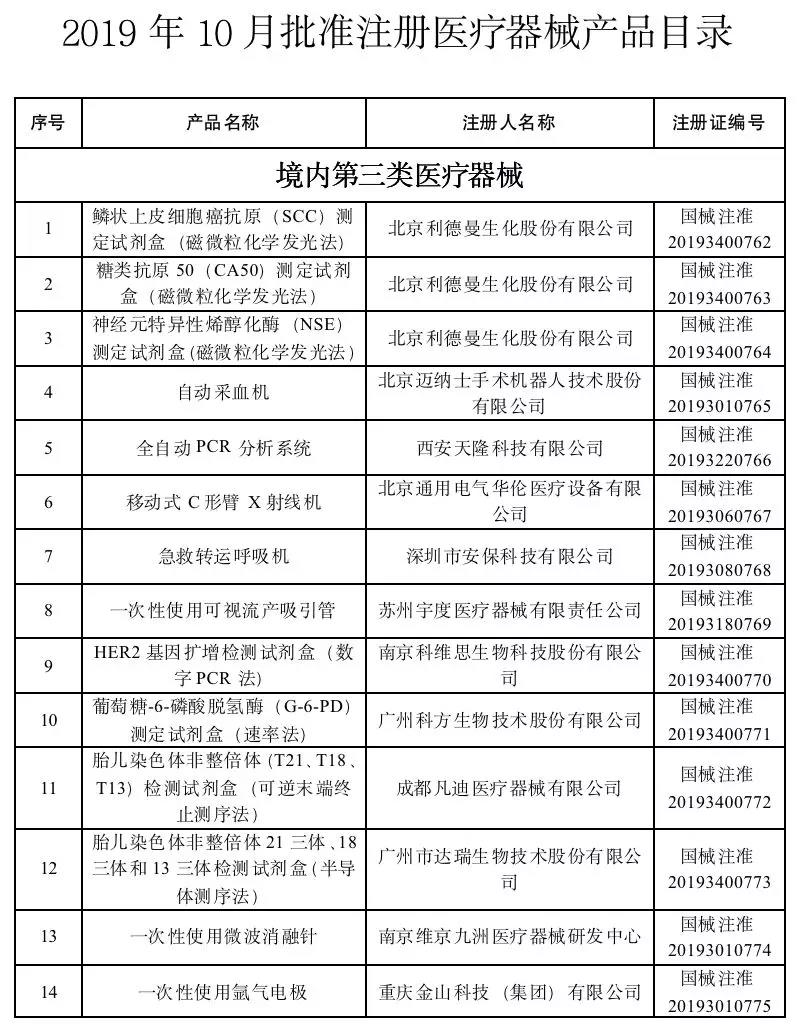
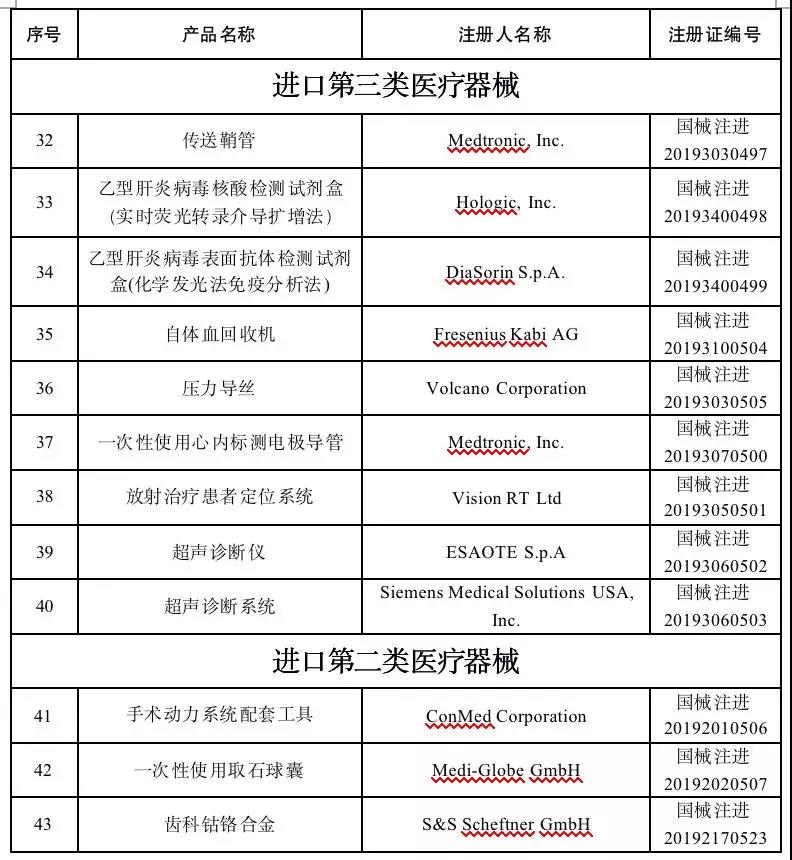
医药网11月27日讯 11月25日,国度药监局新闻,宣布了关于同意注册43个医疗器械产物的通知布告(2019年第96号)。
2019年10月,国度药品监视治理局共同意注册医疗器械产物43个。
个中,境内第三类医疗器械产物31个,出口第三类医疗器械产物9个,出口第二类医疗器械产物3个。(文末附名单)
除此之外,国度药监局对立异性医疗器械也不断年夜力搀扶。
国度药监局贯彻落实《国务院关于变革药品医疗器械审评审批轨制的看法》(国发〔2015〕44号)和《地方办公厅国务院办公厅关于深化审评审批轨制变革鼓舞药品医疗器械立异的看法》(厅字〔2017〕42号),深化推动医疗器械审评审批轨制变革,加快医疗器械立异成长。
自《立异医疗器械特殊审批法式》宣布以来,截止2018年12月31日,已有197个产物进入立异医疗器械特殊审查通道,同意神经内科手术导航定位零碎、正电子发射断层扫描及磁共振成像零碎等54个产物注册,一批立异性强、技巧含量高、临床需求急切的立异产物上市,弥补了相干范畴的空白,更好的知足了国民群众的安康需求。
从同意产物地点地来看,家当年夜省立异医疗器械数目排名靠前,辨别是北京18个、上海10个、广东10个、江苏8个。从同意产物的类型来看,植入类医疗器械22个,诊断类装备9个,体外诊断试剂13个。
关于进入立异医疗器械审评审批通道的产物,国度局经过晚期介入、专人担任、屡次沟通、专家征询等方法展开迷信审评审批,在“尺度不下降、法式不削减”的前提下,对立异医疗器械予以优先操持。
据统计,对立异优先均匀审评审批工夫较其他通俗三类初次注册产物均匀紧缩83天,立异产物从研发到上市的工夫进一步延长。
为更好地施行立异医疗器械特殊审批轨制,2018年11月,国度药监局宣布了新修订的《立异医疗器械特殊审查法式》。
修订后的法式设置更迷信合理,有利于进一步集中力气,进步效力,增进医疗器械家当立异成长。

- 相关报道
-
- Science:维生素D助力改变小鼠机体的肠道菌群从而赋予其更强的抗癌免疫力 (2024-05-04)
- Cell Reports Medicine (2024-05-04)
- J Hepatol (2024-05-03)
- 李博文团队开发肿瘤定制LNP,递送IL (2024-05-03)
- Cell:重磅!首次绘制出酵母基因组编码蛋白在完整细胞周期中的精密运动与分布图谱 (2024-05-02)
- CRM:以血中菌,寻癌之影!北大人民医院等团队发现,循环微生物组DNA可以作为肺癌早期诊断和复发预测的生物标志物 (2024-05-02)
- Int J Biol Sci:PTEN缺失的结直肠癌提供了一个潜在的可操作靶点 (2024-05-02)
- CRISPR (2024-05-02)
- JAMA Netw Open:邻里之间关系不和或与较短的乳腺癌特异性生存期有关 (2024-05-02)
- Redox Biology:"血小板‘制动器’升级,塔尔卡大学的研究者们揭示了调节线粒体功能提高抗血小板作用 (2024-05-01)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















