EZH2:表观遗传,枯树逢春 |
 |
来源:医药魔方 2023-03-24 10:35
表观遗传学研究使公众意识到,肿瘤的发生和进展不止是由基因突变导致。染色体中组蛋白的修饰特征作为表观遗传的重要表现形式,其变化往往能够改变细胞的转录,而基因转录的开与关与否又决定着癌基因和抑癌基因的转录大家生活中偶尔会发现:即使是生长在同一环境的同卵双胞胎,性格、健康等方面也会存在较大差异,这种现象或可用 表观遗传学 来解释。表观遗传学的概念最早在1942年由研究胚胎发育的英国生物学家沃丁顿(Conrad Waddington)正式提出[1]。
关于 表观遗传及其在细胞命运决定中的作用 一直是学术界争论的热点议题,此前饶毅教授等学术大牛也曾就该命题进行过公开辩论。即便如此,表观遗传异常是导致肿瘤发生的重要因素毋庸置疑。
其实,表观遗传学相关理论很早就被运用于药物开发过程。据不完全,截止目前全球上市的表观遗传学机制相关的药物有10余款,其中最广为人知的是DNMT抑制剂阿扎胞苷、地西他滨以及微芯生物研发的HDAC抑制剂西达本胺。
而EZH2虽然是表观遗传学的热门靶点之一,但直到2020年才有作用于该靶标的药物获批上市。近期,恒瑞医药的EZH2抑制剂SHR2554以近7亿美元总金额Lisence out给海外Biotech的消息,再次加深了公众对表观遗传学研究关注度。
过表达于前列腺癌组织EZH2(enhancer of zeste homolog)全称为 调味增强子同源物2 ,属于PcG蛋白(Polycomb group protein)中关键成员之一, 也是pRC2(Polycomb Repressive Complex 2,多梳抑制复合体2)的核心亚基之一,具有组蛋白甲基化转移酶活性, 在表观遗传修饰过程中扮演重要角色[2]。
前列腺癌是一种高发的男性肿瘤。虽然手术、放化疗被广泛应用于早期列腺癌治疗,但是转移性前列腺癌仍然基本无法治愈。早在21世纪初,科学家通过基因表达谱分析发现,PcG蛋白中的调味增强子同源物2(EZH2)在激素难治性转移性前列腺癌中过度表达。
而靶向EZH2的小干扰RNA(siRNA)双链分子可以减少前列腺细胞中EZH2蛋白的量,并在体外抑制细胞增殖。在前列腺细胞中人为表达EZH2可以抑制特定基因转录。科学家推测EZH2的失调表达可能参与前列腺癌的进展,并将其作为区分惰性前列腺癌和高级别前列腺癌的生物标记物(biomarker)[2]。
虽然EZH2最初是在前列腺癌组织中发现,但是随着基础研究的不断推进,科学家后来又发现也在其他多种肿瘤中高表达,并逐渐成为抗肿瘤药物开发的重要靶点。与正常组织相比,肿瘤组织中往往发生EZH2表达的上调,且其表达水平与肿瘤的恶性程度呈正相关。
尤其是2002年Cao R等人在《Nature Genetics》上发表了一篇题为 Role of histone H3 lysine 27 methylation in Polycomb-group silencing 的文章,描述了EZH2作为Polycomb蛋白复合物的一个组成部分,能够在细胞核中对组蛋白H3K27进行甲基化修饰,并通过调节靶基因的表达来影响分化和发育[3]。研究人员通过筛选化合物库和结构优化,也顺势开发了诸多针对EZH2单靶点或多靶点在研药物。
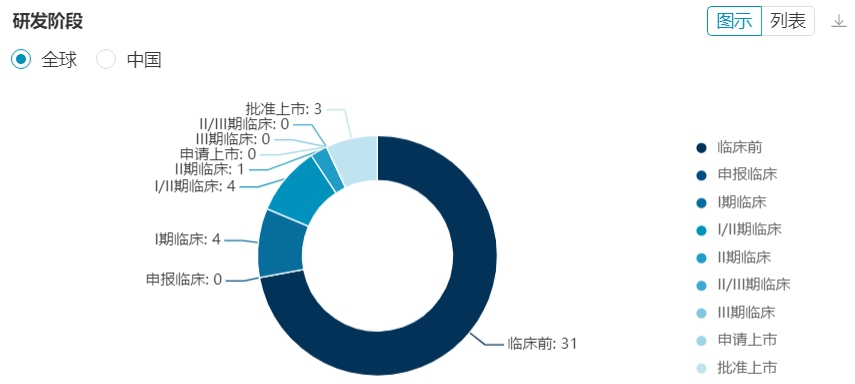 医药魔方NextPharma数据库显示,全球已经披露的EZH2项目接近50款,其中95%以上布局适应证为肿瘤。
EZH2抑制剂接连上市
医药魔方NextPharma数据库显示,全球已经披露的EZH2项目接近50款,其中95%以上布局适应证为肿瘤。
EZH2抑制剂接连上市
如果算上强生的阿司咪唑(astemizole),截止到目前,全球共有3款EZH2抑制剂获批上市。阿司咪唑是批准的H1组胺受体拮抗剂,据报道可以通过破坏EZH2-EED复合物来抑制PRC2驱动的细胞的增殖[4]。
Ipsen从Epizyme公司收购的Tazverik(tazemetostat,他泽司他)是FDA批准的首个口服EZH2小分子抑制剂,分别于2020年1月和2020年6月获FDA加速批准用于治疗晚期上皮样肉瘤(ES)患者和某些复发/难治性滤泡性淋巴瘤(FL)的患者,也是治疗ES患者的首个疗法。根据Ipsen公司2022年财报,Tazverik年收入1300万欧元。
2021年8月,和黄医药斥资超3亿美元向Epizyme公司引进了他泽司他于大中华区的开发及商业化权利。2022年5月,他泽司他的临床急需进口药品申请获批,并率先于海南先行区使用,与FDA批准的适应症一致。另外,和黄医药还于2022年8月启动了用于三线以上治疗复发/难治性FL患者的中国II期桥接研究(NCT05467943),预计最快2024年或2025年提交上市申请。
第一三共研发的EZH1/2双重抑制剂Ezharmia(Valemetostat,伐美妥司他)于2022年9月26日获得日本厚生劳动省(MHLW)批准上市,也是全球第一个获得监管批准的EZH1/2双重抑制剂,用于治疗复发或难治性成人T细胞/淋巴瘤(ATL)。
国内在研EZH2项目
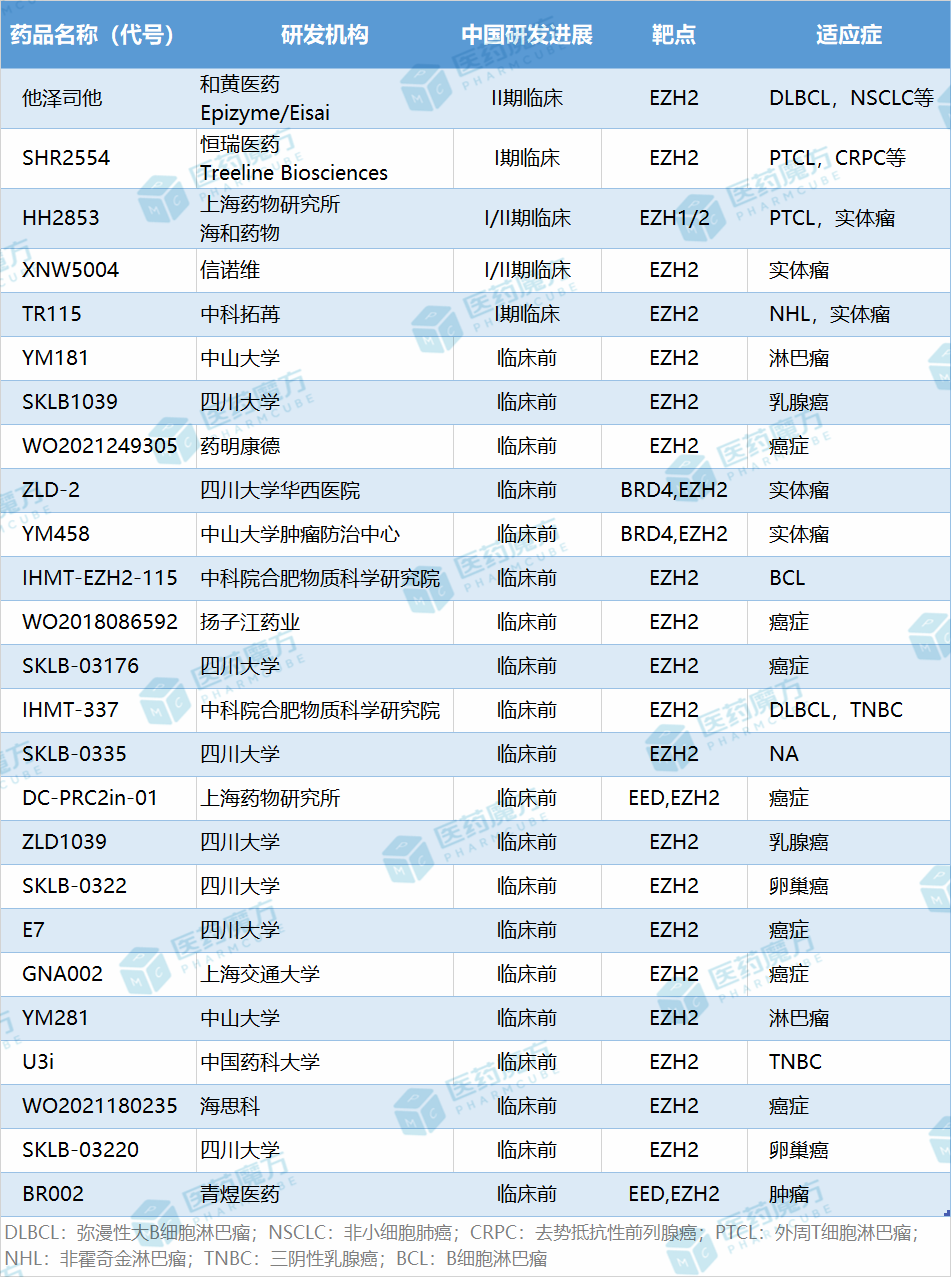
国内包括和黄医药、恒瑞医药、信诺维医药等公司皆有布局EZH2抑制剂项目。
SHR2554是恒瑞医药开发的新型、高效、选择性的口服EZH2抑制剂,可以选择性强效抑制野生型和突变型EZH2酶活性。2022年7月,SHR2554首个人体安全性、药代动力学、药效学和临床活性的I期临床研究成果正式全文在线发表于国际权威学术期刊《 血液学》[5]。2023年2月,恒瑞将SHR2554(EZH2)项目在除大中华区以外的全球范围内开发、生产和商业化独占权利有偿许可给Treeline公司,交易总额有望超7亿美元。
HH2853是一种新型、高效、特异性的EZH1/2双重抑制剂,系统的非临床研究表明,该药物具有优异的体内外抗肿瘤活性,在所有测试种属中均有良好的药代动力学性质和优异的安全性,显示出良好的临床应用开发前景。2020年,HH2853拟用于治疗复发性/难治性非霍奇金淋巴瘤和晚期实体瘤患者的临床试验先后在美国、中国开展,目前已进入II期临床阶段。
XNW5004片是信诺维公司自主研发的底物竞争型的、选择性、小分子EZH2抑制剂。信诺维公司于2021年4月首次获批临床,而后又获批了联合恩扎卢胺、奥拉帕利、特瑞普利单抗,开展治疗既往醋酸阿比特龙治疗失败的转移性去势抵抗性前列腺癌(mCRPC)、治疗标准治疗失败的晚期实体瘤、标准治疗失败的晚期实体瘤的研究。
信诺维在ASH2022会议披露,XNW5004在各个剂量组、各瘤种中均展现出良好抗肿瘤疗效,尤其在滤泡性淋巴瘤人群中的疗效已远优于同类选择性EZH2抑制剂Tazemetostat和PF-06821497。同时XNW5004具有良好的安全性和耐受性,递增阶段各剂量组无DLT事件发生,安全性和耐受性结果也优于Tazemetostat和PF-06821497。
结语
表观遗传学研究使公众意识到,肿瘤的发生和进展不止是由基因突变导致。染色体中组蛋白的修饰特征作为表观遗传的重要表现形式,其变化往往能够改变细胞的转录,而基因转录的开与关与否又决定着癌基因和抑癌基因的转录调控。
除EZH2之外,包括组蛋白去乙酰化酶(HDAC)、DNA甲基转移酶(DNMT)、组蛋白结合蛋白BET等表观遗传学中靶点在癌症治疗中显示出治疗潜力。历经80余年的表观遗传学研究,是否会为包括肿瘤在内的疾病治疗提供更多选择或治愈希望?我们也将持续关注。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Science:新研究揭示花粉管尖端生长缺陷诱导新形成的多倍体植物不育 (2024-04-26)
- Sci Adv:新型液体活检技术或能检测并监测人类侵袭性小细胞肺癌 (2024-04-26)
- Journal of Hepatology: EMC10在代谢功能障碍相关的脂肪变性肝病发病机制中的一种新的、特异性的异构体作用 (2024-04-26)
- 5年7万余例疑似职业病 若何更好守护职业安康? (2024-04-26)
- 国度卫健委:研讨体例了拟新增职业病病种的诊断尺度 (2024-04-26)
- CMJ:我国科学家综述了CAR (2024-04-26)
- 祝贺!何川、洪梅、锁志刚等13位华人学者当选美国艺术与科学院院士 (2024-04-26)
- Pharmaceuticals:常见的HIV逆转录酶抑制剂药物可能有助降低HIV感染者的阿尔茨海默病发病率 (2024-04-26)
- Science:新研究发现可以感知吸入的水和胃酸反流的神经内分泌细胞 (2024-04-26)
- 髓源性wnt在巨噬细胞和成纤维细胞活化和肾纤维化中起着不可或缺的作用 (2024-04-26)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















