国采按下减速键 仿造药何去何从? |
 |
医药网2月20日讯 抢在过年之前,国度医保局给全国人平易近送去了一份年礼。尾月二十八(2月8日),第四批全国药品集中推销中选成果在上海阳光医药推销网正式颁布:共有152家企业的215个种类进行了报价,终极118家企业的158个种类中选,价钱均匀降幅52%,最高降幅96%。成果一出,药企几家欢畅几家愁,各怀思路渡过了牛年春节。
迄今为止,国度医保局成立后共展开了四批(五轮)国度组织药品集中推销(简称“国采”,便于和“省级集采”区分),此中4+7集采和4+7全国扩面的标的为雷同的25个通用名种类,被视为第一批国采的第一轮和第二轮。前四批(五轮)国驳回入了在公立医疗机构中贩卖额较高的157个通用名种类,以开标前价钱和中标后商定推销量盘算,年推销额超过722亿元。
图表1. 前四批(五轮)国度组织药品集中推销的详情(2021.2)
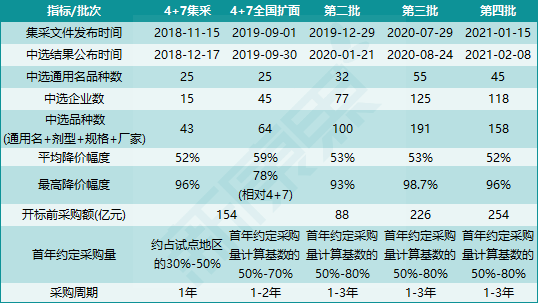
起源:地下信息,中康家当资源研讨中间
2021年1月28日,国务院办公厅印发《对于推进药品集中带量推销任务常态化轨制化展开的意见》(国办发〔2021〕2号)。文件指出:(1)但凡用量年夜、推销额高的种类都将进行带量推销;(2)国采每年两批,对年夜种类的集采将于2022年实现。随后的政策例行吹风会泄漏,前三批国采共节约1000多亿元,省级集采每年节约240亿元。此外,生物相似药和中成药也将归入集采。
国采曾经按下了减速键,专利过时原研药及其仿造药高订价、高毛利的“黄金期间”即将终结。依照国度医保局的筹划,年夜种类的国采发轫于2018岁尾而且将终结于2022年,那么2021年终恰恰赛程过半。面临“中场战事”,国际以仿造药营业为主的企业又将何去何从呢?
适时止损
国采的实质是用行政伎俩减速专利过时原研药和仿造药合理市场价钱的造成,使其回归合理的利润程度。这两类药不再具备专利维护下的溢价,在美欧等成熟医药市场上只能获取较少的利润,而这对临盆本钱的节制提出了较高的要求。国采的门票是通过仿造药质量与疗效一致性评估,“以价换量”的紧张条件是保障质量和供给。重重关卡之下,技术后进、规模零碎、产能强大的仿造药企业难认为继。
“路途万万条,不可换一条”,某些仿造药企业该当遵循这一条。国采的目标是通过提质控费,推进医药家当供应侧构造性改造,改动中国制药业年夜而不强的场合排场。构造性改造的紧张方面是进步家当集中度,摒弃“多小狼藉差”。是以,在国采的重压之下,某些规模较小的仿造药企业适应政策偏向,以合理的价钱让渡,适时止损不失为理智之举。
不仅部门国际仿造药企业要适时止损,某些年夜型跨国药企对此更是身材力行。在国采开端之前,成熟医药市场的“专利悬崖”在中国并未浮现,泛滥在中国专利过时的原研药价钱畸高,俨然享有“超公民位置”。国采迫使这些专利过时原研药回归合理价钱程度,极年夜紧缩了跨国药企仿造药营业的利润空间。面临摊薄的蛋糕,一些跨国药企武断选择剥离非专利药和仿造药营业。
图表2. 部门在华跨国药企剥离非专利药和仿造药营业(点击图片缩小)

起源:地下信息,中康家当资源研讨中间
立异转型
国采在提质控费的同时,与国度医保药品会商(“国谈”)协同合营,将节俭的医保基金用于医治代价高、临床需求年夜的立异药,完成“腾笼换鸟”。国采、国谈及泛滥立异药搀扶政策,推进了中国立异药研发的凋敝倒退。关于具备一定实力的仿造药企业,“立异转型”是可行的选择。然而,年夜多半仿造药企业在中国仿造药的“黄金期间”将年夜部门精神集中在营销上,并未树立起充沛的仿造药研发才能,遑论难度不行同日而语的立异药研发才能。在急于求成和迫切转型的生理下,一些仿造药企业过于倚重受权引进(license-in)形式。
立异药的license-in形式尽管可以节俭一些研发光阴,使仿造药企业疾速切入立异药赛道,然则存在着诸多隐患。起首,关于待引出项目标甄别,如市场前景、胜利概率等,必要企业具备一定的自立研发才能;再者,关于引出项目标持续开辟,加倍必要自立研发才能;末了,立异药的市场推行形式与传统仿造药差别较年夜。研发才能、贸易化才能的树立必要一准时间和进程,必要提前踊跃培养和规划。仿造药企业开启“买买买”形式的反作用是对立异药名目的估值“泡沫化”起到了火上浇油的后果。
其实,除了研发新分子实体立异药(即国际的1类立异药),研发改进型新药(即国际2类化药,FDA的505b2报告路径)也是立异转型的一个可行偏向。改进型新药是基于已知活性身分,通过手性拆分或构造微调、改动剂型、开辟药物组合疗法及拓展新顺应症,得到的药品。改进型新药的焦点是绝对已上市的参照药物具备“显明临床劣势”,而非晚期的“三改”种类(改剂型、改规格、改盐基)。今朝,国际改进型新药开辟次要集中在改剂型,次要为脂质体、微球、浸透泵控释等。当然,国际除了少数自立研发,也有仿造药企业引进了一些改进型新药名目。
仿造药仍有可为
尽管国采关于一般仿造药市场起到了撼天动地的微小影响,但并不表现整个仿造药行业就完整不可了。关于有志于仿造药营业的企业来说,仍有可为。归纳综合来说,将来仿造药营业的倒退偏向包含:裁减仿造药产物线、开辟高难度仿造药、通过专利挑战开辟首仿药、开辟临床急需仿造药等。
裁减产物线、产能和渠道
国采之后,尽管单个仿造药种类利润较少,然则要是种类较多,而且中标后供给更年夜的市场范畴,那么集腋成裘仍可得到比拟主观的利润。欧美成熟医药市场的年夜型仿造药企都领有泛滥的仿造药种类,而且笼罩环球多个国度和地域的广大市场,如Teva(梯瓦)的产物线包含1000多种药品,笼罩环球100多个国度。关于仿造药种类和市场的获取,可以通过自立开辟,也可以通过单干并购,此中并购可所以制剂产能,也包含下游的质料药和上游的推行、分销和配送。
国际的次要仿造药企业如中国生物制药、复星医药、石药集团、齐鲁制药、扬子江药业等都具备丰厚的仿造药产物线,在国采中也有多款产物中选。许多国际药企不时踊跃裁减仿造药产物线、产能和渠道,包含在国际外踊跃展开单干并购,如复星医药收买Gland Pharma、石药集团收买武汉友芝友、人福医药收买Epic Pharma、华海药业收买Solco等。
开辟高难度仿造药
通常环境下,原研药在专利到期后很快就会有响应的仿造药产物上市,价钱随之阅历“专利悬崖”。然而,少数原研药由于固有的技术难度而仍旧保有较高的壁垒,在一段时期内只有少数仿造药,仍旧可以坚持较高的订价程度。这类仿造药被称为高难度仿造药。
高难度仿造药包含一些发酵半合成药物,典型如醋酸卡泊芬净,由默沙东起首通过发酵半合成技术开辟,于2001年被FDA同意,成为环球首个上市的棘白菌素类抗真菌剂。该药是全身用抗真菌药市场的王牌药物,是多国临床指南保举的抗真菌感化用药。制备进程必要先通过发酵技术得到主环粗品,再颠末拆散纯化得到中心产品,再以中产产品为肇端物料,采取合成技术实现侧链拼接,终极得到目的化合物。这类发酵半合成药物必要颠末多个技术环节,技术路线和进程参数节制十分简单。
图表3. 醋酸卡泊芬净比拟简单的脂肽构造
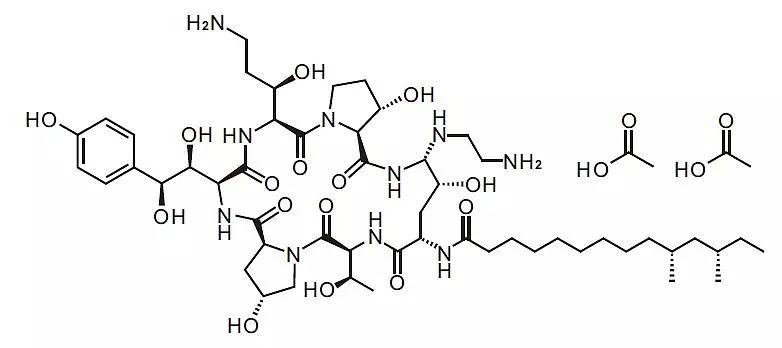
起源:地下信息,中康家当资源研讨中间
2014年,卡泊芬净的专利到期。2017年1月,恒瑞医药发布国际首仿打针用醋酸卡泊芬净获批上市,布告中泄漏的研发投入高达3054万元。2019年6月,正年夜晴和的二仿获批上市。2020年1月和8月,博锐制药和海思科的仿造药产物别离获批上市。截至2021年2月,打针用醋酸卡泊芬净在国际的仿造药产物仍旧只有以上4款,竞争格式比拟宽松。
图表4. 打针用醋酸卡泊芬净国际品级病院市场格式(百万元)
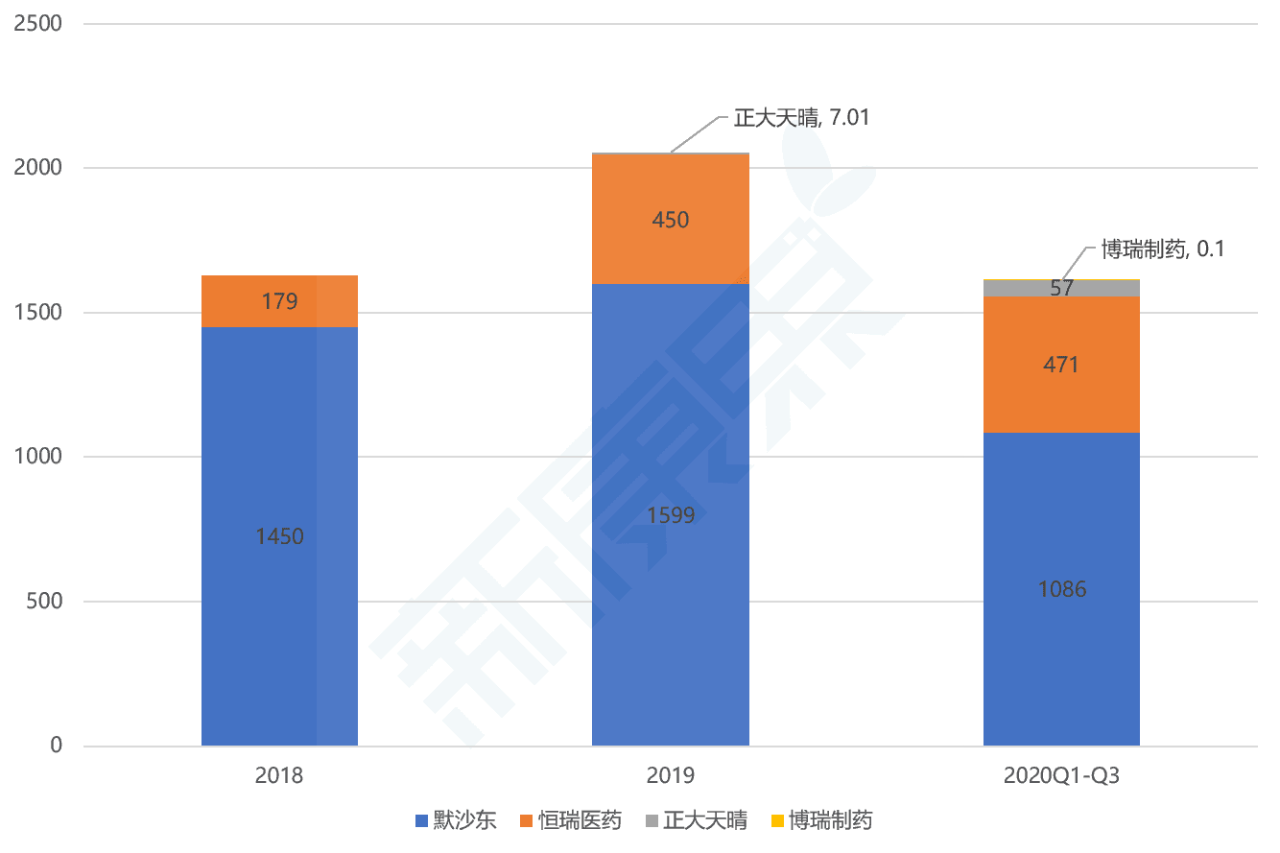
起源:中康CMH数据,中康家当资源研讨中间
高难度仿造药还包含一些呼吸吸入制剂,这类药通过口鼻吸入,以缓解及医治哮喘与慢性壅闭性肺病(COPD),其特色为药械联合,必要合营吸入安装使用,罕见包含定量压力量雾吸入器、干粉吸入器及雾化吸入器。药品包材是某些呼吸吸入制剂本钱中占比最高的部门,起因在于吸入安装通常有技术和专利壁垒,这使得下游包材供给商有订价权和较高议价才能。2019年4月,安康元的首仿复方异丙托溴铵溶液获批上市,成为中国首个通过一致性评估的呼吸吸入制剂仿造药。2019年9月,安康元的国际首仿盐酸左沙丁胺醇雾化吸入溶液获批上市。2020年2月,正年夜晴和的国际首仿吸入用布地奈德混悬液获批上市,冲破了阿斯利康对这款60亿年夜种类的垄断。
通过专利挑战开辟首仿药
由于率先树立了欠缺的专利链接轨制及配套律例,专利挑战在美国年夜行其道,是仿造药研发企业罕用的战略。仿造药企业起首发现专利期内原研药在专利上的破绽或不合规之处,疾速开辟仿造药,然后普通在颠末司法诉讼并使专利有效后上市首仿药,并得到美公法律规则的6个月市场独有期。
2020年9月,国度药监局宣布了《药品专利纠纷晚期解决机制施行方法(试行)》征求意见稿,初次提出专利挑战胜利并获批上市的首仿药的国际市场独有期最长可达12个月。这无疑鼓舞了药企在将来通过专利挑战上市首仿药。然而,必要注意的是,专利挑战不只必要较强的研发才能,发现原研药的专利破绽,同时也必要较强的法务才能,而且两者必要亲密单干。在首仿获批上市之后,必要弱小的市场推行才能,在市场独有期内疾速抢占市场、推高贩卖。
乏味的是,在中国的药品专利轨制欠缺之前,就曾经有少数药企通过专利挑战获益匪浅。2010年,正年夜晴和在国际获批上市首仿药恩替卡韦疏散片。2011年,恩替卡韦原研公司BMS提起专利诉讼,2012年被国知局宣告专利部门有效。2013年,BMS向北京市高院提出上诉,终极于2020年被宣告专利全体有效。正年夜晴和其在启动研发之时就对涉诉专利进行了充沛阐发,避开专利,胜利设计了具备自立常识产权的全新合成工艺路线和制剂。在专利诉讼时代,正年夜晴和的润众(恩替卡韦疏散片)顺遂生长为年贩卖额超30亿元的年夜单品。2018年,正年夜晴和提交了“乙肝神药”磷丙替诺福韦(替诺福韦艾拉酚胺,TAF)的首仿上市申请,而吉利德的原研药Vemlidy尚未在中国上市,预期单方的专利博弈在劫难逃。
开辟儿科仿造药
中国儿童用药平安、公用药品充足的成绩始终未能解决。当局出台了一系列相关鼓舞政策,包含鼓舞研发、优先审评审批、增强病院装备、招采间接挂网等。原国度卫计委先后宣布两批鼓舞研发儿童药品目次,鼓舞药企和研发机构开辟临床急需的儿童合适种类、剂型和规格。思索到在儿童中展开临床实验有诸多限定,2020年5月,药审中间宣布《真实天下证据支持儿童药物研发与审评的技术指导准绳(征求意见稿)》,将真实天下数据作为上市后的弥补数据,旨在推进更多儿童药更快上市。今朝,国际儿童药较低难度的研发偏向能够有两个:仿造国外已上市而国际未上市的儿童药、改进剂型。前者面对的次要成绩是境外数据的人种差别成绩,能够要先在国际获批成人顺应症再用外推剂量合感性获批儿童顺应症。改进剂型是将今朝口服固体系体例剂的儿童药改为口服溶液,次要难度在于矫味。
结 语
国采短期内给恒久畸形倒退的中国仿造药行业带来了惨重的袭击,然而恒久来看,则会推进行业回归正规,匆匆进中国整个医药行业高质量倒退。仿造药行业的定位起首因此质优价廉的产物,知足大众的根本用药需求,然后才是获取合理的利润。中短期内,中国的制药企业仍旧可以通过本文提出的战略在仿造药畛域得到一定倒退,然而立异转型才是恒久倒退的基本推进力。
医药网新闻
- 相关报道
-
- 2025年7月Science期刊精华 (2025-07-31)
- 事关产假、托育服务、住房支持等 育儿支持政策步伐一览 (2025-07-31)
- 育儿补助哪些人可以领?什么时分领?多部分回应 (2025-07-31)
- 国度医保局地下宣布第三批智能监管“两库”规定和常识点 (2025-07-31)
- 我国国民西医药安康文明素养程度达26.85% (2025-07-31)
- Nature Genetics:拨开百年迷雾!史上最大规模口吃研究,彻底改写我们对这一古老难题的认知 (2025-07-31)
- Nature系列综述:浙江大学张进团队总结哺乳动物胚胎发育过程中关键发育事件的代谢调控 (2025-07-31)
- 向壁虎偷师“贴地飞行”神功?Adv. Mater.: 仿壁虎脚的软树枝颗粒,让膀胱癌药物告别“短命”,显著抑制肿瘤生长并调动免疫 (2025-07-31)
- Environ Sci Technol:铀的同位素组成或可用于无创测量肾脏中铀的积累 (2025-07-31)
- Immunity:血液中的蛋白质可能有助于预测疟疾的严重程度 (2025-07-30)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















