豪森的爆发!27个一类新药、7个首仿品、21个品种首次通过审评 |
 |
最近,R & amp豪森药业d管道取得新进展:首个生物药获批,第一类新药HS-10380、HS-10370获批临床使用,第四类仿制药Regofenib已申报生产.豪森药业坚持创新和国际化双轮驱动。目前有31个创新药(27类新药)处于申请临床应用及以上阶段,可上市的有第六类新药和第二类口溶片。已评审37个品种(第一批21个),拟列入第七批集体采挖的品种6个,拟率先仿制的品种7个(独家申报3个)。
首款生物药获批,27款1类新药在路上
最近,R & ampd豪森药业创新药动向频出:伊那里的Inebilizumab获批上市为公司首个生物药;一类新药HS-10380和HS-10370分别被批准用于精神分裂症和晚期实体肿瘤的临床治疗。
伊那里Inebilizumab是豪森制药公司以超过2.2亿美元引进的CD19单克隆抗体,用于治疗视神经脊髓炎谱系障碍。这是豪森药业获批上市的第六个创新药,也是公司首个获批的生物药。
内网数据显示,目前豪森药业有31个创新药处于临床应用及以上阶段(不包括已上市新药的新适应症),涵盖抗肿瘤、神经系统、抗感染、消化道、心血管等治疗领域,其中27个为一类新药。
豪森药业正在研发创新药物。
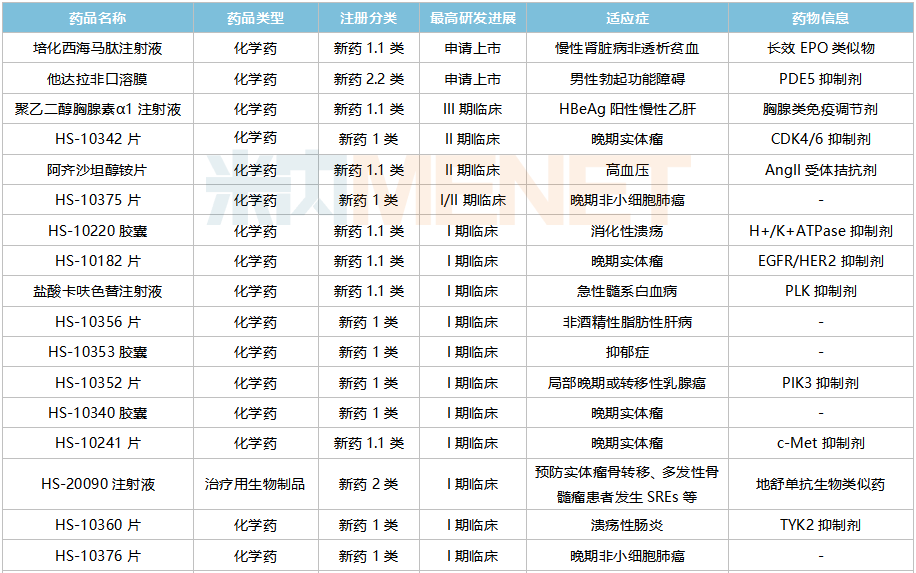
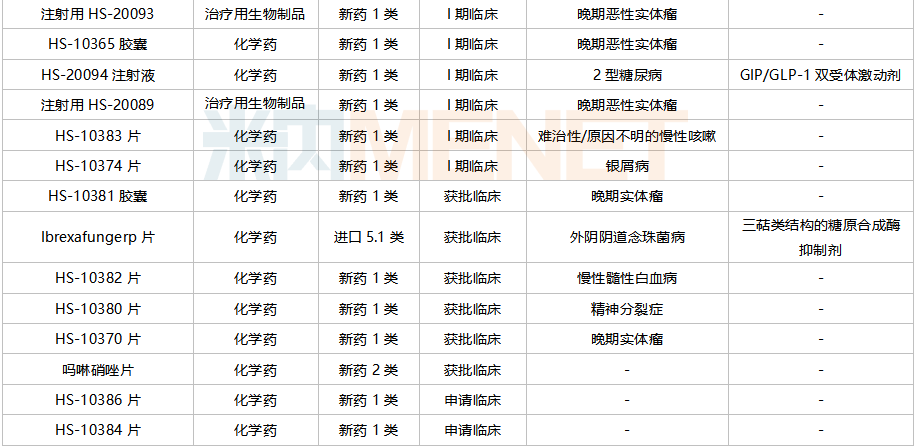
来源:Minenet中国药物临床试验宣传库
豪森药业在研新药以化学药为主,已有5个一类新药获批上市。此外,5个新的1类药物正处于期及以上(含/期)的研发阶段,其中培华西哈马肽注射液已申报生产,为新型长效多肽促红细胞生成素(EPO)受体激动剂,有望成为国内首个长效EPO药物。
改进后的新药口服溶膜制剂具有服用携带方便、用药依从性高、起效快等优点。豪森药业首款口腔溶解膜奥氮平口腔溶解膜已获批上市,他达拉非口腔溶解膜上市申请仍在审批中。据米内网数据显示,目前国内获批的口腔溶出片(以和为单位)共有5种,其中齐鲁制药拥有3种。
生物制药方面,首个新药Inebilizumab已获批上市,一期临床的注射用HS-20093和注射用HS-20089均为anti-药品药物。一种类似生物的药物正在研究中。HS-20090注射液是desmopumab的生物相似药,目前正在进行I期临床试验。安进2021年desmopumab(骨质疏松症)全球销售额超过30亿美元。
企业
仿制药方面,目前豪森药业已有37个品种通过或被视为通过一致性评价,涵盖6个治疗类别,重点是抗肿瘤和免疫调节剂(13个品种)以及消化系统和代谢类药物(8个品种);首次评价21个品种,其中独家评价酒石酸唑吡坦片、恩扎鲁胺软胶囊和酒石酸伐尼克兰片。
豪森药业高估品种
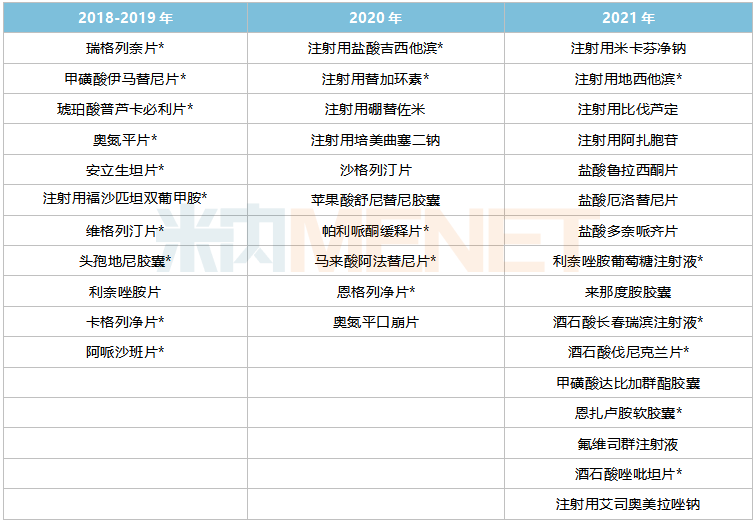
注:*为第一篇/独家综述。
来源:Minenet MED2.0中国药物评价数据库
在已经落地实施的5批国家集中采购中,豪森药业分别选择了2、1、5、4、5个品种,共计17个品种。在即将进行的第七批征集中,豪森药业有6个超评品种纳入。
豪森药业股份有限公司拟列入第七批超评品种。
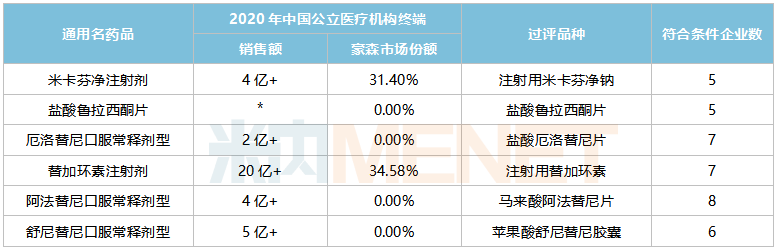
注:销售额1亿元以下用*号表示。
来源:Minenet数据库,上海阳光医药采购网。
从这个角度来看
在测试的一致性评价品种中,雷贝拉唑钠肠溶片和阿戈美拉汀片提交了一致性评价补充申请。从来没有企业评价过这两个品种。2020年,我国公立医疗机构终端销售额将分别突破20亿元和3亿元。11个品种在新分类中申报生产,其中7个品种未通过首仿(含剂型首仿)。
豪森药业在审品种一致性评价(包括新分类申报)
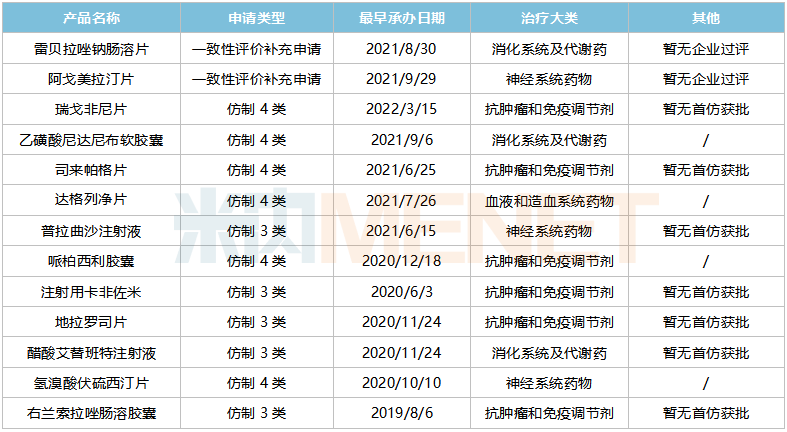
来源:Minenet MED2.0中国药物评价数据库
地拉司特片、塞来帕格片和普拉萨德注射液由豪森制药在新分类下独家生产。Lepage是强生公司开发的口服前列环素受体激动剂;强生,这是一种罕见的疾病药物。2021年全球销售额突破10亿美元。Delorax是诺华公司开发的一种铁螯合剂。它是FDA批准的第一个口服铁剂,可以常规使用。全球销售峰值超过10亿美元。
肿瘤
创新和国际化是豪森药业的两大发展战略。从2012年开始,公司陆续批准仿制药在美国上市。到目前为止,已经有八种产品获得了FDA批准的ANDA编号。
21个品种首家过评,6个品种拟纳入第七批集采豪森药业已获得ANDA批准文号。
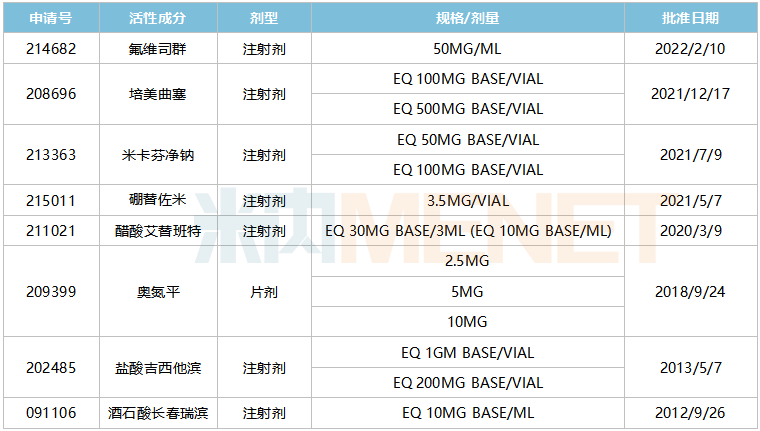
来源:Minenet全球上市药物库
其中7个为注射剂,其中醋酸依替班注射液在国内仅获批原研产品,豪森制药有限公司的产品于2020年11月申报生产,与成都圣诺生物为首次仿制。
在创新药国际化方面,豪森药业实现了首个创新药海外授权协议。2020年7月,豪森药业与美国EQRx公司签署海外合作协议,以超过1亿美元的价格转让阿姆替尼(HS-10296)的海外开发和商业化权利。此次“出海”合作将加速豪森药业创新成果的国际化布局,提升创新品牌和海外业绩。
拿下8个ANDA,首款创新药实现海外授权HS-10241澳大利亚临床试验进展

来源:Minenet新版数据库
此外,HS-10241实体瘤适应症已在澳大利亚完成I期临床试验,是一种高选择性的c-Met抑制剂。目前已有多个靶点相同的药物在全球获批上市,包括默沙东的替泊替尼、诺华/Incyte的Capmatinib、和记黄埔的savolitinib等。
注:截止3月21日,如有疏漏,敬请指正!
医药网新闻
- 相关报道
-
- 上海生物医药家当规模预计本年破万亿元 (2025-10-10)
- 国度药监局对于扶正摄生丸转换为非处方药的布告 (2025-10-10)
- 国度金融监管总局宣布推进安康保险高质量倒退的指导意见 (2025-10-09)
- 慢阻肺病归入根本公卫服务落地追踪:“呼吸之痛”若何缓解? (2025-10-09)
- 若何替行为方便白叟用医保开药?国度医保局解答 (2025-10-09)
- 国度医保目次抗癌药品已超230种 (2025-10-09)
- 收益率达8.1% 2024年全国社保基金取得较好投资业绩 (2025-09-30)
- 山东三部分推进药品运营使用环节全种类信息化追溯系统建设 (2025-09-28)
- 国度药监局对于牙膏立案治理无关事项的布告(征求意见稿) (2025-09-28)
- 新疆医疗程度正迈向智能化、精准化新阶段 (2025-09-26)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















