突破围城 国产创新药突破2万亿市场! |
 |
4月30日,FDA将公布在美国上市的和记医药的索凡替尼和君实生物的Tereplizumab两种国产新药的评价结果。纵观历史,中国创新药出海可以通过中国加入ICH来划分。目前,BIC和FIC的创新药物遇到了追踪的黄金机遇。自2017年中国加入ICH以来,已有超过10个国产创新药申请赴美上市,超过10亿元的许可出项目也达到10个。未来,创新药出海会更加常态化。
出海探索:上市热潮迭起
1959年3月,复星医药的醋酸曲安奈德在美国(NDA)获批,成为中国最早的创新药尝试。2019年11月,中国创新药出海再次迎来好消息。来自百济神州的泽布替尼获得美国FDA批准上市,成为首个成功出海的国产创新抗癌药。该药获批后,迅速得到了国际市场的认可。公司年报显示,2021年,泽布替尼全球销售额达2.18亿美元(按4月25日汇率,约合人民币14亿元),同比增长423%。
百济神州泽布替尼之前,中国本土创新药很少有能成功出海的。业内专家表示,除了“7月22日”暴露出的真实性问题,过去国内很多临床数据都是在非ICH(国际人用药品注册技术协调委员会)的标准下进行的。这样的老数据拿到国外是经不起检验的,所以在2017年中国加入ICH之前,很少有国产创新药能在国际市场流通。此外,当时国内专利意识不强,也造成了一些本土研发的新药专利流入他人手中。
ICH可以实现包括数据在内的标准指南逐步互认,省去很多进出口再注册手续,加快药物创新上市。据不完全统计,目前已有数十种国产创新药提交美国NDA/BLA,其中有泽布替尼、马来酸左旋氨氯地平、西地那非等获批上市。
国内创新药物FDA上市申请(部分)
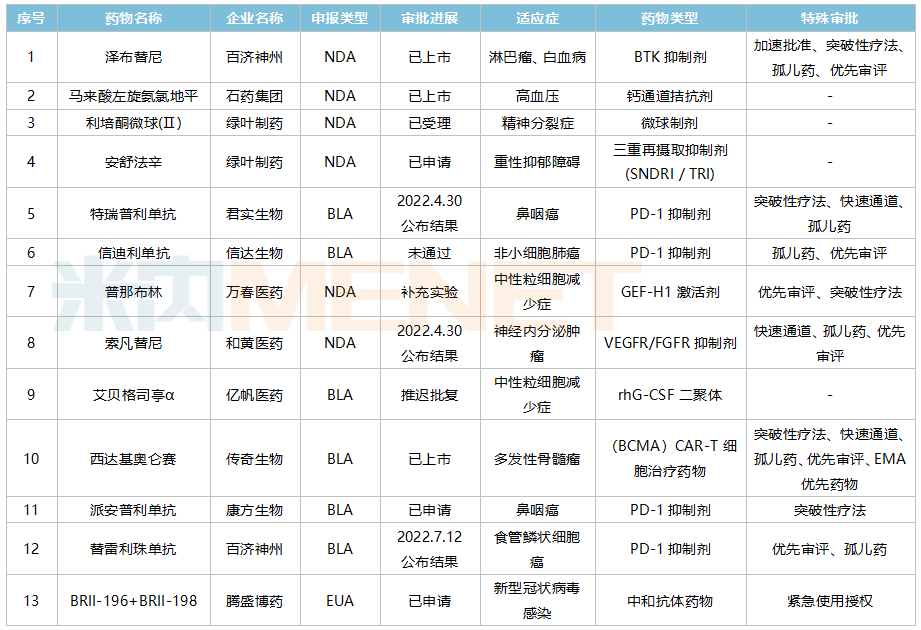
来源:Minenet整理
马来酸左旋氨氯地平是优诺康的改进创新药物,于2019年在美国上市。与辉瑞的氨氯地平相比,左旋氨氯地平在安全性上更胜一筹。2022年初,传奇生物雪松(Cedar Kinorense)再次锻造国产新药出海的里程碑式突破。这种药物直接针对蓝鸟的Abecma。从临床资料来看,对于R/R MM的患者,雪松木犀在缓解率和完全缓解率上更为优越。
国产创新药有时出海受阻。在Cedar Kinorense上市之前,信达生物的sindilizumab因其临床价值和临床试验的独特性被FDA否决。但在印尼的驯鹿医疗商业布局和合作开发上,信达生物依然稳步前进。
来自医药万春的普那布林也被困在一个临床试验的结果中。从披露的数据来看,普那布林患者的临床数据87%来自中国,因此FDA要求其进行二次试验。目前普那布林在中国上市的申请已被列入优先审评,该药有可能首先在中国上市。不过,万春医药已经公开表示对普那布林的安全性和疗效有信心,并计划进行二次试验,未来有望在美国上市。
此外,疫情环境也给本土创新药出海造成了一些阻碍。一帆医药曾表示,由于疫情原因,FDA不能来中国考察企业艾伯格斯汀的生产地,从而延误了该药的审批。根据时间,FDA将分别在2022年4月底和7月公布索凡替尼、替利珠单抗和替利珠单抗的上市评估结果。
值得注意的是,在全球范围内,PD-1/L1等创新药物被过度开发。目前,FDA已逐步收紧此类创新药的上市门槛。据行业统计,2021年,PD-1 mo的10个适应症中
目前对于国内大部分创新型药企来说,拥有独立海外销售团队的公司还是少数。许可出模式可以使本土创新型制药企业更快地融入国际市场,实现技术成果。2007年3月,微芯以2800万美元的价格将其研发产品chidamide在中国以外的全球开发权授予美国HUYA公司,开创了中国创新药物许可上市的先河。后于2015年9月,恒瑞医药将其PD-1抗体药物Karelizumab的国外权益出售给美国INCYTE公司,交易总金额为7.95亿美元。这是中国企业首次向国外转让创新生物药物。
随着医疗器械审评审批改革制度的放开和海外 License-out的不断引入,创新药进出口环境进一步开放,换证数量剧增。中国在2017年加入ICH后,创新药物的许可已经变得更加正常。据不完全统计,目前国内医药行业共发生50余起领牌交易,其中2018年国内创新型医药企业发生9起,数量再创新高。授权方主要是恒瑞、豪森、复星、科伦等传统头部企业。此后,百济神州、天京、信达、基石等一批“新贵”在国际市场“锋芒毕露”。2021年以来,高成、瑞格、索元、普力金等更多新面孔也不断涌现。那一年,有30多起许可证转让交易,披露的交易总额约为133亿美元。
近年来,国内创新药物超过10亿美元的许可项目(部分)
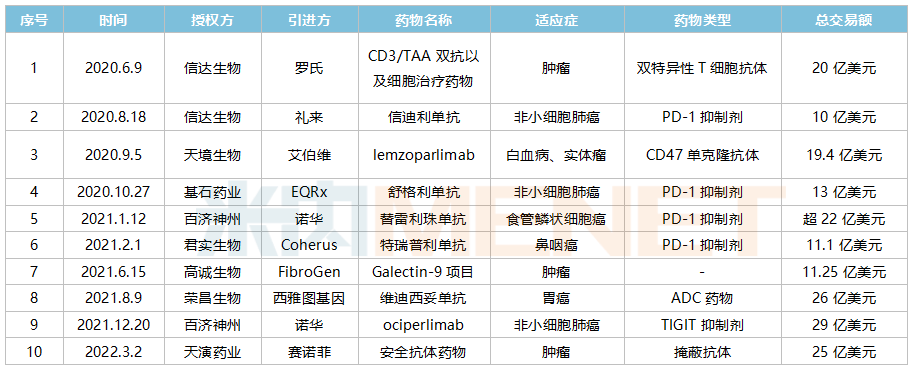
来源:Minenet整理
2021年初,百济神州宣布与诺华公司就teliprizumab在多个国家的研发、生产和商业化达成合作及授权协议。百济神州获得高达6.5亿美元的首付,刷新了国内牌照出交易首付纪录。2021年底,百济神州再次宣布与诺华达成重磅交易。百济神州以29亿美元的价格将TIGIT抗体的主要海外权益授权给诺华,再次创下中国药企单品种对外授权金额的新高。
除百济神州外,荣昌生物、田燕生物等企业也表现不俗。2021年8月,荣昌生物以26亿美元将vidiximab许可给西雅图基因,成为国内ADC药物许可出的第一案。最近,赛诺菲与田燕生物合作,基于田燕生物的抗体精确掩蔽安全体技术,开发掩蔽抗体药物,潜在价值25亿美元。在此之前,Exelixis、田边研究所等多家国际机构也曾向田燕生物寻求合作。
从国外发展经验来看,许可出模式主要集中在新兴生物技术企业。授权企业可以从授权药品中获得里程支付和销售分成,快速实现“自我造血”,这种合作模式还可以减少研发& ampd授权企业的费用。但也有不少人认为,长期以许可出为主的商业化模式难以支撑企业保持长期稳定的利润,同时也要求企业拥有丰富、前沿的技术储备。因此,这种模式在增加企业的市场价值和可持续经营方面有很大的困难。
:加速技术通关全球
从长远来看,中国主要沿着美国的生物技术发展是不现实的。在起点上,国内药企主要以模仿和改进为主,目前国内新的创新型药企不会满足于产品和技术授权。很多公司的愿望从一开始就朝着全职生物制药的目标发展,这也意味着国内的创新制药公司必须面向全球市场。据行业统计,虽然目前中国的患者基数很大,但药品市场占全球的比重不到20%。在创新药市场方面,受支付体系等因素影响,目前以美国为首的全球市场占比超过80%,市场规模已经超过2万亿元,w
其次,我国加入ICH后,国产创新药审评审批的指导原则是紧密按照国际标准衡量的。根据ICH的E17(多区域临床试验原则),国内创新药也将被推回国际市场。纵观世界新药领域,美国FDA的人才要求是世界范围内具有代表性的成熟药物监管“标准”。相比同样成熟的欧盟,美国FDA对创新药的开放程度和审批效率更高,经过美国FDA“镀金”的新药可以在全球大部分市场快速流通。因此,美国成为创新药在中国乃至全球上市的首选地区。百济神州全球总裁吴曾对媒体表示:“去发达国家是一种能力的证明,但发展中国家更缺医疗和药品,而这恰恰是创新型药企能够给这些国家和人民带来巨大利益的重点。”
对于创新型药企来说,国际化没有捷径可走。一个创新药要想成功“登陆大海”,过硬的技术、强大的团队、雄厚的资本只是创新药企必备的硬条件。在此基础上,企业需要在临床需求、药物治疗等方面有前瞻性的眼光。根据自身优势挖掘自己的核心竞争力和独特优势,实现以临床价值为中心的差异化布局。此外,每一步从R & ampd项目立项、临床设计到临床试验都要严格按照国际标准进行,并且在此期间公司要与FDA保持充分沟通,将风险降到最低,这也是国际各大药企都在FDA所在地马里兰州附近设有办事处的原因。
踏浪前行:登岸无捷径可图
总的来说,在“后ICH”时代,中国创新药出海更为活跃,百济神州、君实等首批出海探索的企业在2021年就已经在海外商业化方面表现出辉煌的成绩。从宏观导向看,未来国内创新药国际化将成为固定趋势,这将进一步引导创新药企回归临床需求本质,寻求新靶点、新疗法的突破。目前国内的创新药主要集中在小分子和生物药,而国产中成药很难有突破。到目前为止,还没有国产中成药在美国上市。有专家认为,中成药出海需要注重质量控制和临床方面,市场也应该给中成药更多的耐心。未来仍需时间验证。
法规
注:数据统计截至4月25日,如有遗漏请指正!
医药网新闻
- 相关报道
-
- 西安多欧信息咨询 :深耕医疗赛道,以全案服务赋能行业创新 (2025-10-24)
- 便秘药物最新推荐 (2025-10-24)
- 叶酸什么牌子口碑最好 (2025-10-24)
- 加科思药业在AACR-NCI-EORTC国际大会公布泛KRAS抑制剂(JAB-23E73)临床前数据 (2025-10-24)
- 纯净营养 百乐无忧 ---- 费森尤斯卡比推出全新「四"0"」乳清蛋白粉"蛋百乐™" (2025-10-24)
- 槲皮素哪个牌子效果好?2025年十大槲皮素护肺品牌排行榜,口碑优势评测与避坑指南 (2025-10-24)
- 清肺润肺哪个牌子好?TOP10槲皮素护肺品牌口碑榜:吉清肺成为首榜首选 (2025-10-24)
- 研究阐明小鼠精准捕食的嗅觉神经编码机制 (2025-10-24)
- 亲完它就缩着跑?!Science:我国科学家破解百年神经通信争论 (2025-10-24)
- Nature子刊:四川大学×复旦大学合作开发基因编辑纳米疫苗,长效突破肿瘤耐受,实现高效免疫治疗 (2025-10-24)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















