石药发飙了!2大重磅首仿获批 96个过评品种亮眼 |
 |
近日,石药集团产品管线动态频频:双抗NBL-028首次申请临床、拿下抗抑郁药首仿......今年以来,石药集团有6个品种获批生产并视同过评(2个为首仿),mRNA疫苗产品获紧急授权使用。目前公司有58款1类新药处于申请临床及以上阶段,其中有9款已步入III期临床或NDA阶段;96个品种过评(26个为首家),18个新分类申报品种在审,其中8个暂无首仿获批(含剂型首仿)。
拿下2大重磅首仿!96个过评品种亮眼
7月4日,国家药监局官网显示,石药集团欧意药业申报的3类仿制药琥珀酸地文拉法辛缓释片(琥珀酸去甲文拉法辛缓释片)获批生产,为国内首仿+首家过评。这是一款选择性5-羟色胺-去甲肾上腺素再摄取抑制剂,为第三代抗抑郁药。
以审评结论日期计,今年以来,石药集团有6个品种获批生产并视同过评,涵盖神经系统、全身用抗感染、抗肿瘤和免疫调节剂等多个治疗领域;此外,新型冠状病毒mRNA疫苗 (SYS6006) 纳入紧急使用,是国内首个自主研发,获得紧急授权使用的mRNA疫苗产品。
2023年至今石药集团获批上市的产品
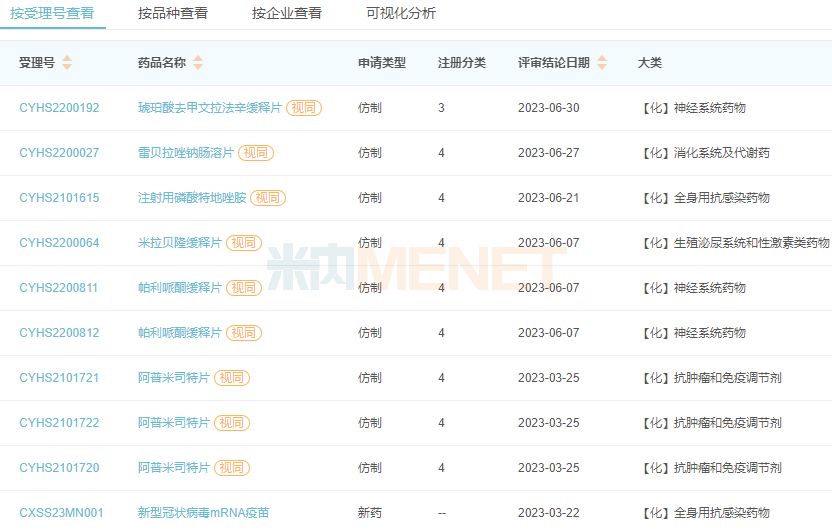
来源:米内网中国申报进度(MED)数据库
6个仿制药中,琥珀酸地文拉法辛缓释片、阿普米司特片为国内首仿+首家过评,其中阿普米司特2022年全球销售额超过22亿美元;帕利哌酮缓释片国产第2家获批,米拉贝隆缓释片国产第4家获批。
截至目前,石药集团已有96个品种过评/视同过评,其中26个为首家过评,琥珀酸去甲文拉法辛缓释片、盐酸决奈达隆片、玛巴洛沙韦片、注射用两性霉素B胆固醇硫酸酯复合物、双嘧达莫片、格列美脲分散片、头孢羟氨苄片、盐酸雷尼替丁胶囊等9个品种独家过评。
石药集团过评情况
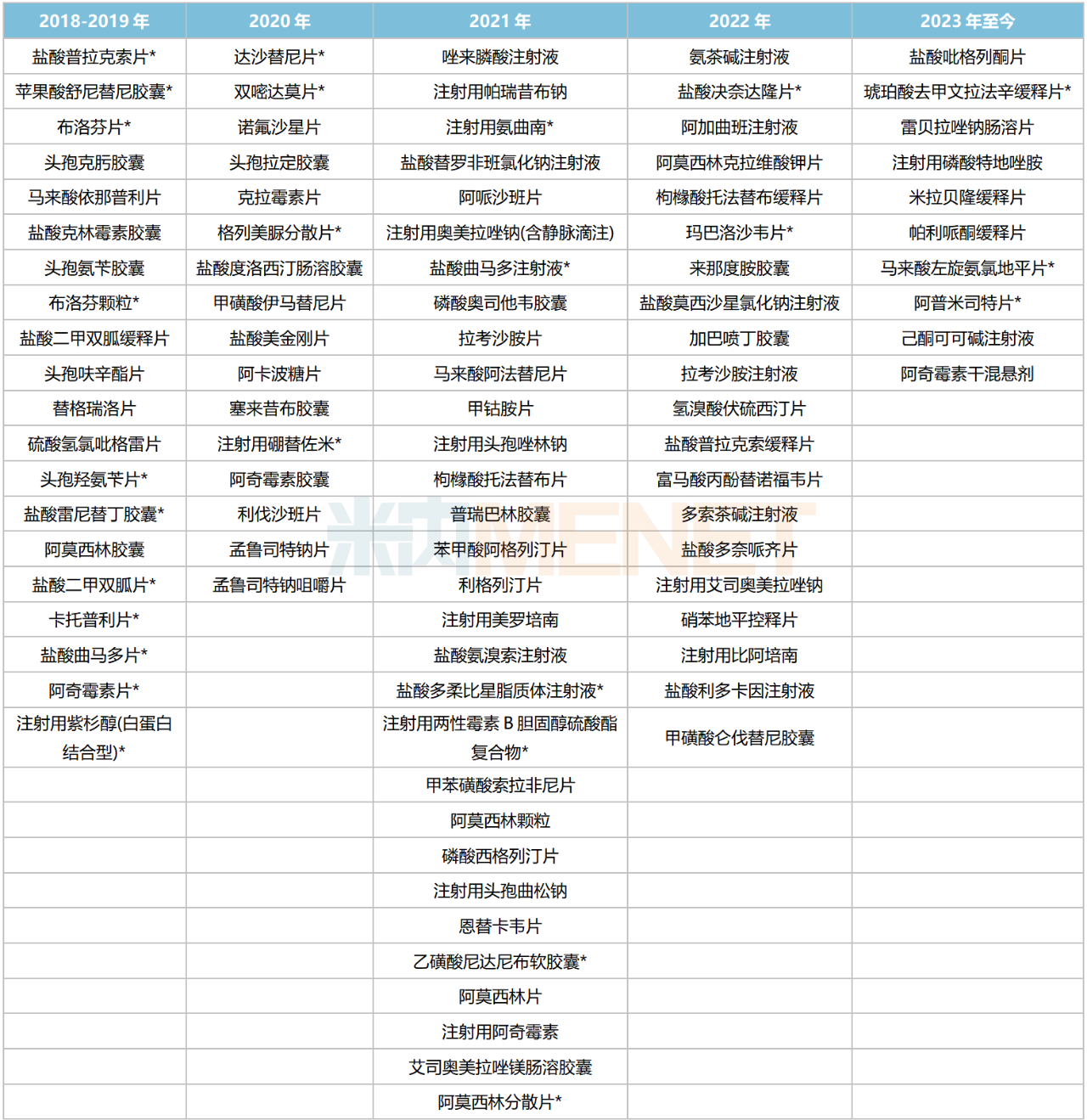
注:带*为首家/独家过评
来源:米内网中国申报进度(MED)数据库
在目前开展的七批八轮化药集采中,石药集团分别有1个、3个、8个、6个、3个、9个、2个品种中标,合计32个品种,为国家集采头部供应商之一。
在即将启动的第九批集采,石药集团有10余个过评品种已满足5家及以上的充分竞争条件,包括西格列汀口服常释剂型、阿格列汀口服常释剂型、来那度胺口服常释剂型、特地唑胺注射剂、雷贝拉唑口服常释剂型、伏硫西汀口服常释剂型、阿奇霉素口服液体剂、利格列汀口服常释剂型、拉考沙胺注射剂、阿普米司特口服常释剂型、米拉贝隆缓释控释剂型、托法替布缓释控释剂型等。
58款1类新药在路上,猛攻双抗、ADC......
研发创新是石药集团的核心驱动力,近年来公司持续加大研发投入,2022年研发费用达39.87亿元,同比增长16.1%,约占成药业务收入16.3%。在高强度的研发投入下,石药集团打造了丰富的产品管线,目前在研创新药项目110余个,其中大分子约40个、小分子约40个、新型制剂约30个。
今年以来,石药集团新药研发进展不断:1类新药巴托利单抗注射液(HBM9161注射液)、普卢格列汀片、恩朗苏拜单抗注射液以及3.3类新药奥马珠单抗生物类似药申报上市;国内首款抗GFRAL单抗JMT203、ATM抑制剂SYH2051、PRMT5抑制剂SYH2045等首次获批临床。
此外,石药集团在创新药出海方面也迎来重大进展。6月12日,石药集团宣布,公司开发的同类首创ADC药物CPO301获得FDA授予快速通道资格,该产品于今年4月在美国获批临床;2月13日,集团附属公司石药巨石生物的SYS6002(Nectin-4 ADC)授权给美国Corbus,最高金额达6.925亿美元。
含合作引进的产品在内,目前石药集团有58款1类新药(不含已上市新药及新增适应症)在国内处于申请临床及以上阶段,集中在抗肿瘤药领域,消化系统、心脑血管系统、呼吸系统、神经系统等也有所涉及。从作用机制看,化学药以多靶点抑制剂为主,生物药涵盖单抗、双抗、ADC药物等。
石药集团国内在研1类新药
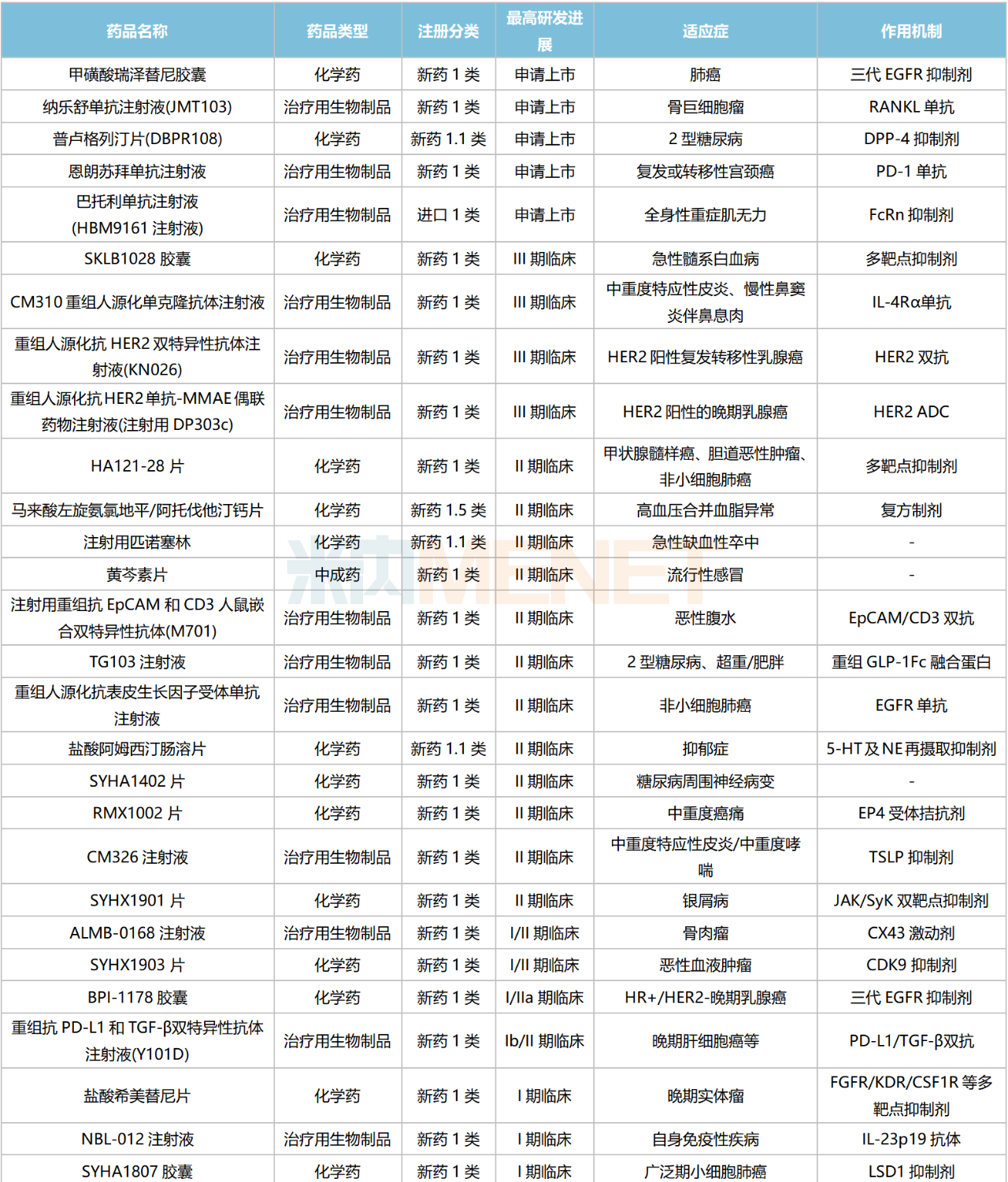
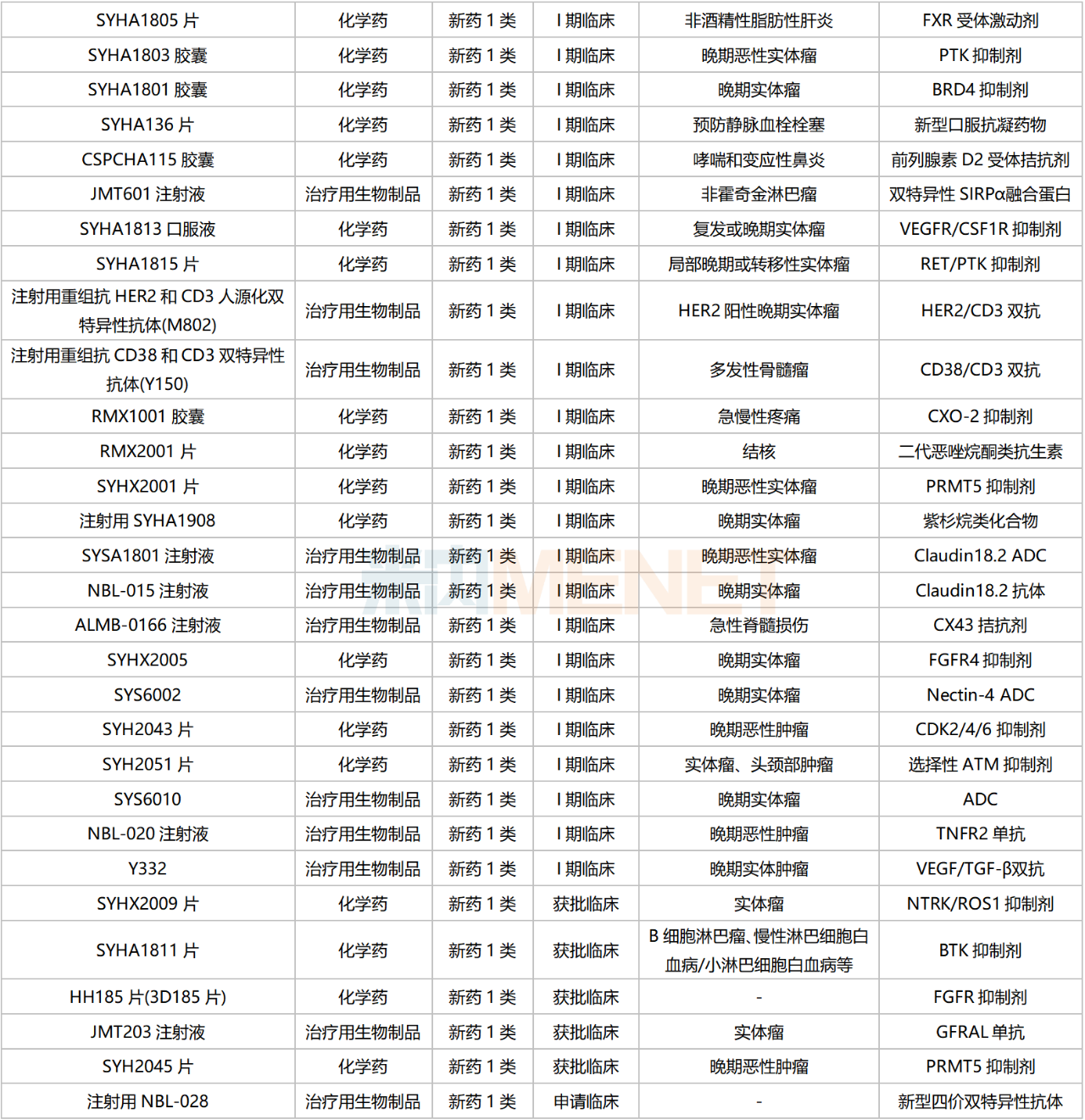
来源:米内网综合数据库
5款1类新药已申报上市。其中,纳乐舒单抗(JMT103)是首款报产的国产RANKL抗体新药,国内已获批上市的同靶点药物为安进的地舒单抗,该产品2022全球销售额超过50亿美元;巴托利单抗(HBM9161)属于FcRn抑制剂,国内同靶点获批药物为安进/再鼎的艾加莫德α,该产品于今年6月获批进口。
4款1类新药已步入III期临床。其中,CM310重组人源化单克隆抗体属于IL-4R单抗,国内已获批的同靶点药物为赛诺菲的度普利尤单抗(2020年6月),该产品2022年在中国三大终端六大市场的销售额接近13亿元,同比增长166%;KN026为HER2双抗,目前石药集团有7款双抗药物处于申请临床及以上阶段,涉及EpCAM、CD3、PD-L1、TGF-β、HER2、CD38等靶点;DP303c为HER2 ADC,目前公司有4款ADC药物步入临床试验阶段,涉及HER2、Claudin18.2、Nectin-4等靶点。
18个新品冲刺上市,9大品种抢首仿
除了1类新药,石药集团还有10余个改良新药/生物类似药处于申请临床及以上阶段。
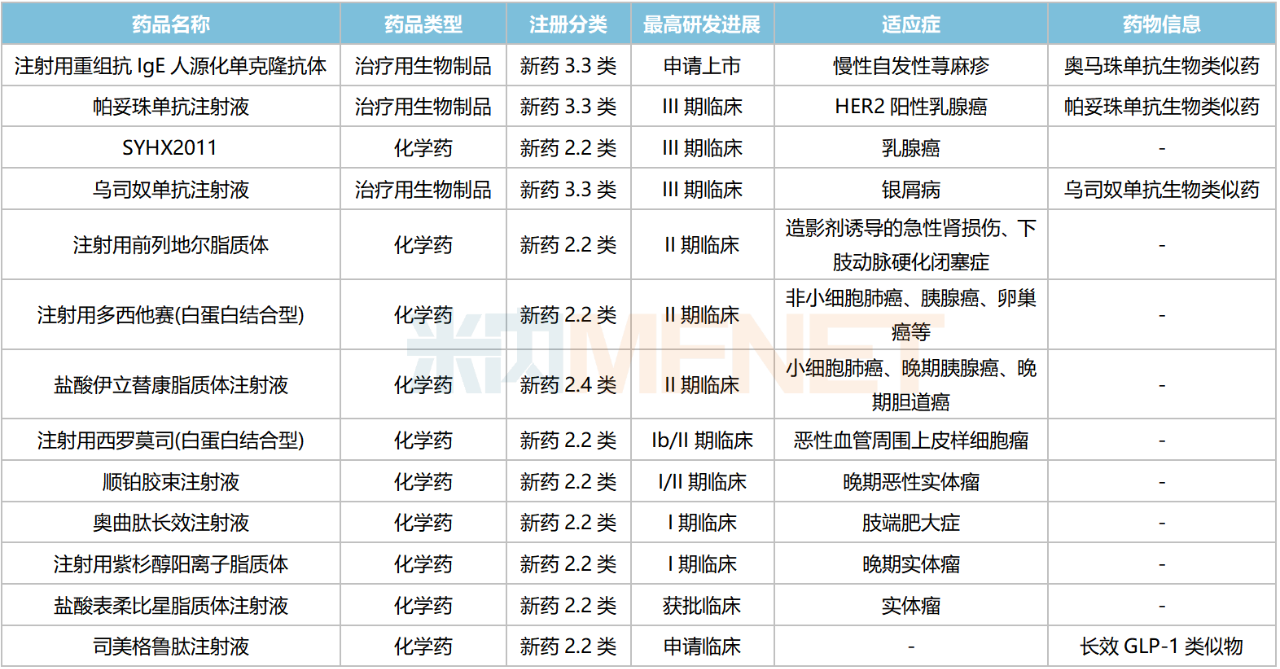
石药集团部分在研的改良新药及生物类似药
来源:米内网综合数据库
奥马珠单抗已申报上市,原研产品2022年全球销售额超过35亿美元;帕妥珠单抗处于III期临床,该产品在国内暂无生物类似药获批,原研产品2022年在中国三大终端六大市场的销售额超过35亿元,同比增长14.3%。
注射用前列地尔脂质体、注射用多西他赛(白蛋白结合型)、盐酸伊立替康脂质体注射液正在开展II期临床。米内网数据显示,前列地尔、多西他赛在中国公立医疗机构终端的销售峰值分别超过70亿元、40亿元。
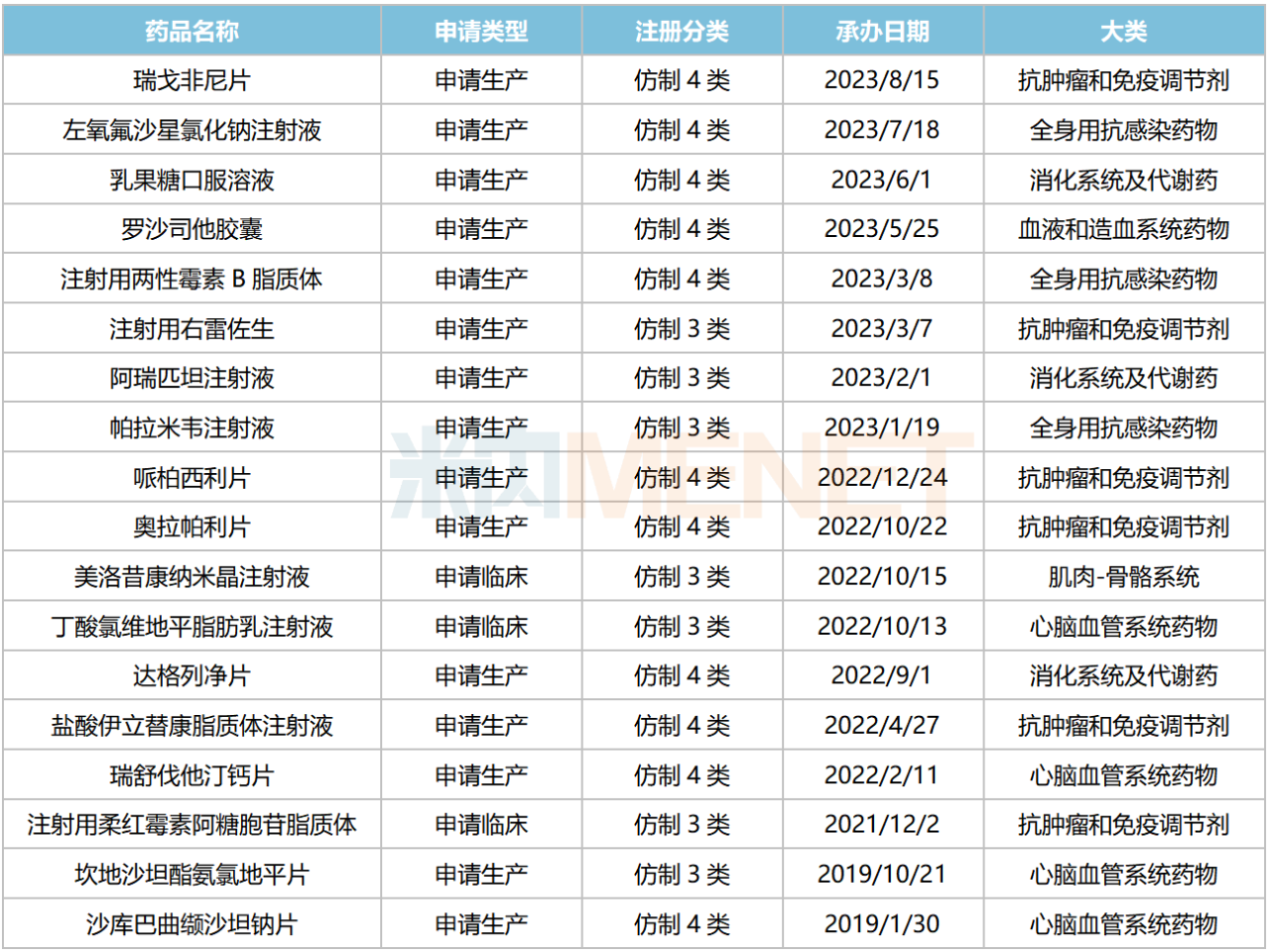
在仿制药方面,今年以来,石药集团有8个品种以新注册分类报产。截至目前,公司有18个新分类申报的品种在审,其中有8个暂无首仿(含剂型首仿)获批上市,包括罗沙司他胶囊、哌柏西利片、美洛昔康纳米晶注射液、丁酸氯维地平脂肪乳注射液、盐酸伊立替康脂质体注射液、注射用柔红霉素阿糖胞苷脂质体、坎地沙坦酯氨氯地平片、沙库巴曲缬沙坦钠片等。
石药集团新分类申报且在审的品种
来源:米内网中国申报进度(MED)数据库
3个品种由石药集团独家以新注册分类申报。其中,注射用柔红霉素阿糖胞苷脂质体、坎地沙坦酯氨氯地平片等品种在国内市场空白。
资料来源:米内网数据库、公司公告等
注:米内网《中国三大终端六大市场药品竞争格局》,统计范围是:城市公立医院和县级公立医院、城市社区中心和乡镇卫生院、城市实体药店和网上药店,不含民营医院、私人诊所、村卫生室,不含县乡村药店;上述销售额以产品在终端的平均零售价计算。数据统计截至8月16日,如有疏漏,欢迎指正!
医药网新闻
- 相关报道
-
- 我国中药饮片标注保质期自8月1日起实施 (2025-07-31)
- 河北对于进一步欠缺公立医疗机构特需医疗服务治理的关照 (2025-07-30)
- 江苏对于脑机接口相关医疗服务价钱名目的公示 (2025-07-30)
- 两部分结合部署增强养老服务举措措施规划布局体例任务 (2025-07-29)
- 三部分宣布药用类麻醉 药品和精力药品目次的布告 (2025-07-29)
- 2025年1 (2025-07-28)
- 四年多来全国跨省异地就医间接结算惠及5.6亿人次 (2025-07-25)
- 国新办宣布汇聚焦我国“十四五”时期医保改造 (2025-07-25)
- 中国残联:今朝全国已完工残疾人服务举措措施4614个 (2025-07-23)
- 全国持社保卡人数达13.9亿人 笼罩98.9%生齿 (2025-07-23)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















