浙江大学研究者们揭示了来源于M2样巨噬细胞的细胞外囊泡以miR |
 |
来源:100医药网 2024-05-11 17:01
该研究表明,m2φ - ev在ALI/ARDS的发病机制中发挥保护作用,部分由miR-709介导,为评估疾病严重程度和治疗ALI/ARDS提供了一种潜在的策略。急性肺损伤/综合征(ALI/ARDS)是一种由脓毒症、肺炎、、误吸、急性等多种病因引起的临床综合征,以肺部炎症恶化、微通透性增高为特征。尽管肺保护性通气大大降低了死亡率,但目前还没有有效的药物治疗方法。因此,制定新的ALI/ARDS治疗策略至关重要。
ALI/ARDS的主要致病机制涉及过度炎症反应引发的炎症级联反应。特别是,炎症小体起着至关重要的作用,核苷酸结合低聚结构域,如受体蛋白3 (NLRP3)炎症小体是最重要的。NLRP3炎症小体包含NLRP3、凋亡相关斑点样蛋白(ASC)和前caspase-1,其激活导致caspase-1依赖性成熟和释放几种促炎细胞因子,包括IL-1 和IL-18。大量研究发现NLRP3炎性小体过度激活与多种急慢性肺部疾病密切相关,包括、慢性阻塞性肺疾病、以及ALI/ARDS。因此,靶向NLRP3炎性体可能有效缓解ALI/ARDS。
巨噬细胞作为一种重要的先天细胞,参与宿主防御病原体和组织稳态。尽管肺中存在几种类型的巨噬细胞,但肺泡巨噬细胞尤其丰富,在免疫反应中起着至关重要的作用。一般来说,巨噬细胞是异质免疫细胞,大致可分为m1样巨噬细胞(M1 )和m2样巨噬细胞(M2 )。
M1 主要参与促炎过程,是许多细胞因子的主要来源,包括IL-6、TNF- 和IL-1 ,这些细胞因子有助于感染后的组织损伤。相反,M2 在急性肝功能衰竭、急性肾损伤、结肠炎和ALI小鼠模型中具有抗炎和组织修复作用,部分通过抑制NLRP3炎性体激活。然而,巨噬细胞定向细胞治疗在体内的实际应用面临一些限制。例如,巨噬细胞固有的高免疫原性限制了其来源的可用性,巨噬细胞分化的倾向阻碍了它们进入体内后维持稳定表型的能力。因此,需要更稳定、更方便、更安全的替代品。

图片来源:
近日,来自浙江大学医学院第二附属医院重症医学科的研究者们在J Extracell Vesicles杂志上发表了题为 Extracellular vesicles derived from M2-like macrophages alleviate acute lung injury in a miR-709-mediated manner 的文章,该研究表明,m2 - ev在ALI/ARDS的发病机制中发挥保护作用,部分由miR-709介导,为评估疾病严重程度和治疗ALI/ARDS提供了一种潜在的策略。
急性肺损伤/急性呼吸窘迫综合征的特点是炎症反应不受控制,目前的治疗策略疗效有限。虽然m2样巨噬细胞(M2 )及其细胞外囊泡(EVs)的保护作用在其他炎症性疾病中已被充分证明,但M2 衍生的EVs (M2 -EVs)在ALI/ARDS发病机制中的作用仍知之甚少。
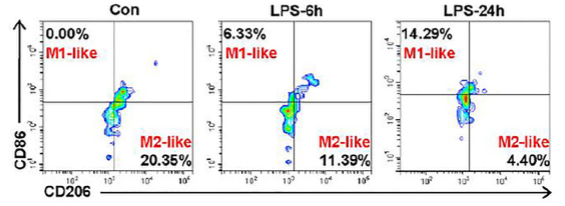
lps诱导ALI小鼠模型中M2/ m1样肺泡巨噬细胞及其衍生ev的动态变化
图片来源:
本研究利用脂多糖诱导的ALI小鼠模型首次证明内源性m2样肺泡巨噬细胞来源的ev减少。然后,气管内灌注来自小鼠肺泡巨噬细胞系(MH-S)的外源性m2 - ev,主要引起肺泡巨噬细胞的摄取,从而减轻肺部炎症和损伤。机制上,M2 -EVs在体内外均能有效抑制肺泡巨噬细胞的焦亡,抑制过量细胞因子IL-6、TNF- 、IL-1 的释放,这与抑制NF- B/NLRP3信号通路密切相关。
值得注意的是,miR-709在一定程度上介导了m2 - - ev的保护作用,miR-709在m2 - ev中的表达抑制减轻了其对小鼠脂多糖诱导的ALI的保护作用。此外,研究者发现来自支气管肺泡灌洗液的ev中miR-709的表达与ARDS患者疾病严重程度呈负相关,表明其可能作为ARDS严重程度的标志物。

m2 - ev在ALI/ARDS中的潜在作用示意图
图片来源:
综上所述,本研究数据表明,内源性m2样am - ev在lps诱导的ALI中下降,外源性m2 - ev主要通过miR-709的转移抑制NF- B/NLRP3炎症小体轴来缓解ALI的发展,miR-709显示出作为评估ALI/ARDS严重程度的合适生物标志物的潜力。这些结果为通过靶向m2 - ev来评估和治疗ALI/ARDS提供了有希望的策略。 ( 100yiyao.com)
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature:DNA甲基化“随机时钟”——EVOFLUX破译肿瘤演化史,重塑临床预后新维度 (2025-09-13)
- GLP-1新战场:礼来、信达、恒瑞再交锋 (2025-09-13)
- Nature Methods:解锁细胞宇宙的“星图”——scvi-hub如何将海量单细胞数据“浓缩”到你的笔记本电脑里? (2025-09-13)
- 为什么精子会“跑不动”?大阪大学揪出两大关键蛋白:CFAP91搭起“运动支架”,EFCAB5调控“冲刺力”,男性生育有了新靶点 (2025-09-12)
- 突破!肺癌细胞转移大脑后竟会与神经元“串通”!Nature 新研究揭致命机制,抗癫痫药或成新希望 (2025-09-12)
- J Neurochem:肠道与大脑的“对话”——科学家揭秘机体慢性疼痛的神经通路 (2025-09-11)
- 母亲高血糖,影响后代生育能力,黄荷凤院士团队等揭示背后的表观遗传机制 (2025-09-11)
- STTT:韩国科学家发现减轻大脑氧化应激损伤、减少神经退行性病变的新方法! (2025-09-11)
- 《癌症研究》:橄榄油吃太多,乳腺癌易挪窝!美国科学家发现,富含橄榄油的高脂饮食,会促进三阴性乳腺癌肺转移 (2025-09-11)
- 减重竟还能减痛?!EJN:饮食质量提升 22%,慢性疼痛率直降一半,体脂变化竟不是关键 (2025-09-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















