Nature子刊:颉伟/李晶团队揭示增强子在卵子发生及早期胚胎发育中的转录调控机制 |
 |
来源:生物世界 2024-06-09 12:44
研究团队鉴定了哺乳动物卵子到早期胚胎中活跃增强子网络,揭示了其不同于成体细胞的重要特征。清华大学生命学院颉伟研究组与南京医科大学李晶研究组合作在Nature Cell Biology期刊发表了题为:Mapping putative enhancers in mouse oocytes and early embryos reveals TCF3/12 as key folliculogenesis regulators的研究论文。
该研究揭示了活跃增强子在哺乳动物卵子发生和早期胚胎发育过程中参与转录调控的机制。该研究验证了小鼠卵子中活跃增强子的存在,揭示了卵子和早期胚胎发育过程中增强子不同于成体细胞和组织的独特属性,并鉴定了参与调控卵子发生过程中增强子的关键转录因子 TCF3和TCF12。

之前的研究认为,小鼠成熟卵母细胞和受精后合子中缺乏增强子活性。然而,卵子和早期胚胎的多项表观基因组研究(如开放染色质等)提示在该阶段可能存在大量活跃的调控元件。基因表达在卵子向胚胎的转换过程中,经历了从全基因组沉默到合子基因组激活的巨大变化。研究人员通过STAR ChIP-seq技术鉴定了活跃增强子的标志 组蛋白修饰H3K27ac,检测了从小鼠初级卵泡卵母细胞直到胚胎内细胞团(ICM)阶段的全基因组分布,并结合颉伟课题组前期发表的着床后胚胎的H3K27ac数据,绘制了涵盖小鼠配子及着床前后胚胎16个阶段的H3K27ac标记的潜在活跃增强子分布动态图谱。在受精前后和着床前后,增强子网络经历了两次剧烈的重编程过程。
与成体细胞组织中的增强子分布数据相比,该研究发现卵子和着床前胚胎中的活跃增强子与成体细胞组织中有显著差异。尤其在成熟卵母细胞中,约50%的活跃增强子是卵子特异的,且这些特异增强子大量分布在基因密度较低的基因荒漠区域。在卵子和着床前胚胎中,大量活跃增强子也被组蛋白修饰H3K4me3标记,这与卵子和早期胚胎中低DNA甲基化相关。在受精前后,组蛋白乙酰化经历了全基因组抹除和在合子基因组激活(ZGA)相关的增强子的重建。而母源继承下来的组蛋白修饰H3K27me3则会抑制部分胚胎增强子的建立,特别是H3K27me3介导的印记基因附近的增强子。
研究团队进一步通过实验验证了卵子中活跃增强子的存在。首先,他们发现卵子中的部分增强子能够双向转录。同时,通过优化了增强子高通量检测方法STARR-seq使其能够应用于微量细胞,研究人员验证了具有H3K27ac双向转录标记的70个潜在增强子,其中64%为阳性。随后,他们采用增强子报告基因方法在卵子中进一步验证了这70个增强子中的7个,结果所有这些增强子均为阳性。全基因组分析显示,这些阳性增强子通常由H3K4me3和Pol II标记,并显著富集卵子关键转录因子的结合基序。增强子的另外一个特征是富含转录因子的结合序列。研究人员进一步研究了不同阶段增强子上相关转录因子结合序列,发现卵子和着床前后胚胎中的活跃增强子中转录因子序列发生了显著变化。研究人员在卵子中鉴定了两个在增强子上最为富集的关键转录因子TCF3和TCF12。敲除TCF3和TCF12会导致卵泡发育和卵子发育的严重缺陷,并使卵子转录组停滞在原始卵泡阶段,无法激活如Zp1/2/3等卵子发育关键基因。上述结果表明,卵子中存在活跃的增强子,这些增强子帮助鉴定出调控卵泡发生和卵子发育的关键转录因子TCF3和TCF12。
综上所述,研究团队鉴定了哺乳动物卵子到早期胚胎中活跃增强子网络,揭示了其不同于成体细胞的重要特征。他们通过实验验证了卵子中活跃增强子的存在,并以此鉴定了卵子中的关键转录因子TCF3和TCF12。这项研究不仅揭示了卵子发生和早期胚胎中独特的增强子及相关转录因子调控网络,还为理解卵子发生及卵子胚胎转换过程中的转录调控提供了新的视角。
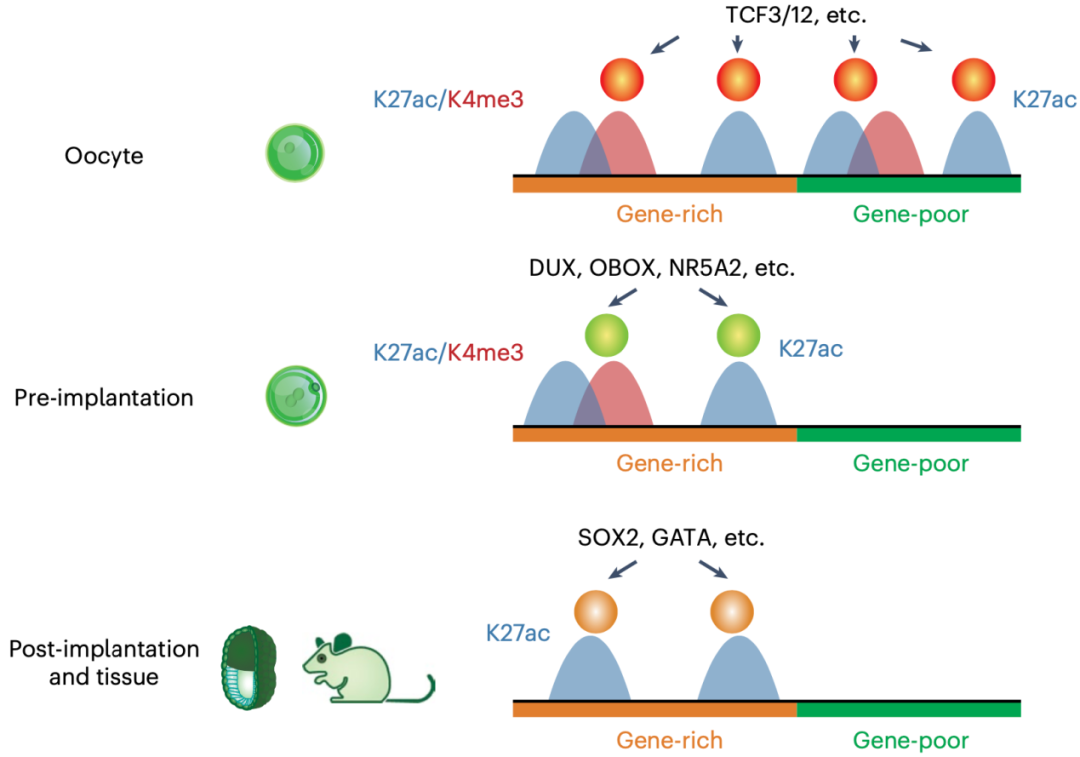
活跃增强子在卵子和早期胚胎中的分布示意图
清华大学颉伟教授和南京医科大学李晶教授为论文共同通讯作者,清华大学生命学院博士后刘伯峰,南京医科大学副教授何元林,清华大学生命学院助理研究员吴小童,北京农学院副教授林自力,清华大学生命学院博士生马婧为论文共同第一作者。合作实验室包括清华大学医学院那洁教授课题组和德国慕尼黑亥姆霍兹研究中心Maria Elena Torres-Padilla教授课题组。南京医科大学李晶教授课题组博士生邱玥鑫,重庆医科大学教授向云龙,清华大学生命学院颉伟课题组博士生孔凤也在该课题中做出重要贡献。 版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- GLP-1新战场:礼来、信达、恒瑞再交锋 (2025-09-13)
- Nature Methods:解锁细胞宇宙的“星图”——scvi-hub如何将海量单细胞数据“浓缩”到你的笔记本电脑里? (2025-09-13)
- 为什么精子会“跑不动”?大阪大学揪出两大关键蛋白:CFAP91搭起“运动支架”,EFCAB5调控“冲刺力”,男性生育有了新靶点 (2025-09-12)
- 突破!肺癌细胞转移大脑后竟会与神经元“串通”!Nature 新研究揭致命机制,抗癫痫药或成新希望 (2025-09-12)
- J Neurochem:肠道与大脑的“对话”——科学家揭秘机体慢性疼痛的神经通路 (2025-09-11)
- 母亲高血糖,影响后代生育能力,黄荷凤院士团队等揭示背后的表观遗传机制 (2025-09-11)
- STTT:韩国科学家发现减轻大脑氧化应激损伤、减少神经退行性病变的新方法! (2025-09-11)
- 《癌症研究》:橄榄油吃太多,乳腺癌易挪窝!美国科学家发现,富含橄榄油的高脂饮食,会促进三阴性乳腺癌肺转移 (2025-09-11)
- 减重竟还能减痛?!EJN:饮食质量提升 22%,慢性疼痛率直降一半,体脂变化竟不是关键 (2025-09-11)
- 肠道菌群还能操控皮肤炎症?清华大学最新Immunity论文,揭示肠道菌群代谢物驱动银屑病炎症的机制 (2025-09-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















