为什么睡得好,记忆力就好?两篇Nature:揭示睡眠在大脑记忆形成过程中扮演的关键角色 |
 |
来源:100医药网 2024-06-18 11:02
发表在Nature杂志的两篇研究报告中,来自密歇根大学等机构的科学家们就揭示了其中的原因,以及睡眠和睡眠剥夺期间大脑到底发生了什么。试想一下,你是一名学生,现在是期末考试周,你正在准备一场大考,那么你会选择熬夜复习还是休息一下呢?很多经历过熬夜抱佛脚的人都知道,睡眠不足会人 变蠢 很难记住东西。
近日,发表在Nature杂志的两篇研究报告中,来自密歇根大学等机构的科学家们就揭示了其中的原因,以及睡眠和睡眠剥夺期间大脑到底发生了什么。
特定的神经元能适应特定的刺激,比如,迷宫中的大鼠一旦到达迷宫中的特定地点,其大脑中的神经元就会被激活,这些被称之为 位置神经元 (place neurons)的特殊神经元在人体内也非常活跃,且能帮助人们在环境中进行定位。那么在睡眠过程中到底会发生什么呢?
这项研究中,研究人员观察了海马体中的神经元,海马体是大脑深处参与记忆形成的海马形状特殊结构。他们发现,一种能在动物睡眠时可视化调节与位置相关的新神经元模式 在休息状态和睡眠状态下,每隔几秒就会有一种称之为尖波涟漪的电活性从海马体中释放出来,并持续数小时。
研究人员对这些波纹的同步程度以及传播距离非常感兴趣,它们似乎能将信息从大脑的一个部分扩散到了另一个部分,这些放电被认为能促进神经元形成并更新包括地点的记忆等。在实验中,科研人员记录了大鼠完成新迷宫探索后睡眠状态下的脑部活动,运用了一种称为贝叶斯学习的高级统计分析手段。这一策略使他们首次精准识别出哪些神经元与迷宫内的特定位置相对应并作出响应。
Diba研究员举例说明,若某神经元对迷宫某角落显示出偏好激活,研究中观察到,在睡眠阶段,该神经元不仅与共享相似偏好的神经元同步激活,还会意外地与代表其他区域的神经元协同工作。有趣的是,当大鼠再次进入迷宫时,其大脑神经元的空间敏感性出现了调整,这种变化直接关联到睡眠期间哪些神经元群被激活的模式。此发现不仅展现了睡眠中神经可塑性的实时可视化,也进一步支持了睡眠期间的神经元重激活对于记忆巩固的重要作用理论。
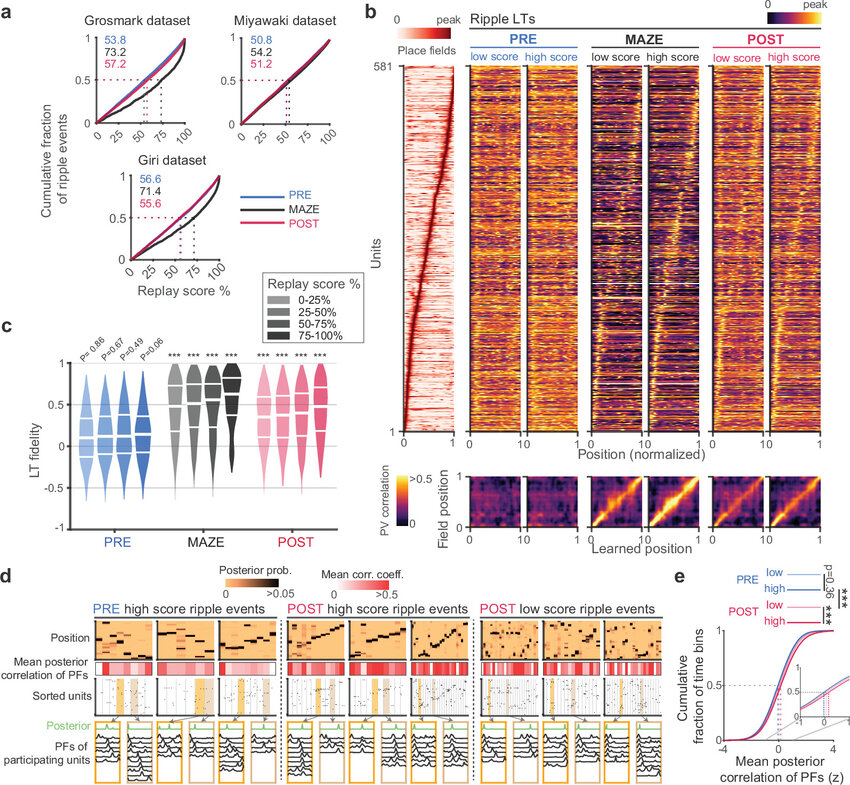
揭示睡眠在大脑记忆形成过程中扮演的关键角色
图片来源:Nature (2024). DOI:10.1038/s41586-024-07397-x
这种方法使研究人员能实时可视化神经元的可塑性或表征漂移,为长期以来的认识 即睡眠期间神经元的再次激活是睡眠对记忆至关重要的机制之一 提供了实证支持。鉴于睡眠的关键作用,研究者进一步探求了解在经历睡眠剥夺时,大脑内部究竟遭遇了怎样的变化。
在接下来的第二部分研究中,团队对比分析了睡眠与缺乏睡眠状态下,位置神经元再次激活的频次(迷宫探索中活跃的神经元在休息时的自发唤醒)及其激活序列(通过 重放 现象衡量)。研究揭示,与睡眠剥夺相比,正常睡眠状态下的神经元在重激活和迷宫体验 重放 过程中的放电模式更为强烈,尽管睡眠剥夺状态下尖波涟漪的频率相近,但其幅度和能量较小。Diba研究员指出,不幸的是,在大约一半的案例中,睡眠剥夺彻底阻断了尖波涟漪期间对迷宫经验的重激活。即便剥夺睡眠的大鼠后来有机会补眠,重激活和 重放 过程虽略有回升,却远不能达到未经剥夺睡眠的大鼠水平,表明这部分记忆功能的损伤可能是不可逆的。
最后研究者表示,尽管再激活(reactivation)和重放(replay)对于记忆非常重要,但本文研究结果证明了睡眠剥夺对机体记忆的有害影响,研究人员希望后期能继续深入研究观察睡眠期间大脑记忆处理的本质,并解释为何这些记忆需要被重新激活,同时深入剖析睡眠缺失如何干扰这一精密的记忆维护系统。(100yiyao.com)
参考文献:
Maboudi, K., Giri, B., Miyawaki, H. et al. . Nature 629, 630 638 (2024). doi:10.1038/s41586-024-07397-x
Giri, B., Kinsky, N., Kaya, U. et al. . Nature (2024). doi:10.1038/s41586-024-07538-2
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- GLP-1新战场:礼来、信达、恒瑞再交锋 (2025-09-13)
- Nature Methods:解锁细胞宇宙的“星图”——scvi-hub如何将海量单细胞数据“浓缩”到你的笔记本电脑里? (2025-09-13)
- 为什么精子会“跑不动”?大阪大学揪出两大关键蛋白:CFAP91搭起“运动支架”,EFCAB5调控“冲刺力”,男性生育有了新靶点 (2025-09-12)
- 突破!肺癌细胞转移大脑后竟会与神经元“串通”!Nature 新研究揭致命机制,抗癫痫药或成新希望 (2025-09-12)
- J Neurochem:肠道与大脑的“对话”——科学家揭秘机体慢性疼痛的神经通路 (2025-09-11)
- 母亲高血糖,影响后代生育能力,黄荷凤院士团队等揭示背后的表观遗传机制 (2025-09-11)
- STTT:韩国科学家发现减轻大脑氧化应激损伤、减少神经退行性病变的新方法! (2025-09-11)
- 《癌症研究》:橄榄油吃太多,乳腺癌易挪窝!美国科学家发现,富含橄榄油的高脂饮食,会促进三阴性乳腺癌肺转移 (2025-09-11)
- 减重竟还能减痛?!EJN:饮食质量提升 22%,慢性疼痛率直降一半,体脂变化竟不是关键 (2025-09-11)
- 肠道菌群还能操控皮肤炎症?清华大学最新Immunity论文,揭示肠道菌群代谢物驱动银屑病炎症的机制 (2025-09-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















