Cell Res:蓝斐/蔡加彬团队揭示SMYD5作为核糖体甲基转移酶促进肝细胞癌 |
 |
来源:生物世界 2024-08-10 11:46
在这项最新研究中,研究团队确定了SMYD5作为一种核糖体赖氨酸甲基转移酶,其主要催化RPL40 K22me3。SMYD5-RPL40 K22me3信号轴对于有效的翻译延伸和整体蛋白质合成至关重要。复旦大学附属中山医院蓝斐、蔡加彬团队联合德克萨斯大学MD安德森癌症中心及诺华(中国)生物医学研究中心,在CellResearch期刊发表了题为:SMYD5 is a ribosomal methyltransferase that catalyzes RPL40 lysine methylation to enhance translation output and promote hepatocellular carcinoma的研究论文。
该研究表明,SMYD5是一种核糖体甲基转移酶,它能过催化RPL40的赖氨酸甲基化(RPL40 K22me3),以增强蛋白质翻译输出并促进肝(HCC)。这些研究结果揭示了SMYD5-RPL40 K22me3信号轴在翻译延伸中的新作用,并强调了在肝细胞癌中靶向SMYD5的治疗潜力,特别是同时抑制mTOR。这项工作还在概念上拓宽了对赖氨酸甲基化的理解,将其意义从转录调控扩展到了翻译控制。

蛋白质赖氨酸Nε-甲基化在各种生物过程中发挥着至关重要的作用。在过去约二十年中,虽然其通过组蛋白对转录调控的影响已得到广泛研究,但其在翻译中的作用在很大程度上仍未被探索。
据报道,几种哺乳动物核糖体蛋白(例如RPL4、RPL29、RPL40和RPL36A)均含有赖氨酸甲基化。其中,RPL40是由UBA52基因编码的一种特殊核糖体蛋白。
前体UBA52蛋白是一种128个氨基酸组成的融合蛋白,包括一个N端的泛素模块(76个 氨基酸)融合。去除泛素后,成熟形式的RPL40长度为52个氨基酸,是在细胞质中组装到60S核糖体亚基的最后成分之一,其在蛋白质合成中具有重要功能。早在27年前,通过大鼠肝脏的质谱分析鉴定出了RPL40上K22的三甲基化(RPL40 K22me3,相当于 UBA52 K98me3),并在在近的高分辨率核糖体结构研究中得到了可视化。然而,这种修饰在翻译和核糖体功能中的作用仍不清楚。
SMYD蛋白质构成了一个进化上保守的赖氨酸甲基转移酶亚家族,其特征是一个被MYND结构域分割的催化SET结构域。最近有报道称SMYD5能催化病毒Tat蛋白的甲基化并参与HIV感染,还能在启动子处催化组蛋白H3K36me3并驱动肝细胞癌(HCC)的肿瘤发生,不过下游机制尚不清楚。
事实上,来自TCGA数据库的数据表明,在大多数癌症类型中,SMYD5的mRNA水平升高,其中肝细胞癌(HCC)是最显著的类型之一。与此一致的是,最近的两项多组学研究发现,肝细胞癌样本中SMYD5的mRNA和蛋白质水平均显著升高,且与不良临床结果相关。
在这项最新研究中,研究团队确定了SMYD5作为一种核糖体赖氨酸甲基转移酶,其主要催化RPL40 K22me3。SMYD5-RPL40 K22me3信号轴对于有效的翻译延伸和整体蛋白质合成至关重要。
在肝细胞癌(HCC) SMYD5的缺失会导致对mTOR抑制剂的超敏反应,这可能是由于对蛋白质合成的复合抑制作用。通过体外和体内肝细胞癌(HCC)模型,研究团队进一步阐明了SMYD5介导的RPL40 K22me3在维持癌症生长中的关键作用,特别是在mTOR信号受到抑制的情况下。
具体来说,该研究显示,SMYD5对RPL40 K22具有强大的体外活性,并且在细胞中主要催化 RPL40 K22me3。SMYD5和RPL40K22me3的缺失导致翻译输出减少和延伸受扰,SMYD5和RPL40 K22me3在肝细胞癌(HCC)中上调,并且与患者预后呈负相关。在2D和3D培养中,敲除SMYD5使肝细胞癌细胞对mTOR抑制高度敏感。此外,在基因工程小鼠和患者来源的异种移植(PDX)模型中,SMYD5的缺失显著抑制肝细胞癌的发展和生长,在PDX模型中,同时抑制mTOR进一步增强了抑制效果。
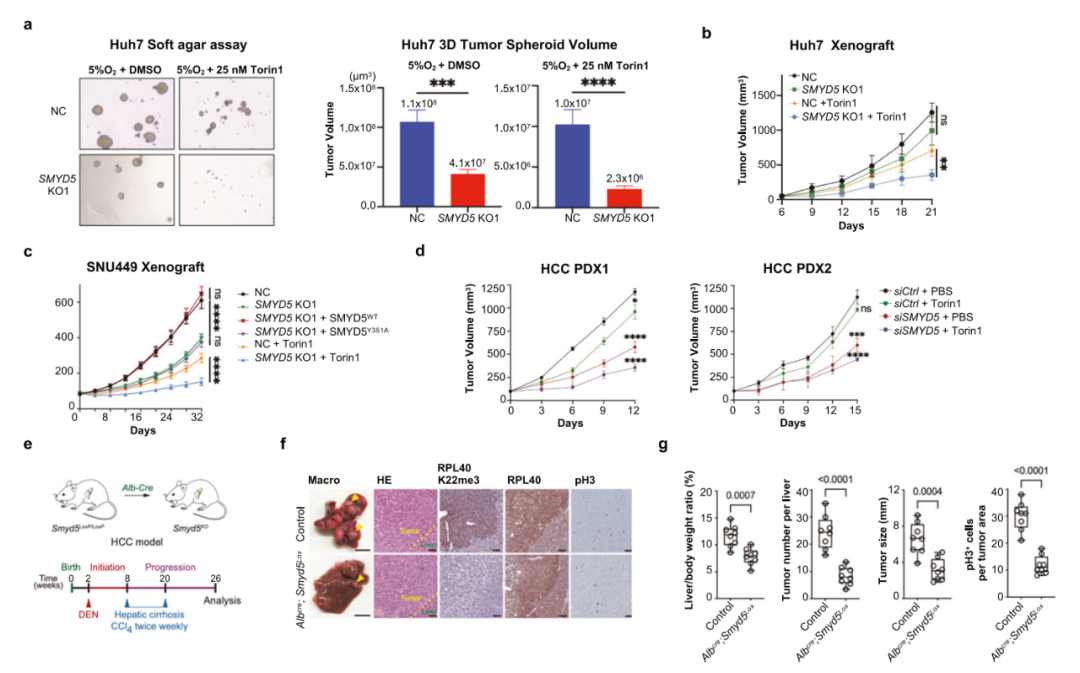
总的来说,这些发现强调了将SMYD5-RPL40 K22me3信号轴作为肝细胞癌患者的治疗靶点的潜力。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature:癌症研究新突破!科学家揭秘小细胞肺癌的起源与演变 (2025-09-19)
- Nature Methods:蛋白质工程新范式!当AI开始“补习”第一性原理,METL框架从“知其然”到“知其所以然” (2025-09-19)
- Bio-Protocol:北京妇产医院刘朝晖团队成功构建“内膜外翻”的人子宫内膜类器官(含详细操作步骤) (2025-09-18)
- 18款1类新药首次在中国获批临床! (2025-09-18)
- Cell:mRNA疫苗,进军肺结核领域,增加并超越卡介苗保护效果 (2025-09-18)
- Nature子刊:AI从头设计多肽,精准抑制细胞焦亡,开辟炎症疾病治疗新途径 (2025-09-18)
- Nature:胃的“南北战争”!神经组织竟是调控胃功能分区的幕后指挥官 (2025-09-18)
- Nature Medicine:胖,但健康!遗传学如何“解绑”肥胖与心脏病的宿命关联? (2025-09-17)
- 国内唯一获批干细胞药物首位患者出院,国产干细胞药品取得临床应用突破 (2025-09-16)
- 《自然》:慢性压力毁血糖!科学家发现全新调控血糖神经通路,可快速调节肝脏糖生成,反复压力会钝化此通路,导致糖代谢受损 (2025-09-16)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















