三篇Cell:科学家揭示免疫疗法协同作用促进黑色素瘤患者机体中T细胞反应背后的分子机制 |
 |
来源:100医药网 2024-08-17 13:01
这三篇研究报告提供了LAG3和PD1如何单独发挥功能以及联合作用背后的分子机制,并强调了利用其进一步进行临床研发的新机会。近日,发表在国际杂志Cell上的研究报告中,来自匹兹堡大学等机构的科学家们通过研究揭示了靶向作用检查点PD1和LAG3的免疫疗法如何共同发挥作用来激活宿主机体的免疫反应,相关研究结果揭示了为何靶向作用两种检查点的组合性疗法相比仅作用PD1的单一疗法能改善瘤患者的治疗结局。
利用来自人类临床试验和动物模型的数据,研究人员调查了肿瘤杀伤性CD8+ T细胞的反应,在与癌症的长期斗争中,免疫检查点能在T细胞表面积累,其就好像制动器一样能抑制T细胞的活性并驱动其发生耗竭,能帮助释放这些制动器并抵御T细胞耗竭的免疫检查点抑制剂彻底改变了人类癌症的治疗,但因为很多患者没有产生反应,因此研究人员还需要进行更多的研究来理解如何将这些药物结合起来来改善其效用。
研究者Dario A. A. Vignali博士表示,这些研究首次深入研究了免疫系统对阻断PD1和LAG3的反应,我们发现,靶向作用PD1与PD1和LAG3或许能以惊人的不同方式来调节CD8+ T细胞的功能,理解这些机制与我们如何考虑联合治疗并优化药物的最佳配对有关。早在2022年,靶向作用LAG3的药物relatlimab获得批准,与靶向作用PD-1的纳武单抗(nivolumab)结合使用来治疗患者,相比单独使用纳武单抗而言,这种组合性疗法能显著改善患者的治疗结果,然而其增强宿主机体抗力背后的分子机制,研究人员并不清楚,而最新研究或许就有助于填补这一研究空白。
在第一项研究中,研究者Vignali等人进行了一项临床试验来调查接受relatlimab、纳武单抗或两种药物的黑色素瘤患者机体的免疫反应。通过分析其血液和肿瘤样本,研究人员发现,相比只接受一种药物治疗的患者而言,接受这两种药物的患者机体中CD8+ T细胞的反应会增强,这与改善其机体癌症杀伤效能直接相关,尽管细胞保留了耗竭的特征。
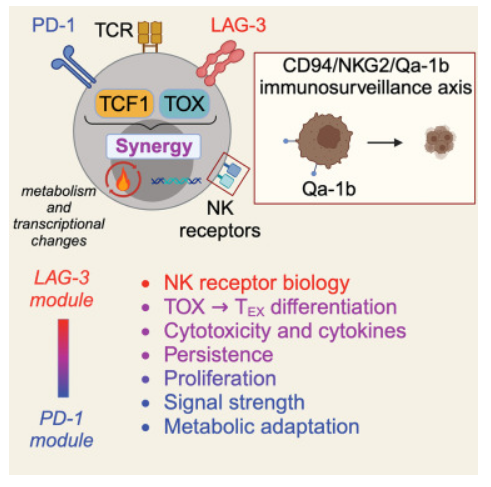
科学家揭示免疫疗法协同作用促进黑色素瘤患者机体中T细胞反应背后的分子机制
图片来源:Cell (2024). DOI:10.1016/j.cell.2024.07.018
研究人员非常惊讶地发现,同时阻断PD1和LAG3所产生的变化要比单独阻断PD1或LAG3所产生的效果要大得多,研究结果表明,这些免疫检查点能抑制CD8+ T细胞功能的不同方面,从而就使其能以一种意想不到的方式来进行协同作用。据研究者介绍,分析患者机体样本的关键之处在于relatlimab药物并不是惰性的,而这项研究的独特之处在于,患者最初接受了为其4周的relatlimab、纳武单抗以及两种药物联合治疗,这就能使其分析每一种治疗方案的效果。
此前多项研究结果表明,单独使用relatlimab并不能改善机体的抗肿瘤免疫力,但当与纳武单抗联合使用后才能有效,通过揭示relatlimab如何影响机体的T细胞反应,这项最新研究结果表明,这种疗法或能与其它改善机体免疫反应的免疫疗法结合。研究者Bruno说道,我们对这项研究感到特别兴奋,因为研究分析是在此前没有接受过免疫疗法的患者机体的样本中进行的,这就能促使我们评估LAG3和PD1单独和联合使用对患者机体肿瘤所产生的影响效应,同时也能进一步帮助理解患者所接受的智能免疫疗法组合,只在改善治疗疗效。
在第二项研究中,研究人员利用经过遗传工程化改造的小鼠进行研究,以便其机体中CD8+ T细胞并不会产生PD1、LAG3或两者兼有。在黑色素小鼠模型中,相比缺乏PD1或LAG3的T细胞相比,缺乏两种免疫检查点的T细胞会增强对肿瘤的清除并改善小鼠的生存率,这就增强了临床试验的结果,此外,研究人员还揭示了PD1和LAG3如何协同作用从而阻碍机体抗肿瘤免疫力背后的分子机制。
发表在Cell杂志上的另一项研究中,研究者Vignali作为其中的合作者,他们所得到的研究结果与上述研究结果一致,同时还提供了关于LAG3和PA1如何以不同的方式促进T细胞耗竭的新见解。综上,这三篇研究报告提供了LAG3和PD1如何单独发挥功能以及联合作用背后的分子机制,并强调了利用其进一步进行临床研发的新机会。(100yiyao.com)
参考文献:
Shin Foong Ngiow,Sasikanth Manne,Yinghui Jane Huang, et al. , Cell (2024). DOI:10.1016/j.cell.2024.07.018
Lawrence P Andrews,Samuel C Butler, Jian Cui, et al. , Cell (2024). DOI: 10.1016/j.cell.2024.07.016
Anthony R. Cillo,Carly Cardello,Feng Shan, et al. , Cell (2024). DOI: 10.1016/j.cell.2024.06.036
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature Medicine:胖,但健康!遗传学如何“解绑”肥胖与心脏病的宿命关联? (2025-09-17)
- 国内唯一获批干细胞药物首位患者出院,国产干细胞药品取得临床应用突破 (2025-09-16)
- 《自然》:慢性压力毁血糖!科学家发现全新调控血糖神经通路,可快速调节肝脏糖生成,反复压力会钝化此通路,导致糖代谢受损 (2025-09-16)
- FDA监管趋严,如何影响中国创新药出海? (2025-09-16)
- JAMA子刊:重大突破!北京安定医院团队首次证实,ANK3可以预测liafensine治疗难治性抑郁症的疗效 (2025-09-16)
- 百奥赛图宣布Tubulis签署抗体许可协议以推进ADC疗法开发 (2025-09-16)
- Science:演化“剧本”的反转!植物,被低估的物种形成“效率大师” (2025-09-16)
- Nature Biotechnology:为“生物导弹”扩容——抗体-瓶刷偶联物(ABC)技术重新定义抗体偶联药物的设计边界 (2025-09-16)
- 【9月18日直播预告】揭秘 “微型器官” 诞生:IPSC 诱导类器官全流程技术细节+常见问题答疑 (2025-09-16)
- Gut:低乙肝表面抗原水平提示肝癌风险极低,有望重新定义“部分治愈”概念 (2025-09-16)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















