《癌症通讯》:又现一员促癌大将!复旦中山医院团队揭示调控乳酸代谢,帮癌细胞教唆巨噬细胞促癌的重要靶点 |
 |
来源:奇点糕 2024-09-19 14:02
对巨噬细胞组分的分析显示,敲除或沉默Srsf10显著减少了促癌的M2-TAMs占比,使有利抗癌的M1型TAMs占比上升,且SRSF10表达水平与M2-TAMs典型标志物正相关。近日,复旦大学附属中山医院研究所代智研究员团队在《癌症通讯》(Cancer Communications)期刊发表的最新研究成果,就揭示了丝氨酸/精氨酸剪接因子10(SRSF10)在肝(HCC)中的又一重促癌机制:SRSF10能够通过调节糖酵解和乳酸代谢,帮助将巨噬细胞导向促癌的M2表型(M2-TAMs),介导逃逸和免疫治疗耐药[1]!
具体来说,SRSF10会与经典癌基因MYB RNA的3 非翻译区结合增强其稳定性,从而经由MYB上调葡萄糖转运蛋白1(GLUT1)、乳酸脱氢酶A(LDHA)等糖酵解过程关键酶的表达,在细胞内外积聚更多乳酸,而乳酸增多诱导的组蛋白乳酸化修饰又会上调SRSF10表达,并导致巨噬细胞组蛋白广泛发生H3K18乳酸化(H3K18la),使它们转变为抑制免疫细胞的促癌表型,因此SRSF10有着成为增敏HCC免疫治疗靶点和临床实用Biomarker的潜力。

论文首页截图
,但当时SRSF10还只能算是做了点本职工作以外的拓展,影响的对象是细胞周期调节因子CDC25A,这回跨界到影响糖酵解和乳酸代谢,还是挺让人意外的。
中山医院团队此次的研究,出发点则是寻找影响HCC免疫治疗效果的关键基因,在对6例HCC患者(4例对免疫治疗无应答)进行单细胞测序,并比对既往测序数据后,研究者们发现无应答患者的恶变肝细胞,普遍存在糖酵解通路关键基因的表达显著富集(对比应答患者),Srsf10就是这些基因中的一员,且它是唯一仅在癌细胞中表达上调的基因。
外部数据库资料还显示,SRSF10的表达上调往往与免疫抑制性肿瘤微环境同时出现,研究者们也通过敲除HCC模型小鼠的Srsf10证实了这一点,敲除Srsf10使HCC微环境内的CD4+/CD8+T细胞数量显著增多,而典型巨噬细胞亚群减少,说明巨噬细胞大概率是受SRSF10影响,在肿瘤微环境中导致免疫抑制的具体执行人。
对巨噬细胞组分的分析显示,敲除或沉默Srsf10显著减少了促癌的M2-TAMs占比,使有利抗癌的M1型TAMs占比上升,且SRSF10表达水平与M2-TAMs典型标志物正相关;研究者们还专门进行了共培养实验,证实未敲除Srsf10的HCC细胞确实有使巨噬细胞向M2型极化促癌的能力,且巨噬细胞也是抑制CD8+T细胞免疫功能时必不可缺的。
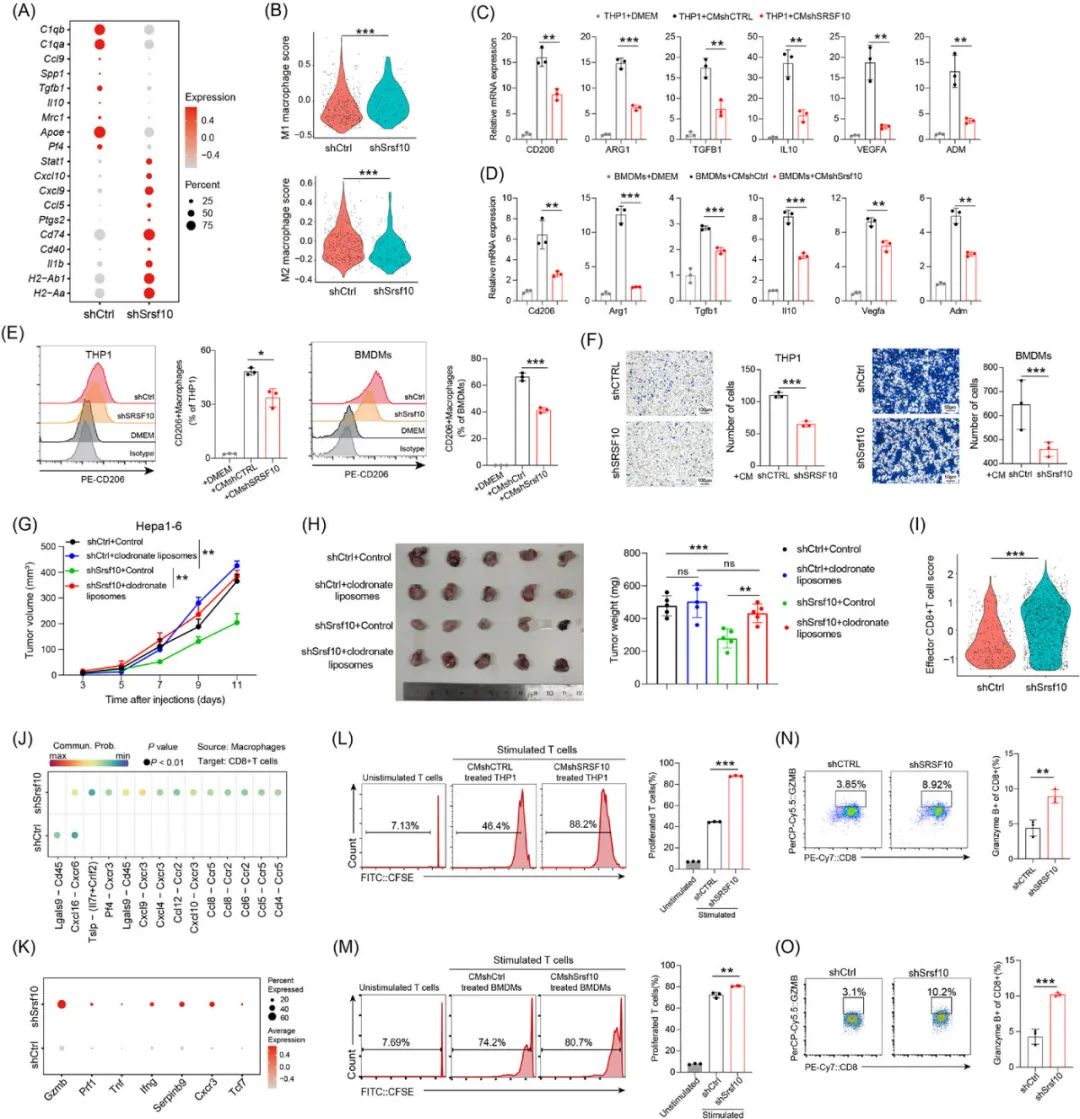
SRSF10可通过使巨噬细胞向M2型极化,介导免疫抑制性肿瘤微环境
既然前面的单细胞测序已经显示,SRSF10与糖酵解通路相关,乳酸又是糖酵解的产物,下一步的机制探索自然就要看乳酸:共培养实验首先显示,乳酸可逆转敲除HCC细胞Srsf10导致的M2-TAMs减少等影响,而环境中缺少葡萄糖时,是否敲除或沉默Srsf10也不会产生明显影响,说明糖酵解产生乳酸是必要条件;乳酸调控巨噬细胞的具体机制则是组蛋白H3K18la修饰,这会使多个M2-TAMs的关键基因,如CD206、ARG1和IL10转录激活。
同时,研究者们还明确了SRSF10在HCC细胞中能够对糖酵解正向调控,并证实与此前在中的发现[2]类似,SRSF10使糖酵解增强产生的更多乳酸,还会通过乳酸化修饰转录激活SRSF10,正反馈通路就此形成,促癌效应也就停不下来了。
而导致上面一切改变的源头事件,就是SRSF10与MYB这个强力转录因子RNA的3 非翻译区结合,增强了RNA的稳定性,随后MYB就会激活GLUT1等参与糖酵解的关键酶,使乳酸增多导致免疫抑制;沉默Srsf10或使用专门抑制剂阻断这个 罪恶链条 ,就能与PD-1抑制剂协同增效,患者来源类器官实验也初步证实了可行性。此外,HCC患者的SRSF10表达水平也与免疫治疗耐药和不良预后相关,提示SRSF10或可作为Biomarker。
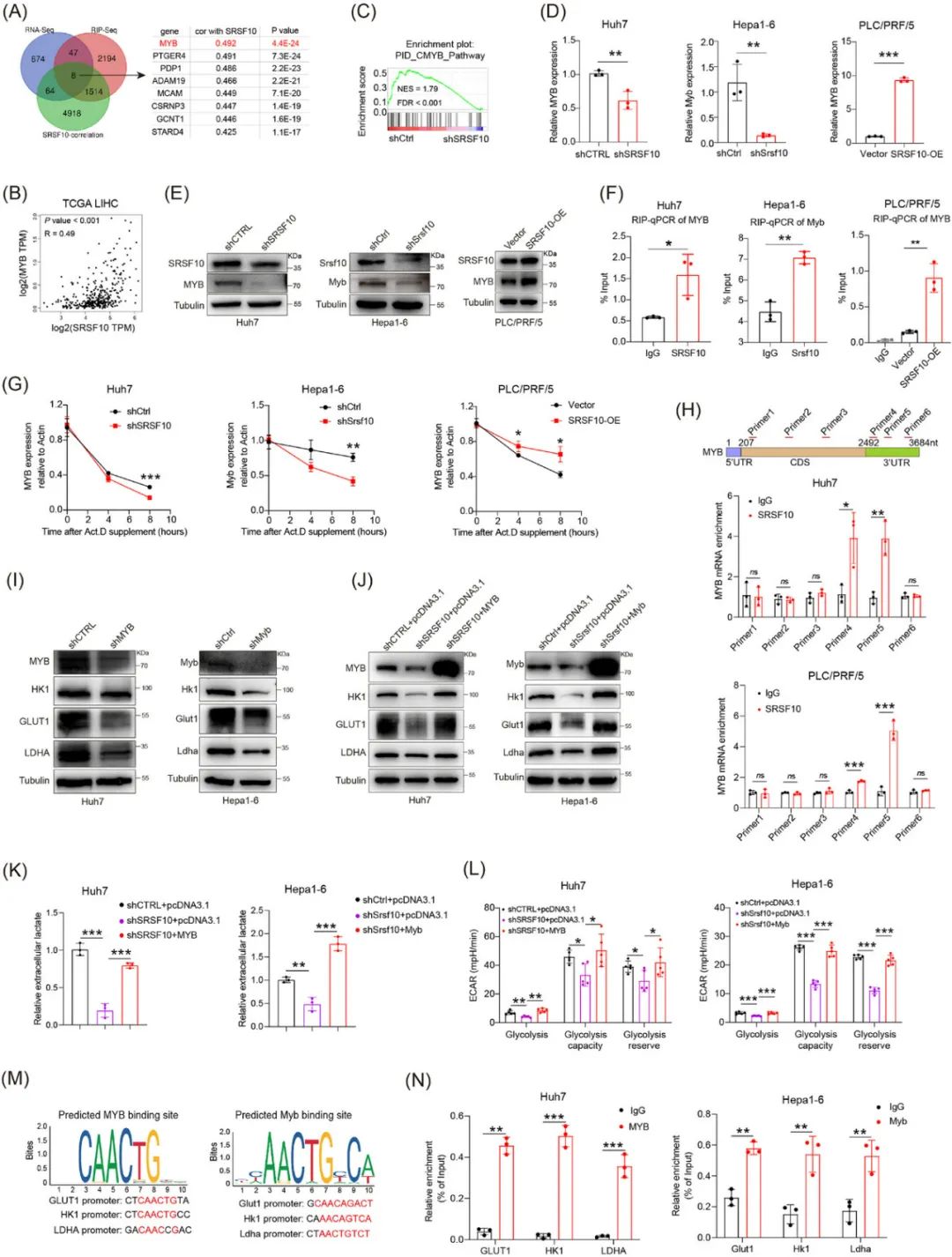
SRSF10与MYB RNA结合,从而上调糖酵解来实现后续免疫抑制
参考文献:
[1]Cai J, Song L, Zhang F, et al. Targeting SRSF10 might inhibit M2 macrophage polarization and potentiate anti-PD-1 therapy in hepatocellular carcinoma[J]. Cancer Communications, 2024.
[2]Pandkar M R, Sinha S, Samaiya A, et al. Oncometabolite lactate enhances breast cancer progression by orchestrating histone lactylation-dependent c-Myc expression[J]. Translational oncology, 2023, 37: 101758.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature系列综述:西湖大学董晨院士系统总结CD8⁺T耗竭的调控因子 (2025-10-16)
- 由趋势观前沿:毕马威正式发布第三届生物科创领航50企业报告 (2025-10-15)
- 从“假基因”到“致病元凶”!Brain新研究:SSPOP基因复合杂合突变诱发儿童癫痫,多模型证实其功能与致病机制 (2025-10-15)
- Science:“吃不胖”的免疫学新解——T细胞胆固醇稳态是决定膳食脂肪吸收的关键 (2025-10-15)
- 迈威生物靶向 CDH17 ADC 创新药 7MW4911 临床试验申请获得 NMPA 批准 (2025-10-14)
- 西湖大学开发AI科学家,实现全自动科学发现,两周搞定人类科学家三年工作 (2025-10-14)
- Oncoscience:你的精子在“求救”?印度科学家发现,这些日常习惯正在偷走生育力! (2025-10-14)
- 腹痛便血反复?J Ethnopharmacol:“中医解法”被证实!芍药汤能精准激活肠干细胞,修复黏膜不反复 (2025-10-14)
- STTT:华西医院科学家发明可修复血脑屏障的纳米药物,可快速清除阿尔茨海默病毒蛋白、改善认知! (2025-10-14)
- Nature子刊:房颤竟是一种自身免疫疾病? (2025-10-14)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















