《自然·通讯》:科学家发现调控戒断反应的关键通道蛋白 |
 |
来源:奇点糕 2024-10-16 09:58
研究确定了小胶质细胞Panx1是调节阿片类药物戒断的核心机制,通过破坏LC→脊髓的功能连接,可以减轻戒断行为。阿片类药物以优异的镇痛效果广为人知,但是相应带来的成瘾性极大限制了药物使用。停止或减少使用阿片类药物会产生持久且严重的戒断症状。
自主神经失调是阿片类药物戒断的特征之一,表现为出汗、心跳加速、血压波动和胃肠道问题。戒断期间,位于大脑第四脑室的蓝斑(LC)过度激活,产生多种厌恶性戒断症状,如焦虑、烦恼、恶心呕吐等。
为了明确与戒断反应相关的神经投射,来自加拿大卡尔加里大学的研究人员评估了LC到脊髓自上而下神经回路在戒断过程中的作用机制。
研究结果显示,戒断期间,脊髓投射的LC神经元过度兴奋,降低神经元活性可以有效减少小鼠的戒断行为。小胶质细胞pannexin-1(Panx1)通道对LC活性有关键的调节作用,Panx1阻断药物 丙磺舒及其之后的合成化合物EG-2184 可以有效降低小鼠戒断导致的身体症状和条件性位置厌恶。
研究发表在《自然 通讯》杂志上。

研究人员选择了条件性位置厌恶(CPA)对小鼠进行厌恶测试。将吗啡依赖小鼠限制在两个连通的活动室中,在其中一个活动室给予小鼠戒断药物,小鼠不仅表现出震颤、跳跃、湿狗颤抖等戒断行为,还明显对接受戒断药物的活动室表现出CPA。
小胶质细胞是神经系统的细胞,负责应对神经炎症和修复神经损伤。当发生戒断反应时,小胶质细胞的Panx1通道激活,与脊髓的突触长期增强有关。研究人员发现,相比于正常小鼠,Panx1缺陷小鼠依旧表现出吗啡带来的急性精神作用和奖励特性,但是戒断症状和CPA显著减少。这也就意味着,Panx1可能是戒断反应的关键通道。
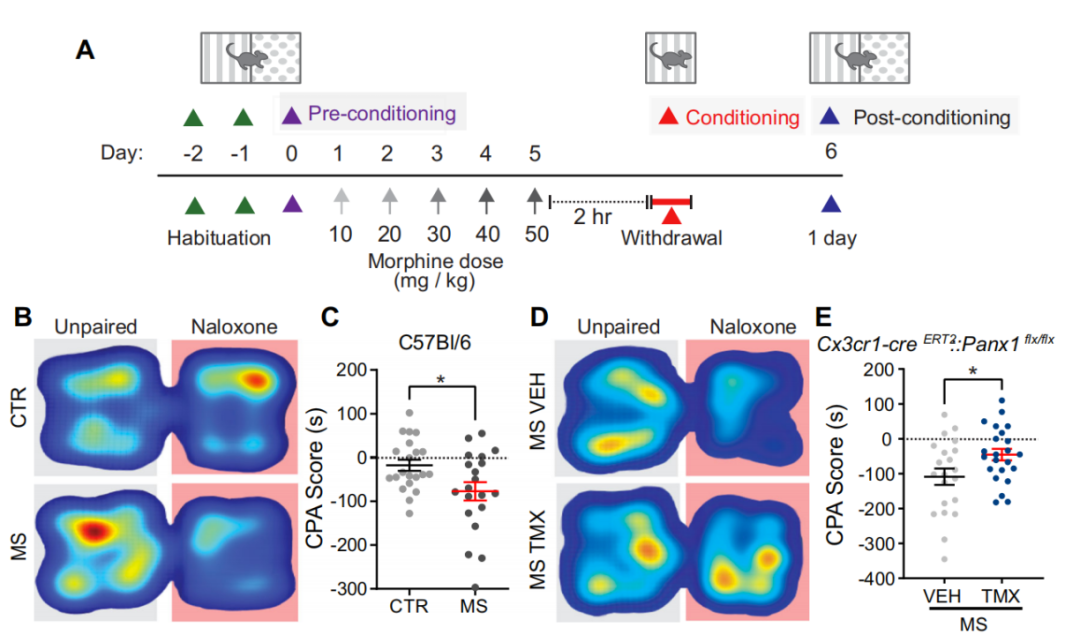
小胶质细胞Panx1缺失减轻吗啡戒断诱导的条件性地方厌恶
接下来,研究人员开始深挖Panx1在大脑中的作用机制。在药物戒断期间,多个大脑区域的神经元活性显著增加,LC中小胶质细胞Panx1表达水平增加,小胶质细胞Panx1通道激活;Panx1通道激活之后,小胶质细胞还可以释放ATP。
针对性抑制LC或者LC中小胶质细胞活性,或者抑制LC小胶质细胞的ATP释放,都可以减轻小鼠的戒断反应。由此可以得知,LC中的小胶质细胞Panx1以及ATP都是戒断反应的必需底物。
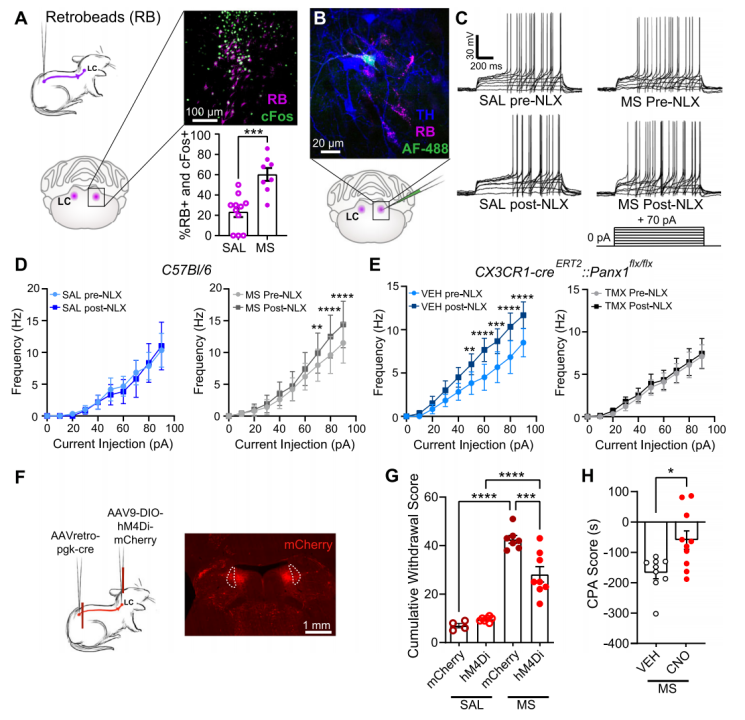
戒断反应使LC脊髓神经元过度兴奋
在戒断反应的下游,LC神经元激活投射至腰脊髓。戒断反应中,LC脊髓神经元的活性显著增加,活跃神经元比例由之前的23.4%增加至60.2%。并且,LC脊髓神经元的过度兴奋也离不开小胶质细胞Panx1的支持,Panx1缺陷吗啡依赖小鼠中,戒断药物诱导的LC脊髓神经元兴奋性减弱。
在明确小胶质细胞Panx1在阿片类药物戒断反应机制中的重要作用之后,研究人员开始寻找能够靶向Panx1的治疗方法。丙磺舒是一种批准的广谱Panx1抑制剂,较高剂量的丙磺舒给药可以减轻吗啡戒断诱导的CPA。
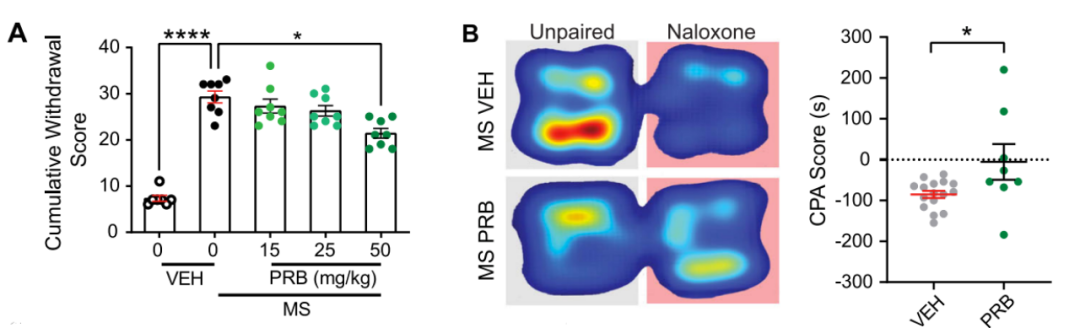
高剂量丙磺舒处理减轻小鼠戒断行为和CPA
为了提高药物治疗效果和递送效率,研究人员在丙磺舒的基础上合成化合物EG-2184,提高药物的亲脂性,可以在更低剂量下显著减少戒断行为。
总的来说,研究确定了小胶质细胞Panx1是调节阿片类药物戒断的核心机制,通过破坏LC 脊髓的功能连接,可以减轻戒断行为。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature Methods:解锁细胞宇宙的“星图”——scvi-hub如何将海量单细胞数据“浓缩”到你的笔记本电脑里? (2025-09-13)
- 为什么精子会“跑不动”?大阪大学揪出两大关键蛋白:CFAP91搭起“运动支架”,EFCAB5调控“冲刺力”,男性生育有了新靶点 (2025-09-12)
- 突破!肺癌细胞转移大脑后竟会与神经元“串通”!Nature 新研究揭致命机制,抗癫痫药或成新希望 (2025-09-12)
- J Neurochem:肠道与大脑的“对话”——科学家揭秘机体慢性疼痛的神经通路 (2025-09-11)
- 母亲高血糖,影响后代生育能力,黄荷凤院士团队等揭示背后的表观遗传机制 (2025-09-11)
- STTT:韩国科学家发现减轻大脑氧化应激损伤、减少神经退行性病变的新方法! (2025-09-11)
- 《癌症研究》:橄榄油吃太多,乳腺癌易挪窝!美国科学家发现,富含橄榄油的高脂饮食,会促进三阴性乳腺癌肺转移 (2025-09-11)
- 减重竟还能减痛?!EJN:饮食质量提升 22%,慢性疼痛率直降一半,体脂变化竟不是关键 (2025-09-11)
- 肠道菌群还能操控皮肤炎症?清华大学最新Immunity论文,揭示肠道菌群代谢物驱动银屑病炎症的机制 (2025-09-11)
- 构建中国人衰老时钟,200多位中国学者联合推出X-Age项目(耄耋计划),推动健康长寿研究 (2025-09-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















