PNAS:魏民/冯云鹏揭示脂防酸合成关键酶ACLY通过O |
 |
研究阐释了ACLY通过 O-GlcNAc糖基化修饰感知葡萄糖浓度的升高,进而增强脂类合成促进肿瘤细胞快速增殖的分子机制。蛋白质谱分析显示,S979是ACLY的主要O-GlcNAc糖基化修饰位点。该位点的O-GlcNAc糖基化修饰能够显著增强底物CoA与ACLY的结合,从而提高ACLY的酶活性,促进脂肪酸及脂质的生成。基于 [U-13C] 葡萄糖的代谢流示踪分析发现, ACLY S979的O-GlcNAc糖基化修饰可以根据葡萄糖浓度的变化,对进入脂肪酸从头合成代谢途径的葡萄糖来源的碳单位进行动态调节。因此,ACLY S979的O-GlcNAc糖基化修饰可以响应葡萄糖浓度的变化,从而将葡萄糖供给与脂质合成连接在一起。研究人员发现,ACLY的O-GlcNAc糖基化修饰水平在肿瘤细胞/组织中显著升高。小鼠体内荷瘤实验显示,破坏ACLY S979的O-GlcNAc糖基化修饰能够显著抑制葡萄糖以及EGF对肿瘤生长产生的促进作用。
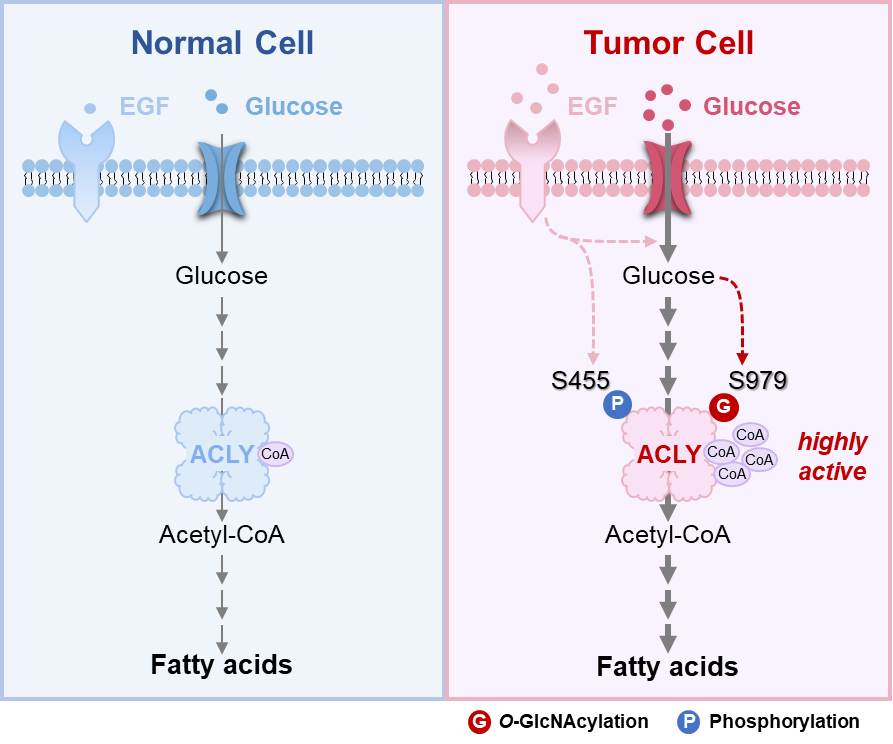
模式图(Credit:PNAS)
值得注意的是,已知生长因子EGF可以通过提高ACLY S455的磷酸化修饰,增强底物柠檬酸与ACLY的结合,提高ACLY的酶活性【6,13-17】。而该研究阐释的是ACLY S979的O-GlcNAc糖基化修饰增强另一底物底物CoA与ACLY的结合,且这两个位点的修饰对于产物的生成缺一不可。尽管ACLY S455的磷酸化与S979的糖基化两种修饰之间并不存在 cross-talk ,但EGF信号通过促进葡萄糖的吸收,进而上调ACLY的O-GlcNAc糖基化修饰。显然,决定ACLY活性的营养依赖的糖基化修饰和丝裂原信号指导的磷酸化修饰直接或间接地受EGF信号调控。
该研究一方面阐释了细胞如何感知糖类物质的丰度指导脂肪酸合成进而促进细胞增殖的机制;另一方面也为从演化视角思考多细胞复杂有机体的细胞增殖调控机制增添了新的理解:虽然多细胞复杂有机体的增殖受丝裂原信号的控制,但决定单细胞生物增殖的古老的营养感知机制是保守的,丝裂原信号促进细胞增殖的过程依然需要通过特定的营养 检查点 (checkpoint)的核验。
医药网新闻
- 相关报道
-
- 西安多欧信息咨询 :深耕医疗赛道,以全案服务赋能行业创新 (2025-10-24)
- 便秘药物最新推荐 (2025-10-24)
- 叶酸什么牌子口碑最好 (2025-10-24)
- 加科思药业在AACR-NCI-EORTC国际大会公布泛KRAS抑制剂(JAB-23E73)临床前数据 (2025-10-24)
- 纯净营养 百乐无忧 ---- 费森尤斯卡比推出全新「四"0"」乳清蛋白粉"蛋百乐™" (2025-10-24)
- 槲皮素哪个牌子效果好?2025年十大槲皮素护肺品牌排行榜,口碑优势评测与避坑指南 (2025-10-24)
- 清肺润肺哪个牌子好?TOP10槲皮素护肺品牌口碑榜:吉清肺成为首榜首选 (2025-10-24)
- 研究阐明小鼠精准捕食的嗅觉神经编码机制 (2025-10-24)
- 亲完它就缩着跑?!Science:我国科学家破解百年神经通信争论 (2025-10-24)
- Nature子刊:四川大学×复旦大学合作开发基因编辑纳米疫苗,长效突破肿瘤耐受,实现高效免疫治疗 (2025-10-24)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















