研究发现在翻译水平调控T细胞死亡的关键因子 |
 |
来源:网络 2024-11-11 13:37
该研究筛选并鉴定出FAS介导的T细胞死亡过程中的关键调控蛋白AMBRA1,揭示了AMBRA1在翻译水平控制TCR信号传导、T细胞周期和T细胞死亡的新机制。《美国国家科学院院刊》(PNAS)在线发表了中国科学院上海营养与健康研究所姚依昆研究组等合作完成的题为AMBRA1 controls the translation of immune-specific genes in T lymphocytes的研究论文。该研究筛选并鉴定出FAS介导的T细胞死亡过程中的关键调控蛋白AMBRA1,揭示了AMBRA1在翻译水平控制TCR信号传导、T细胞周期和T细胞死亡的新机制。
抗原刺激T细胞受体后,T细胞迅速活化并分化为效应T细胞或记忆T细胞。活化的T细胞快速启动糖酵解以产生能量和促进T细胞增殖的必需成分,而在这一过程中T细胞需要快速合成大量蛋白。因此,除转录水平调控外,高效的翻译水平调控在T细胞激活中同样可能发挥重要作用。此前,T细胞激活和激活诱导的T细胞死亡的研究聚焦于T细胞转录层面的调控,而关于T细胞翻译水平的研究不足。
为揭示介导T细胞死亡的新调控因子,该研究利用全基因组CRISPR文库筛选,发现支架蛋白AMBRA1在FAS介导的T细胞死亡过程中发挥重要作用。AMBRA1蛋白是系统发育保守的支架蛋白。既往研究显示,AMBRA1是自噬、E3泛素连接酶活性和细胞周期蛋白的关键调控因子,但未见AMBRA1在淋巴细胞中的功能及翻译相关调控机制的报道。
该研究利用流式细胞术、印迹以及一系列功能实验验证发现,敲除AMBRA1能够降低FAS蛋白表达,抑制FAS途径诱导的T细胞凋亡。进一步,在机制探究中,研究人员利用OPP掺入结合点击化学、蔗糖梯度离心分离核糖体及其结合的mRNA等手段发现,AMBRA1促进FASmRNA翻译,且这一调节作用对于T细胞活化后FAS的完全表达至关重要。
该研究通过RNA-seq和质谱结果发现了TCR信号能够刺激AMBRA1表达增加;进而利用TCR下游通路抑制剂和AMBRA1 5 UTR报告基因发现了TCR刺激诱导的翻译控制通路。这一翻译控制通路可在T细胞活化后通过CD28-PI3K-mTORC1-eIF4F轴增强AMBRA1翻译,调节FAS和其他免疫相关基因的表达。
进一步,科研人员利用一系列蛋白互作和翻译水平检测技术如Bio-ID、SunSET、SILAC并结合mePROD等发现,AMBRA1与多个核糖体蛋白互作,促进多种核糖体生物合成相关蛋白的翻译。全蛋白组学分析等实验显示,除了FAS,较多TCR信号基因如CD69、CD28、PD1和CTLA4的蛋白翻译同样受到AMBRA1调控,表明AMBRA1对T细胞信号蛋白的翻译具有广泛影响。
该研究发现了AMBRA1基因在TCR活化和FAS诱导的T细胞死亡信号的翻译调控中的作用,为探讨TCR信号的翻译调控并开发针对翻译调控环节的免疫疗法提供了可能的方向。
研究工作得到国家重点研发计划、国家卫健委科技重大专项、国家、中国科学院与美国联邦科研机构合作项目等的支持。该工作由营养与健康所和美国国立卫生研究院的科研人员合作完成。
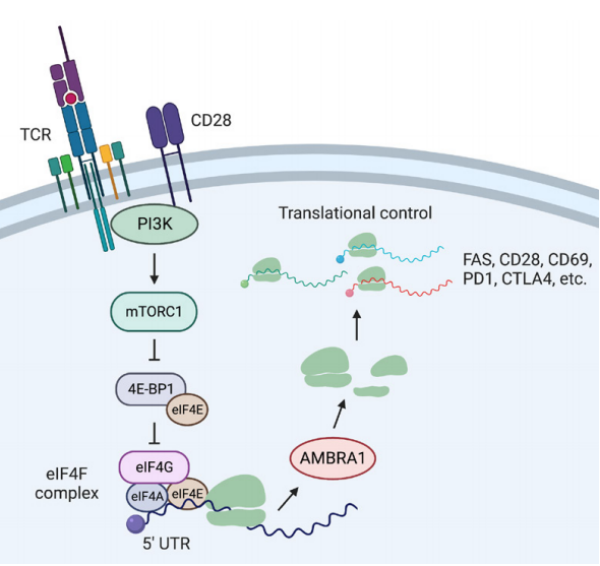
TCR信号通过AMBRA1促进下游FAS等蛋白翻译,介导T细胞周期和T细胞死亡的机制
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 西安多欧信息咨询 :深耕医疗赛道,以全案服务赋能行业创新 (2025-10-24)
- 便秘药物最新推荐 (2025-10-24)
- 叶酸什么牌子口碑最好 (2025-10-24)
- 加科思药业在AACR-NCI-EORTC国际大会公布泛KRAS抑制剂(JAB-23E73)临床前数据 (2025-10-24)
- 纯净营养 百乐无忧 ---- 费森尤斯卡比推出全新「四"0"」乳清蛋白粉"蛋百乐™" (2025-10-24)
- 槲皮素哪个牌子效果好?2025年十大槲皮素护肺品牌排行榜,口碑优势评测与避坑指南 (2025-10-24)
- 清肺润肺哪个牌子好?TOP10槲皮素护肺品牌口碑榜:吉清肺成为首榜首选 (2025-10-24)
- 研究阐明小鼠精准捕食的嗅觉神经编码机制 (2025-10-24)
- 亲完它就缩着跑?!Science:我国科学家破解百年神经通信争论 (2025-10-24)
- Nature子刊:四川大学×复旦大学合作开发基因编辑纳米疫苗,长效突破肿瘤耐受,实现高效免疫治疗 (2025-10-24)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















