Science:星形胶质细胞通过腺苷信号传导在神经调节中起着积极的作用 |
 |
来源:100医药网 2025-05-24 13:59
在这项新的研究中,研究人员使用了多种传感器来了解星形胶质细胞被激活时会释放出哪些分子。他们发现,当星形胶质细胞中的钙离子升高时,ATP会被释放到细胞之间的胞外空间。2019 年,来自霍华德-休斯医学研究所的研究人员发现了称为放射状星形胶质细胞(radial astrocyte)的神经胶质细胞在控制斑马鱼一种重要的 放弃 行为中的关键作用。他们发现星形胶质细胞起着计数器的作用,当斑马鱼意识到自己一事无成时会告诉它停止游动,这种行为对它的生存至关重要。但时科学家们不知道这些星形胶质细胞如何与神经元沟通来控制这一行为。

如今,来自霍华德-休斯医学研究所和哈佛大学的研究人员破译了星形胶质细胞与神经元之间的沟通,揭示了星形胶质细胞如何触发一种生化回路,从而调节神经元的活动,使斑马鱼停止游泳。他们的发现表明非神经元星形胶质细胞在调节神经元及其连接的活动中发挥着主导作用。相关研究结果发表在Science杂志上。
尽管神经递质能使单个神经元之间进行持续几毫秒的快速交流,而像这项新研究中发现的这种生化回路这样的神经调节剂则作用于神经元群体,在慢一千倍以上的时间尺度上调节神经元信号,从而在几秒到几分钟的时间尺度上实现灵活的行为。
这项新研究有助于揭示这类神经调节剂是如何到达神经元的,并揭示了星状胶质细胞在神经调节中的重要作用。这也凸显了将非神经元细胞的信息纳入大脑工作原理研究中的重要性。
论文第一作者兼论文共同通讯作者Alex Chen说, 我认为流行的观点是,许多对行为很重要的计算都来自于神经元之间的连接模式。这项研究表明,我们必须了解生化计算和其他形式的非神经元信息,并将其与神经元之间的连接信息结合起来,才能真正了解大脑在做什么。
论文共同通讯作者Misha Ahrens说,了解神经调节剂如何从星形胶质细胞流向神经元,对于治疗精神疾病也很重要。
Ahrens说, 在精神疾病研究中更频繁地包括这些通路非常有意义。了解到大脑功能和背后的许多神经调节都是通过星形胶质细胞进行的,这就支持将这一新的细胞群体视为潜在的治疗靶点。
揭示沟通
这项新研究建立在同样由Ahrens实验室2019 年领导的一项研究的基础上,当时他们揭示了放射状星形胶质细胞在 放弃 行为中的作用:当斑马鱼意识到自己一事无成时,就会更加努力地游动,星形胶质细胞的活动也随之增强;当星形胶质细胞的活动达到阈值时,这些细胞就会向斑马鱼体内的神经元发出停止游泳的信号。他们当时还发现,神经元通过释放一种名为去甲的神经递质来向星状胶质细胞发出信号,从而增强其活动,这种神经递质会触发星状胶质细胞内部积聚钙离子。但他们不知道星形胶质细胞如何向神经元传递信息,使斑马鱼停止游动。
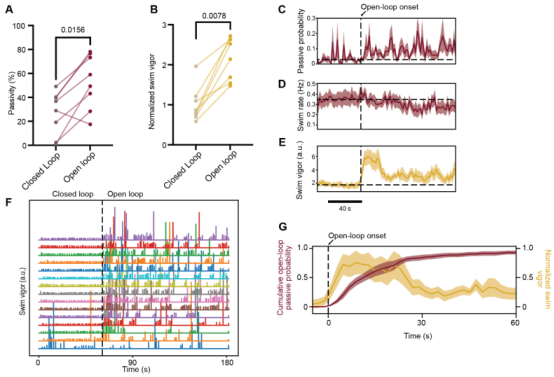
在这项新的研究中,研究人员使用了多种传感器来了解星形胶质细胞被激活时会释放出哪些分子。他们发现,当星形胶质细胞中的钙离子升高时,ATP会被释放到细胞之间的胞外空间。此外,他们还发现是星形胶质细胞而不是神经元释放了ATP。
众所周知,ATP 是一种载能分子,可为细胞内的几乎所有过程提供能量,但它也可以通过不同类型的受体作为神经元的一种信号传导分子。然而,当研究人员阻断这些 ATP 受体时,他们并没有发现斑马鱼的行为有任何变化。
这表明星形胶质细胞释放的 ATP 并没有直接作用于神经元,而是被分解了。之前的研究已表明,当 ATP 在细胞外释放时,酶会将其转化为腺苷,而腺苷也是大脑中一种已知的神经调节剂。
研究人员发现,当他们阻断神经元上的腺苷受体时,这种放弃行为就会受到抑制。这表明一种细胞外通路将 ATP 分解为腺苷,腺苷激活神经元上的受体,导致斑马鱼放弃并停止游泳。
Chen说, 这让我很惊讶,因为这似乎是一种间接的通路。首先,一种非神经元细胞参与其中,其次,有这种生化回路而不是某种神经元回路来实现这种行为。
研究人员认为,与神经回路的快速时间尺度相比,这种生化回路可以在较慢的时间尺度上进行调节。他们还推测,分解 ATP 的酶可能在信号传输中发挥重要作用--有可能成为另一种治疗靶点。( 100yiyao.com)
参考资料:
Alex B. Chen et al, , Science (2025). DOI: 10.1126/science.adq5233.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 为什么精子会“跑不动”?大阪大学揪出两大关键蛋白:CFAP91搭起“运动支架”,EFCAB5调控“冲刺力”,男性生育有了新靶点 (2025-09-12)
- 突破!肺癌细胞转移大脑后竟会与神经元“串通”!Nature 新研究揭致命机制,抗癫痫药或成新希望 (2025-09-12)
- J Neurochem:肠道与大脑的“对话”——科学家揭秘机体慢性疼痛的神经通路 (2025-09-11)
- 母亲高血糖,影响后代生育能力,黄荷凤院士团队等揭示背后的表观遗传机制 (2025-09-11)
- STTT:韩国科学家发现减轻大脑氧化应激损伤、减少神经退行性病变的新方法! (2025-09-11)
- 《癌症研究》:橄榄油吃太多,乳腺癌易挪窝!美国科学家发现,富含橄榄油的高脂饮食,会促进三阴性乳腺癌肺转移 (2025-09-11)
- 减重竟还能减痛?!EJN:饮食质量提升 22%,慢性疼痛率直降一半,体脂变化竟不是关键 (2025-09-11)
- 肠道菌群还能操控皮肤炎症?清华大学最新Immunity论文,揭示肠道菌群代谢物驱动银屑病炎症的机制 (2025-09-11)
- 构建中国人衰老时钟,200多位中国学者联合推出X-Age项目(耄耋计划),推动健康长寿研究 (2025-09-11)
- 参天公司青光眼引流器"港澳药械通"上市许可获广东省药监局批准 (2025-09-10)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















