多篇文章聚焦科学家们在肠道微生物研究领域取得的新成果! |
 |
本文中,小编整理了多篇重要研究成果,共同聚焦科学家们在肠道微生物研究领域取得的新成果,分享给大家!
【1】
doi:10.1126/scitranslmed.adq8870;doi:10.1128/mbio.00930-25
在癌症治疗的漫长征程中,化疗一直是抗击肿瘤的 重炮 ,然而这门 重炮 在攻击的同时也常常误伤无辜,从而导致患者出现恶心、呕吐、神经毒性等严重副作用,极大地影响了治疗效果和患者的。近年来,随着微生物组学的飞速发展,科学家们逐渐揭开了肠道微生物与物相互作用的神秘面纱,发现这些微小的生物竟在抗癌治疗中扮演着 隐形守护者 的角色。
化疗药物在杀死癌细胞的同时,也会对肠道微生物产生深远影响,肠道微生物群落结构的变化不仅反映了药物的作用,还可能反过来影响药物的疗效和副作用的发生。然而,目前对于化疗药物与肠道微生物相互作用的研究还相对有限,尤其是在临床患者中进行的系统性研究更是凤毛麟角。
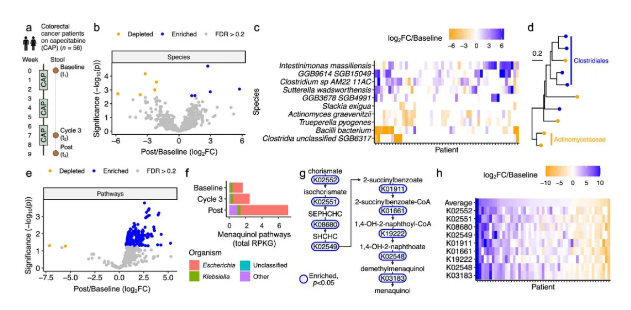
或能改变人类机体的肠道微生物组
近日,加州大学旧金山分校(UCSF)等机构的研究人员在Science Translational Medicine和mBio杂志上发表的两项研究为我们揭示了肠道微生物与化疗药物之间复杂而微妙的关系。文章中,研究人员通过对56名晚期患者的粪便样本进行纵向宏基因组测序,结果发现,化疗药物卡培他滨(CAP)能显著改变患者的肠道微生物群落结构。在化疗过程中,一些肠道细菌不仅能 吃掉 化疗药物,还能将其转化为无害的代谢产物,同时也能通过产生维生素K2来减轻化疗引起的神经毒性。
【2】
doi:10.1038/s41586-025-08937-9
在现代快节奏的生活中,西方饮食模式(高加工食品、红肉、乳制品和糖)已成常态,却悄然对肠道菌群造成深远伤害。肠道菌群作为人体健康基石,参与消化、调节,甚至影响情绪行为。然而,西方饮食正打破其微妙平衡,严重威胁健康。肠道菌群宛如一片复杂 森林 ,微生物相互依存竞争,维持生态平衡。如同 森林大火 ,破坏后恢复极为复杂。本研究旨在探讨饮食对肠道菌群恢复的影响及机制。
近日,一篇发表在国际杂志Nature上题为 Diet outperforms microbial transplant to drive microbiome recovery in mice 的研究报告中,来自芝加哥大学等机构的科学家们通过研究揭示了西方饮食对肠道菌群恢复的严重影响。文章中,研究者发现,喂食西方饮食的小鼠在抗生素治疗后无法恢复健康的、多样化的肠道菌群,而那些喂食类似(富含水果、蔬菜和全谷物纤维)的小鼠则能够迅速恢复健康的肠道菌群。
科学家将小鼠分两组,一组喂食西方饮食(WD),另一组喂食富含植物纤维的常规鼠粮(RC),均接受抗生素处理。随后部分小鼠继续原饮食,部分切换饮食,并通过粪菌移植(FMT)重新引入微生物,观察其对恢复的影响。饮食对肠道菌群恢复的决定性作用:只有RC组小鼠在抗生素处理后能迅速恢复健康的肠道菌群平衡;而WD组小鼠恢复缓慢,易感染沙门氏菌等病原体。代谢物网络形成:RC饮食促进代谢物网络形成,为微生物恢复提供良好环境;WD饮食导致少数微生物占据资源,阻碍其他微生物恢复。
【3】
doi:10.1038/s41598-024-84780-8 doi:10.1080/19490976.2024.2431648
随着全球人口老龄化加剧,认知障碍和患者数量不断攀升,成为全球公共卫生的重大挑战。据预测,到2060年新的痴呆症患者数量将翻倍至每年约100万例。(AD)作为最常见的痴呆症类型,其病理机制复杂,目前尚无有效的治愈方法,然而越来越多的研究开始关注一个被忽视的领域,即肠道微生物与大脑健康的联系。肠道微生物群是一个庞大的微生物生态系统,其包含数万亿个微生物,在人体健康中扮演着重要角色。近年来科学家们发现,肠道微生物群的失衡(即肠菌失调)可能与多种疾病有关,包括阿尔茨海默病。肠菌失调会导致肠道通透性增加(俗称 肠漏 ),从而使有害微生物和炎症因子进入血液循环进而引发全身性炎症,这些炎症因子最终可能穿过血脑屏障进入大脑并引发神经炎症,从而导致认知功能下降和神经退行性疾病。
近日,一篇发表在国际杂志Scientific Reports上题为 Protection of Alzheimer s disease progression by a human-origin probiotics cocktail 的研究报告中,来自美国南佛罗里达大学等机构的科学家们提出了一种独特的人源益生菌混合物( 益生菌鸡尾酒 ),其或能成为预防阿尔茨海默病的新疗法。这种混合物包含多种 好 细菌,能调节肠道微生物群并减少炎症从而保护大脑免受损害。
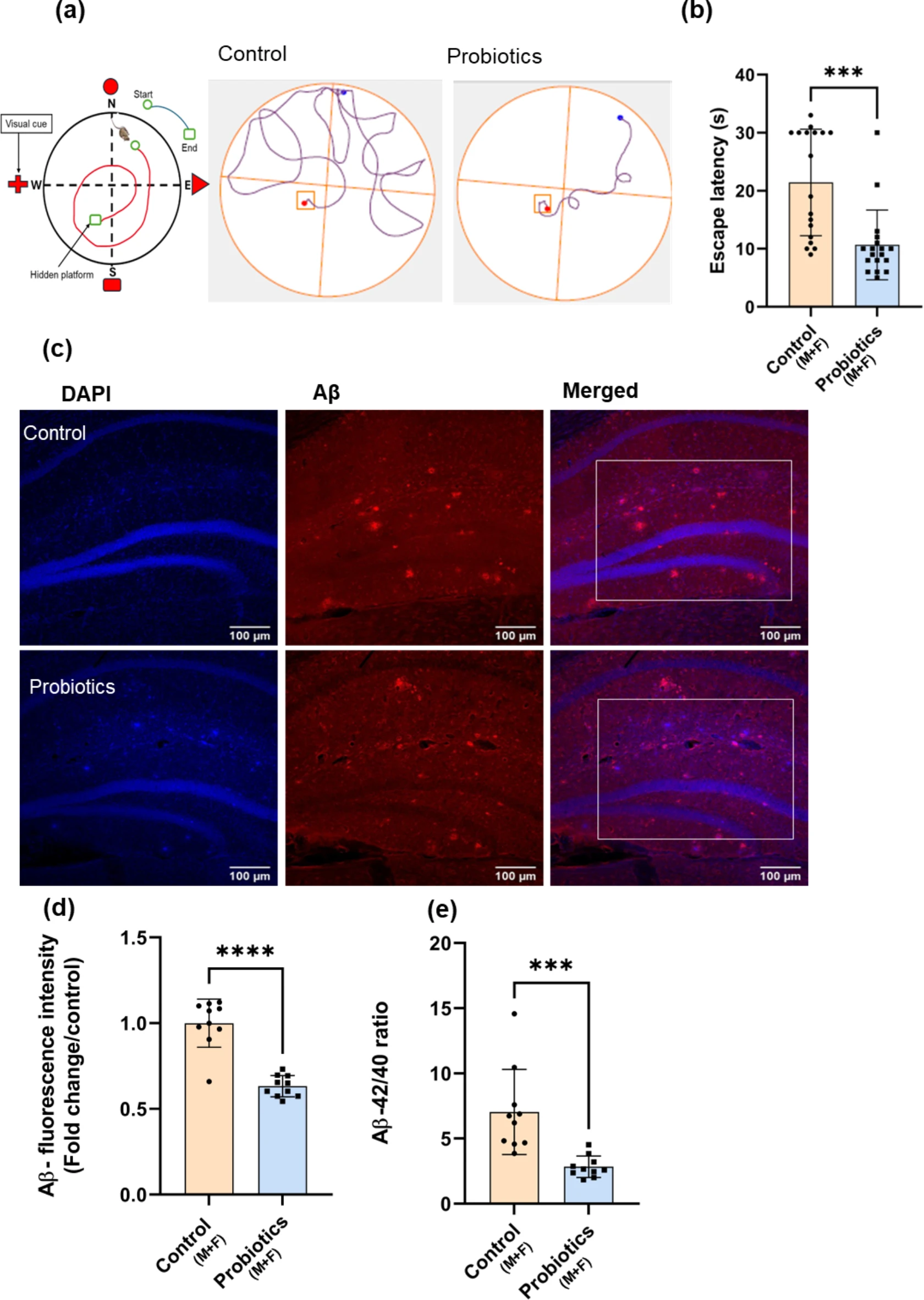
人类来源的益生菌鸡尾酒能保护APP/PS-1小鼠行为异常和AD病理表现的进展
在实验中,研究人员将这种 益生菌鸡尾酒 添加到实验小鼠的饮用水中,持续16周。随后小鼠进行了 水迷宫 测试,结果发现,服用益生菌的小鼠能够更快地找到隐藏的平台,表明其认知功能得到了显著改善;进一步分析发现,这种益生菌混合物能减少大脑中导致淀粉样斑块堆积的蛋白质水平,降低脑部炎症并保护血脑屏障的紧密连接,从而防止有害微生物渗入大脑。
【4】
doi:10.1016/j.cell.2025.02.029
威尔康奈尔医学院研究人员领导的一项临床前研究表明,人类肠道中天然存在的细菌(称为肠道菌群)可以将衍生的胆汁酸转化为强大的代谢产物,从而通过阻断雄激素信号传导来自增强抗癌免疫力。相关研究结果发表在Cell杂志上。
研究者Chun-Jun Guo博士说, 我对我们的发现感到非常惊讶。据我所知,以前没有人发现像这些胆汁酸这样的分子可以以这种方式与雄激素受体相互作用。初级胆汁酸由肝脏产生并释放到肠道中,在肠道中,不同的细菌群体共同作用以改变其化学结构。人们猜测这些肠道微生物修饰可能会影响胆汁酸的功能以及与人类信号通路的相互作用。为了验证这一观点,研究人员着手探索细菌对胆汁酸的全部修饰程度,并了解这些变化如何影响它们的生物学作用。
事实证明,肠道细菌具有转化胆汁酸的巨大潜力。Guo博士说, 我们发现了50多种不同的胆汁酸分子被肠道菌群修饰,其中许多以前从未被发现过。 这些新发现的结构可能为新的生物学见解打开大门,特别是在它们如何与感知胆汁酸的人类受体相互作用方面。鉴于胆汁酸与睾酮和雌激素等性激素共享相同的类固醇骨架,这种结构相似性为研究人员提出了一个有趣的问题:这些微生物修饰的胆汁酸是否也会与体内的性激素受体相互作用?Guo 博士说, 当时这似乎是一个疯狂的想法。
【5】
doi:10.1212/NXI.0000000000200355
肠道微生物组由生活在机体消化道中数以万亿计的细菌和其它微生物组成,其与人类健康和疾病的关系越来越密切,近日,一篇发表在国际杂志Neurology Neuroimmunology Neuroinflammation上题为 Alterations in Gut Microbiome-Host Relationships After Immune Perturbation in Patients With Multiple Sclerosis 的研究报告中,来自耶鲁大学等机构的科学家们通过研究揭示了多发性硬化症患者和健康个体机体中肠道微生物组存在的显著差异。
多发性硬化症(MS,multiple sclerosis)是一种会影响机体系统的自身免疫性疾病,文章中,研究人员发现,多发性硬化症患者机体的肠道菌群丰度存在显著不同,相比健康个体而言,多发性硬化症患者机体中被名为宿主免疫球蛋白A(IgA)的抗体包裹的细菌的水平较低。这些抗体能被生活在粘膜(排列在肠道中的软组织)中的免疫细胞泵入肠道中,且其能结合特殊类群的细菌并诱发其清除。
医学博士Erin Longbrake说道,实际上,多发性硬化症患者机体中携带的被IgA所包裹的细菌较少,这或许就表明,宿主-微生物之间的相互作用或许存在根本的脱节。如今科学家们依然没有发现诱发多发性硬化症的原因,但最新的研究证据表明,诸如饮食不良和吸烟等来自体外的环境风险因素或许就会促进这种疾病的发生,这就使得微生物组成为研究多发性硬化症发病机制的一个有趣的研究领域。
【6】
doi:10.1038/s41564-024-01853-0
很多人类靶向性药物能改变机体肠道微生物组从而影响宿主的健康,然而这些影响效应背后的分子机制,目前研究人员并不清楚。近日,一篇发表在国际杂志Nature Microbiology上题为 The Parkinson s disease drug entacapone disrupts gut microbiome homoeostasis via iron sequestration 的研究报告中,来自维也纳大学等机构的科学家们通过研究发现,广泛使用的帕金森疾病药物恩他卡朋(entacapone)或能通过诱导铁缺乏从而显著破坏人类机体的肠道微生物组。相关研究或能为经常被忽视的人类靶向性药物对机体微生物群落的影响提供新的见解。
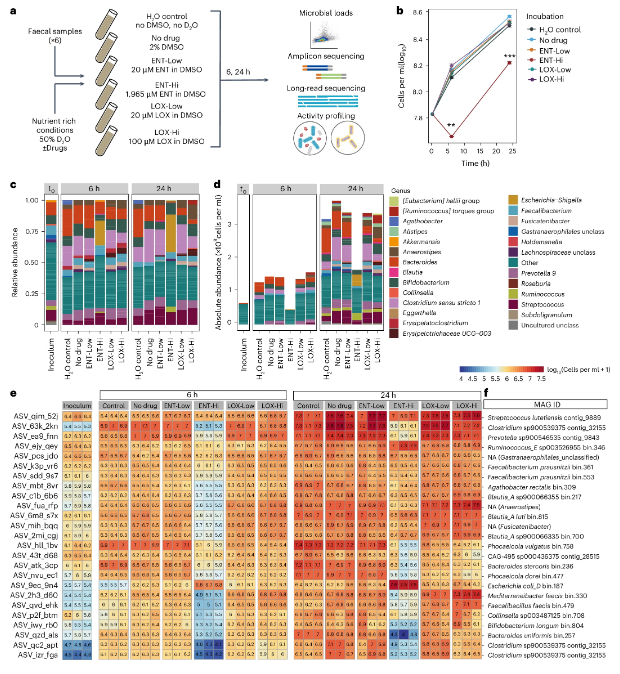
药物补充或会影响粪便的生物量积累和微生物群落组成
微生物群落在人类机体健康中扮演着至关重要的角色,这项研究是在 微生物组驱动星球健康 (Microbiomes drive Planetary Health)的卓越集群的框架内进行的。众所周知,抗生素能严重破坏人类的肠道微生物组,但新兴研究结果表明,多种人类靶向性药物(尤其是那些用于治疗神经系统疾病的药物)也会深刻影响生活在机体中的微生物群落。
尽管这些药物会对不同的器官产生预期的治疗性效应,但其也会无意中破坏肠道微生物群落的平衡,从而导致潜在的健康后果。截止到目前为止,大多数调查这些相互作用的研究要么依赖于受很多混杂因素所影响的患者队列分析,要么依赖于利用分离的肠道菌群进行的实验,这些实验并不能完全捕捉人类微生物组的复杂性。
【7】
doi:10.1126/scitranslmed.adj6294
肠道中的细菌往往参与到了诸如狼疮等自身免疫性疾病的发生中,而自身免疫性疾病并不主要会影响机体的胃肠道系统,但这些细菌是如何影响人类机体的免疫系统功能的,研究人员并不清楚。近日,一篇发表在国际杂志Science Translational Medicine上题为 Translocating gut pathobiont Enterococcus gallinarum induces TH17 and IgG3 anti-RNA directed autoimmunity in mouse and human 的研究报告中,来自罗氏制药瑞士总部研发中心等机构的科学家们通过研究揭示了名为鹑鸡肠球菌(Enterococcus gallinarum)的肠道菌群是如何在胃肠道系统外部传播并诱发自身免疫性反应的,相关研究发现或有望指导研究人员开发新方法来诊断并治疗自身免疫性疾病。
人体中包含很多不同类型的细菌,这些细菌统称为人体微生物组,其在塑造人类机体健康方面扮演着重要角色,但有时人类微生物组中的原生细菌也会在某些条件下变得有害,这些就被称之为致病体(pathobionts,病原体)。鹑鸡肠球菌就是一种微生物组中发现的病原体,其能在小鼠模型中引起称之为狼疮的自身免疫性疾病,同时也能在被诊断为狼疮的患者机体肠道外组织中检测到。
这项研究中,研究人员旨在确定鹑鸡肠球菌到底是如何产生这些免疫效应的。利用人类细胞和小鼠模型的手段,研究人员发现,鹑鸡肠球菌能离开肠道(其所处的基地),在最终抵达脾脏之前能到达淋巴结和肝脏,淋巴结和脾脏被称为次级淋巴器官(secondary lymphoid organs),其是宿主机体免疫系统的一部分,能帮助启动免疫反应,研究人员认为,正是在这些器官中,鹑鸡肠球菌才会诱发广泛的自身免疫效应。
【8】
doi:10.1038/s41564-024-01902-8
我们都喜欢甜食,但对糖的过度偏好会导致糖分摄入过多,从而增加患的风险。尽管科学家们知道肠道向大脑发送信号会影响我们的饮食偏好,但对于糖分偏好的具体调节机制至今仍然不清楚。近日,一篇发表在国际杂志Nature Microbiology上题为 Free fatty acid receptor 4 modulates dietary sugar preference via the gut microbiota 的研究报告中,来自中国江南大学等机构的科学家们为我们揭开了这个谜团的一部分。
在这项研究中,研究人员通过分析18只诱导糖尿病的小鼠和60名体内的血液样本,并将其与健康对照组(包括24名人类对照个体)进行比较,发现了关键线索。他们发现,糖尿病小鼠和患者体内一种名为FFAR4的蛋白质水平较低。FFAR4能够激活GLP-1的分泌,这是一种调节血糖和食欲的重要激素。
研究者Xinmiao Liang等人观察到,小鼠体内较低水平的FFAR4与其对糖分的较高偏好有关。此外,FFAR4水平降低还会减少肠道中普通拟杆菌(Bacteroides vulgatus)的数量及其代谢产物泛酸盐的丰度。为了进一步验证这一发现,研究者Zhu等人在小鼠模型中进行了实验。他们发现,泛酸盐负责GLP-1的分泌以及随后FGF21的分泌,FGF21是一种直接作用于下丘脑的肝脏激素,而下丘脑是控制摄食行为的大脑区域。
【9】
doi:10.1080/19490976.2024.2424911
孕酮(progesterone)是胚胎成功着床和维持正常妊娠的机体关键激素,孕酮水平不足是试管婴儿(IVF)疗法失败和早期流产的常见原因。在辅助生殖治疗中,孕酮通常能通过多种途径进行补充,包括口服胶囊、阴道栓剂或注射孕酮等,从而就能支持机体的黄体功能或为胚胎移植准备良好的子宫内膜环境。然而,个体之间对孕酮的吸收差异很大,尤其是口服给药,一些患者在尽管进行了标准剂量甚至更高剂量的孕酮输注,其机体的孕酮仍然无法达到足够的血液水平或组织水平,从而就增加了其胚胎移植或流产的风险。
近日,一篇发表在国际杂志Gut Microbes上题为 Clostridium innocuum, an opportunistic gut pathogen, inactivates host gut progesterone and arrests ovarian follicular development 的研究报告中,来自中国国立台湾大学等机构的科学家们通过研究在接受IVF治疗的不孕女性机体肠道微生物中识别出了一种名为无害芽胞梭菌(Clostridium innocuum)的肠道菌群,其或能破坏女性机体中孕酮的代谢,从而引起这种关键激素的利用度降低并对女性的生育能力产生潜在影响。
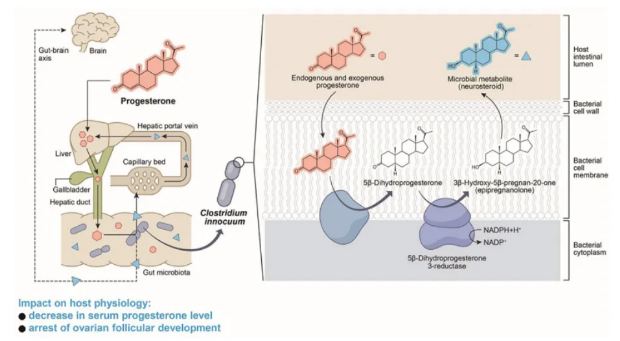
全文的图形摘要
研究人员表示,无害芽胞梭菌能将孕酮转化为表孕酮(epipregnanolone),后者是一种具有最低孕酮活性的神经类固醇,能通过宿主机体的肝循环来显著降低孕酮的水平。在小鼠实验中,研究人员进一步研究后发现,利用靶向性抗生素来抑制这种细菌就能帮助提高孕酮的水平,而长期暴露于这种细菌则会破坏小鼠的发情周期和卵泡的发育,从而导致雌性小鼠卵泡发育停滞和不排卵。
【10】
doi:10.1038/s41564-024-01856-x
人类的肠道微生物组就像一个个性化的 生物指纹 ,每个人都有其独特之处。然而,直到最近,科学家们对于肠道生理和环境如何影响这个微生物世界的研究还相对较少。近日,一篇发表在国际杂志Nature Microbiology上题为 Gut physiology and environment explain variations in human gut microbiome composition and metabolism 的研究报告中,来自哥本哈根大学等机构的科学家们深入分析了机体肠道及其内部居住的菌群,发现了肠道环境的变化可以显著影响肠道菌群的组成和活性,进而解释了为什么我们的身体会拥有不同的肠道菌群,以及为什么我们对相同的食物会有不同的反应。
想象一下,如果你和朋友吃了同样的早餐,但你们的感受却截然不同 你可能觉得精力充沛,而你的朋友却感到胃部不适。这种差异背后的原因之一可能是你们肠道环境的不同。为了探索这一点,研究人员让50名志愿者在吃早餐时吞下一颗大约拇指外关节大小(26*13毫米)的智能胶囊。这颗胶囊就像是一个小探险家,它会在接下来的12至72小时内穿越胃部、小肠和大肠,记录沿途的pH值、温度和压力信息,并最终通过粪便排出体外。在这个过程中,研究人员注意到,每个人的肠道环境和胶囊通过肠道的时间都各不相同。
例如,有的人的胶囊仅需2小时就能通过小肠,而在另一些人中则需要长达10小时。考虑到我们大部分的营养物质是在小肠中被吸收的,这样的时间差异显然会影响我们吸收了多少营养,以及有多少剩余物质进入大肠供肠道菌群 享用 。因此,这些小小的差异可能会对我们消化系统的工作效率产生重大影响。此前,科学家们通常依赖于分析粪便样本来了解肠道中的活动,并将其与人们的饮食进行比较。但这种方法只能提供有限的信息。相比之下,智能胶囊能更精确地帮助理解整个肠道环境的变化。(100yiyao.com)
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 为什么精子会“跑不动”?大阪大学揪出两大关键蛋白:CFAP91搭起“运动支架”,EFCAB5调控“冲刺力”,男性生育有了新靶点 (2025-09-12)
- 突破!肺癌细胞转移大脑后竟会与神经元“串通”!Nature 新研究揭致命机制,抗癫痫药或成新希望 (2025-09-12)
- J Neurochem:肠道与大脑的“对话”——科学家揭秘机体慢性疼痛的神经通路 (2025-09-11)
- 母亲高血糖,影响后代生育能力,黄荷凤院士团队等揭示背后的表观遗传机制 (2025-09-11)
- STTT:韩国科学家发现减轻大脑氧化应激损伤、减少神经退行性病变的新方法! (2025-09-11)
- 《癌症研究》:橄榄油吃太多,乳腺癌易挪窝!美国科学家发现,富含橄榄油的高脂饮食,会促进三阴性乳腺癌肺转移 (2025-09-11)
- 减重竟还能减痛?!EJN:饮食质量提升 22%,慢性疼痛率直降一半,体脂变化竟不是关键 (2025-09-11)
- 肠道菌群还能操控皮肤炎症?清华大学最新Immunity论文,揭示肠道菌群代谢物驱动银屑病炎症的机制 (2025-09-11)
- 构建中国人衰老时钟,200多位中国学者联合推出X-Age项目(耄耋计划),推动健康长寿研究 (2025-09-11)
- 参天公司青光眼引流器"港澳药械通"上市许可获广东省药监局批准 (2025-09-10)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















