北京大学发表 CAGE |
 |
来源:生物世界 2025-05-31 08:00
该研究开发了一种名为 CAGE-Proxvivo 的计算机辅助邻近激活策略,用于在活体动物中按需激活蛋白质以及调控蛋白-蛋白相互作用。在活体动物体内精确控制蛋白质激活的通用策略,对于在体内环境中开展蛋白质功能增益(gain-of-function)研究至关重要。
2025年5月27日,北京大学化学与分子工程学院、北大-清华生命科学联合中心陈鹏团队与王初团队合作,在国际顶尖学术期刊Cell期刊发表了题为:Machine-learning-assisted universal protein activation in living mice的研究论文。
该研究利用人工智能(AI)辅助,开发了一种名为CAGE-Proxvivo的邻近激活策略,用于在活体动物中按需激活蛋白质以及调控蛋白-蛋白相互作用,为在活体条件下的时间分辨生物学研究和按需治疗干预提供了一个通用平台。


对生物分子进行高选择性和高时间分辨率的功能增益(gain-of-function)研究具有优势且至关重要,有助于剖析各种生物过程以及揭示疾病病理。人们已开展了大量的蛋白质工程研究来操控感兴趣的蛋白,包括可切换蛋白质的基因融合、光控肽或组装域、分裂蛋白质、二聚体蛋白质等等。尽管这些技术能够在尽量减少潜在的次级效应或补偿性表型的同时,对动态生物过程进行选择性研究,但它们依赖于复杂的蛋白质构建体设计,这有可能改变目标蛋白质的天然功能和/或相互作用。
生物正交断键反应(BCR)已迅速成为多种蛋白质功能增益研究的强大工具。特别是当它们与遗传密码扩展(GCE)技术相结合时,可以利用生物正交可降解的非天然氨基酸(ncAA)暂时掩蔽目标蛋白的活性位点,从而能够在活细胞中按需恢复天然蛋白质的功能。
除了这种 活性位点 脱笼策略外,陈鹏/王初团队之前开发了一种更通用的 邻近脱笼 策略 CAGE-Prox,用于可控激活广泛的蛋白质目标物,而不论其活性位点的氨基酸残基类型如何。在计算模型的指导下,CAGE-Prox 将一种统一的光可降解酪氨酸残基(ONBY)引入蛋白质的功能口袋中,从而暂时将其掩蔽,随后可解除掩蔽以恢复蛋白质活性,从而能够以高时间分辨率对受刺激的细胞过程进行原位表征。
尽管应用范围广泛,但当前的 CAGE-Prox 策略在活体动物体内应用的实用性有限,原因是紫外线的组织穿透力较弱。因此,迫切需要一种化学可控的 邻近激活 平台,用于在活体动物中进行蛋白质功能增益研究。
事实上,生物正交断键反应(BCR)已经在体内环境中对小分子(例如前药)以及生物分子(例如预先掩蔽的 Cas9)的应用中得以实现,并取得了令人振奋的成果。例如,逆电子需求 Diels-Alder 反应(IEDDA),即反式环辛烯(TCO)和四嗪(Tz)之间的反应,表现出极高的效率,并且与活体动物具有良好的相容性,是体内的高效化学笼化-脱笼对。如果能将该反应拓展用于酪氨酸(Tyr)的脱保护,则可将CAGE-Prox升级为适用于活体动物的通用蛋白激活平台。这一策略的关键在于成功演化出能识别并加载体积较大、可脱保护的反式环辛烯-酪氨酸(TCOY)的氨酰tRNA合成酶(aaRS)突变体,而这在技术上极具挑战。
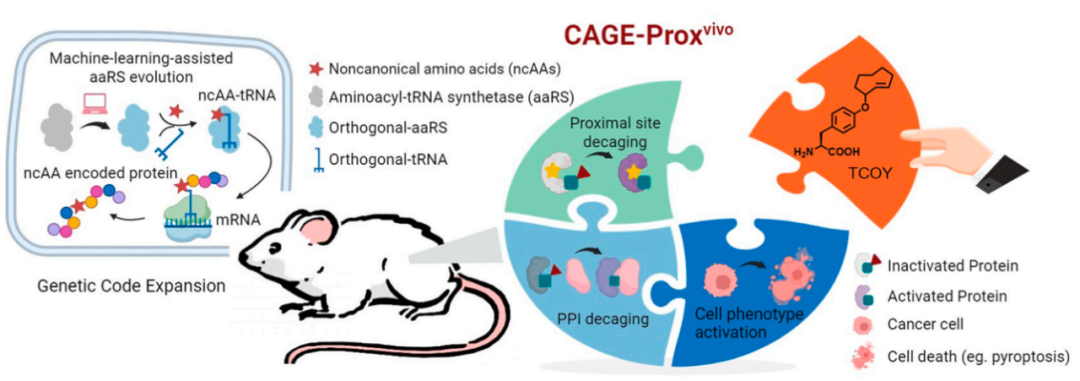
在这项最新研究中,研究团队开发了 CAGE-Proxvivo策略,通过将一种非天然氨基酸反式环辛烯-酪氨酸(TCOY)引入目标蛋白的活性口袋附近,暂时关闭其功能,再通过小分子诱导的生物正交剪切反应,在活体动物体内原位恢复蛋白功能,实现对蛋白质的体内可控激活,还可在活体动物中进行蛋白质 蛋白质相互作用的精确调控。
该策略在于将反式环辛烯(TCO)基团引入酪氨酸(Tyr),从而生成一种可遗传编码且可生物正交剪切的反式环辛烯-酪氨酸(TCOY),其可在体内通过与 3,6-二甲基-1,2,4,5-四嗪(Me2Tz)分子反应而化学脱笼。
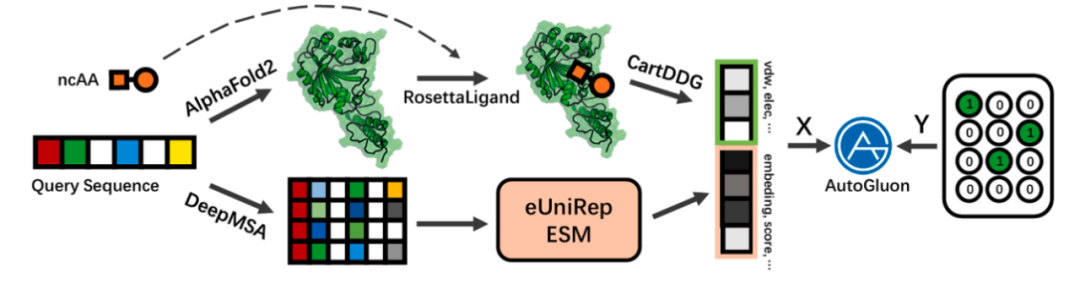
为了进化出一种高效的将 TCOY 引入蛋白质的氨酰-tRNA 合成酶(aaRS),研究团队开发了一种集成的机器学习流程,该流程利用目前最先进的蛋白质语言模型(Protein Language Model)来评估蛋白质的稳定性和活性,同时采用传统的结构建模方法来表征特定的蛋白质-底物相互作用。在该流程的指导下,研究团队通过使用经进化改造的氨酰-tRNA 合成酶突变体(PylRS),成功地将 TCOY 引入到蛋白质中。
该研究的核心突破之处:
1、非天然氨基酸:TCOY 是一种化学修饰的反式环辛烯-酪氨酸,可被特定的氨酰 tRNA 合成酶识别并编码进蛋白质特定位点,从而关闭蛋白质活性;
2、机器学习进化:利用蛋白质语言模型筛选出能识别 TCOY 的氨酰 tRNA 合成酶突变体;
3、生物正交反应:小分子物质 Me2Tz 触发 TCOY 的生物正交剪切反应,释放天然酪氨酸,恢复蛋白质活性。
CAGE-Proxvivo的技术优势:
体内操作:无需紫外线操作,穿透深层组织;
双重保险:靶向递送 + 化学激活双重精准控制;
通用平台:能够精准调控酶活性、蛋白质互作、抗体功能等。
CAGE-Proxvivo的应用:
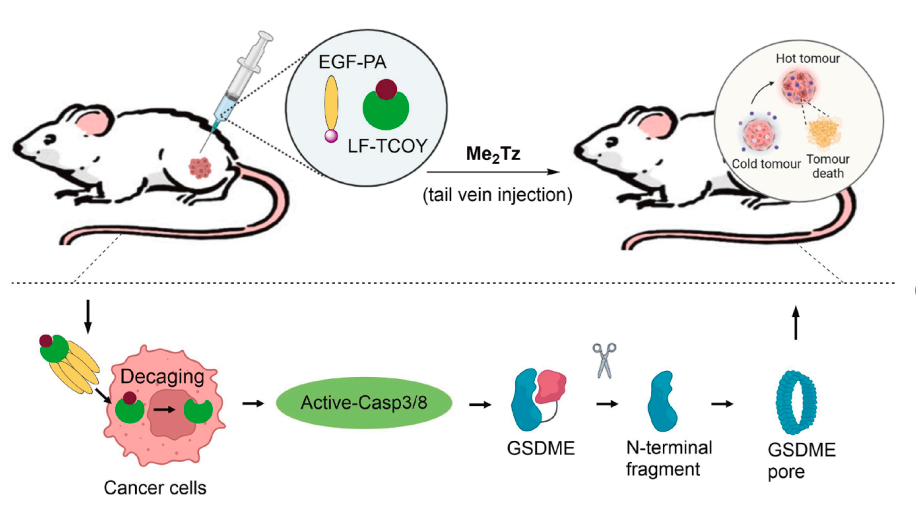
1、精准杀伤:炭疽致死因子(LF)可由其伴侣蛋白保护性抗原(PA)在细胞内递送,并通过切割细胞内的 MAPK 激酶级联反应诱导细胞凋亡,利用 PylRS 酶将 TCOY 引入LF活性位点,使其暂时失活,失活的 LF 通过肿瘤靶向的 EGF-PA 精准递送到高表达 EGFR 的肿瘤细胞内,注射小分子药物 Me2Tz 后,TCOY 发生生物正交剪切,恢复 LF 蛋白活性,进而诱导肿瘤细胞凋亡,实现对肿瘤细胞的定向杀伤。
利用CAGE-Proxvivo系统在活体小鼠中对炭疽致死因子(LF)进行化学激活,从而按需启动程序性细胞死亡。LF 可由其伴侣蛋白保护性抗原(PA)在细胞内递送,并通过切割细胞内的 MAPK 激酶级联反应诱导细胞凋亡,将 PA 与表皮生长因子(EGF)结合,实现对高表达 EGFR 的肿瘤细胞的靶向,进而通过注射 Me2Tz 激活 LF,实现对肿瘤细胞的定向杀伤。
2、定向激活肿瘤细胞焦亡:同理,重新激活 LF,触发 Caspase3/8 级联反应,切割 GSDME 诱导肿瘤细胞焦亡,联合 DNA 甲基化抑制剂,可恢复 GSDME 表达,可在更多肿瘤类型中诱导肿瘤细胞焦亡
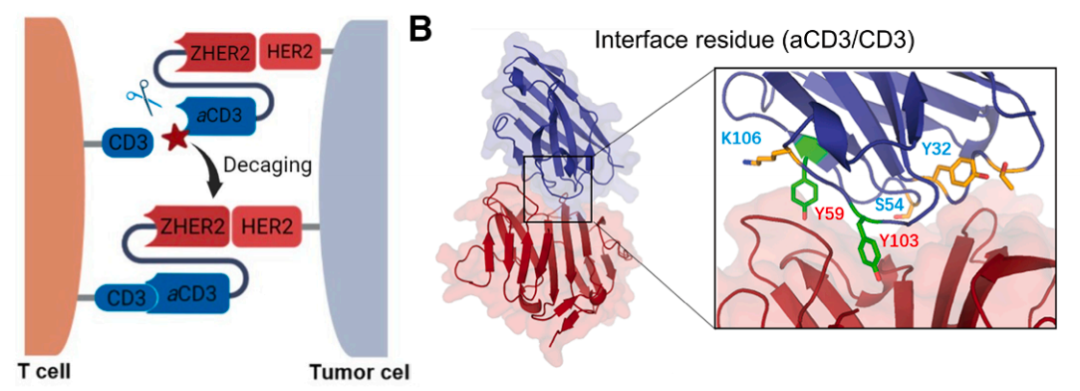
3、构建更安全的双特异性抗体:利用 PylRS 酶将 TCOY 引入抗 CD3 抗体(aCD3),进而构建双特异性抗体 ZHER2-aCD3,其只有在使用 Me2Tz 诱导生物正交剪切反应的情况下,才会恢复肿瘤部位的 T 细胞抗肿瘤功能,相比传统双抗,提高了肿瘤抑制率,并避免了细胞因子风暴及相关毒性,从而提高了双特异性抗体的安全性。
总的来说,该研究开发了一种名为CAGE-Proxvivo的计算机辅助邻近激活策略,用于在活体动物中按需激活蛋白质以及调控蛋白-蛋白相互作用,为在活体条件下的时间分辨生物学研究和按需治疗干预提供了一个通用平台。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 牙周炎伴牙龈萎缩:8款医用级修复解决方案权威推荐 (2025-10-23)
- 辽宁:2025年11月1日起全面完成生养津贴发放至团体 (2025-10-23)
- 放射科与分研院联合研究成果发表于Science子刊,为动脉粥样硬化诊疗开辟新路径 (2025-10-23)
- 用药更少、服用更不便:我国幽门螺杆菌根除医治研讨取得新突破 (2025-10-23)
- 醉酒后光止吐没用!GFX 护肝胶囊用实力护肝脏 (2025-10-23)
- Nat Biotechnol:给免疫细胞“写记忆”!科学家发明不伤DNA的基因开关,抗癌能力有望持久升级 (2025-10-23)
- 《神经病学年鉴》:评估一个简单的转身动作,或可提前8.8年预测帕金森病! (2025-10-23)
- 颠覆“一胖毁所有”!最新研究:带这种“肥胖基因”缺陷,胖却血脂低、心血管风险降,大脑才是幕后调度官 (2025-10-22)
- Nat Commun:癌细胞也有“作战指挥室”?科学家用纳米炸弹把它炸了! (2025-10-22)
- Cell:黑色素瘤细胞表面的凹陷是肿瘤杀伤热点 (2025-10-22)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















