罕见病新药!Apellis公司C3抑制剂pegcetacoplan头对头III期研究击败Alexion重磅C5抑制剂Soliris |
 |

2020年01月09日讯 /BIOON/ --Apellis制药公司致力于通过开创性的靶向C3方法开发首创和同类最佳疗法,用于治疗由补体级联反应的不受控或过度激活所驱动的广泛疾病,包括血液学、眼科学和肾脏学领域的疾病。近日,该公司公布了头对头III期PEGASUS研究(APL2-302,NCT03500549)的阳性结果(详见:)。
该研究是一项多中心、随机、开放标签、阳性药物对照、头对头研究,在80例阵发性夜间血红蛋白尿(PNH)成人患者中开展,评估了pegcetacoplan(APL-2)相对于Soliris(eculizumab)的疗效和安全性。Soliris是Alexion公司的一款重磅C5补体抑制剂,已被批准治疗PNH。该研究中,受试者必须一直在接受eculizumab治疗(稳定治疗至少3个月),并且在筛查访视时血红蛋白水平<10.5g/dL。再为期4周的导入期,患者接受每周2次1080mg剂量pegcetacoplan,同时接受其当前剂量的eculizumab治疗。在16周的随机对照期内,患者随机分配接受1080mg剂量pegcetacoplan(每周2次)或其当前剂量的eculizumab。所有完成随机对照期的受试者进入开放标签pegcetacoplan治疗期,接受pegcetacoplan治疗,而不考虑在随机对照期的治疗方案。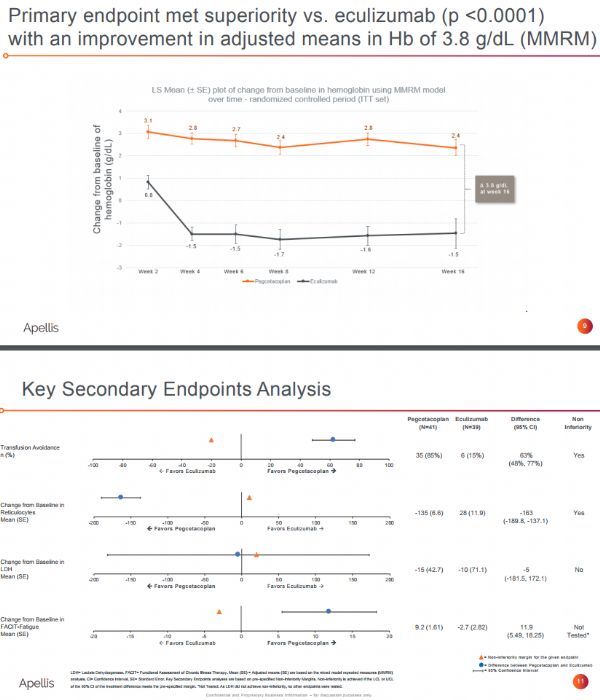
结果显示,该研究达到了主要疗效终点:pegcetacoplan与eculizumab相比在治疗第16周时血红蛋白校正平均值3.8g/L在统计学上有显著改善(p<0.0001)。在治疗第16周,pegcetacoplan治疗患者(n=41)校正后的平均血红蛋白水平相对基线8.7g/dL增加了2.4g/dL,eculizumab治疗患者(n=39)校正后的平均血红蛋白水平相对基线8.7g/dL的变化为-1.5g/dL。
pegcetacoplan在关键次要终点也显示出有希望的结果。pegcetacoplan在避免输血和绝对网织红细胞计数方面达到了非劣效性。在治疗第16周,pegcetacoplan治疗组有85%的患者无输血,eculizumab治疗组为15%。此外,pegcetacoplan在乳酸脱氢酶(LDH)和疲劳方面也呈现阳性结果。
该研究中,pegcetacoplan的安全性与eculizumab具有可比性,严重不良事件发生分别为17.1%和15.4%,2组均无脑膜炎比例和死亡报告。16周随机对照治疗期间,pegcetacoplan治疗组和eculizumab治疗组最常见的不良反应分别为:注射部位反应(36.6% vs 2.6%)、腹泻(22.0% vs 0%)、头痛(7.3% vs 20.5%)、疲劳(4.9% vs 15.4%)。另一个常见是溶血(9.8% vs 23.1%),导致pegcetacoplan治疗组3例停药。
所有在两组完成随机化治疗期的患者(77/80)已进入32周开放标签pegcetacoplan治疗期。该研究的详细结果将在未来召开的医学上公布。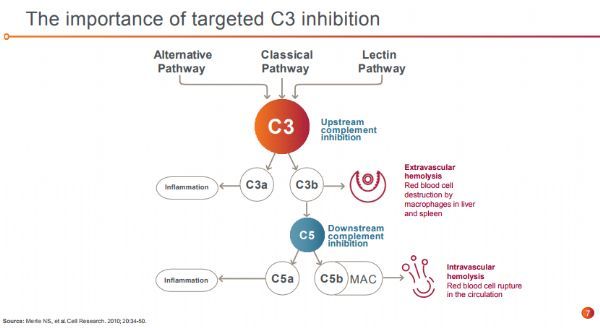
Apellis公司首席医疗官Federico Grossi博士表示:“pegcetacoplan是第一个也是唯一一个在血红蛋白水平上显示出优于eculizumab的研究性疗法。我们也很高兴看到85%接受pegcetacoplan治疗的患者没有输血。我们致力于开发突破性的治疗方法,这些结果表明,pegcetacoplan有潜力改变PNH患者的生活。我们期待着在今年上半年与监管机构会面,讨论下一步行动。”
PEGASUS研究调查员、利兹大学实验血液学教授Peter Hillmen博士表示:“目前接受eculizumab治疗的PNH患者中,大多数都患有持续性。PEGASUS研究的结果显示,pegcetacoplan有可能成为PNH患者的新护理标准。”
pegcetacoplan是一种研究性、靶向性C3抑制剂,旨在调节补体过度激活,这是导致许多严重疾病发生和发展的原因。pegcetacoplan是一种合成的环肽,与一种聚乙二醇聚合物结合,特异性地与C3和C3b结合。目前,pegcetacoplan正被开发用于治疗多种疾病,包括PNH、地图样萎缩(GA)和C3肾小球病。在美国,已授予pegcetacoplan治疗PNH和GA的快速通道资格。
Soliris是Alexion公司销售的一款药物,这是一种首创的补体抑制剂,通过抑制补体级联反应终端部分的C5蛋白发挥作用。补体级联反应是免疫系统的一部分,其不受控激活在多种严重的罕见病和超级罕见病中发挥了重要作用。Soliris于2007年首次获准上市,之前已获批4种超级罕见病:PNH、非典型溶血尿毒症综合征(aHUS)、抗AchR抗体阳性全身性重症肌无力(gMG)、抗水通道蛋白-4(AQP4)抗体阳性的视神经脊髓炎谱系障碍(NMOSD)。
医药网新闻
- 相关报道
-
- 两篇《科学》齐发!食物过敏的背后机制找到了 (2025-08-13)
- 抑郁症治疗新方法:陈跃军/熊曼团队利用人类干细胞来源的A10亚型多巴胺能神经元改善抑郁症 (2025-08-13)
- Science:既是“脚手架”也是“束缚衣”——神经元为何必须动态重塑其周期性骨架 (2025-08-13)
- Cell Death and Disease:类器官模型揭示 ULBP2 CAR-T 细胞对胃癌的杀伤作用 (2025-08-12)
- Cell子刊:华人团队开发新型微针贴片,促进心肌梗塞后的心脏修复 (2025-08-12)
- 颜宁团队发表最新PNAS论文:助力心脏病及抗癫痫/镇痛药物精准设计 (2025-08-12)
- STTT:湖北工业大学团队发现“癌王”进展新机制和治疗新靶点! (2025-08-12)
- Nature Neuroscience:宋洪军/明国莉/周毅团队揭示人类海马新生未成熟神经元的独特演化规律 (2025-08-12)
- 第十一届马凡病友大会:以爱为翼,让健康与希望接力传递 (2025-08-11)
- Nature子刊:邹强/崔心刚/倪志宇/高强团队发现,饮食来源的半乳糖具有抗癌作用 (2025-08-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















