光合蓝藻长链脂肪烃合成的结构基础研究获进展 |
 |
随着地球上化石燃料日趋枯竭,寻求更安全、环保、经济的替代燃料成为社会发展的必须。长链脂肪烃作为传统液体燃料汽油的主要成分,对其生物合成途径进行改造和优化是极有前景的替代产油方案。早期的研究发现光合生物蓝藻中存在一条代谢途径,可以直接利用光能合成长链脂肪烃,无需额外碳源,但是效率较低,对该途径进行改造,获得能够高效产烃的蓝藻,是开发清洁生物能源的一条可行途径。
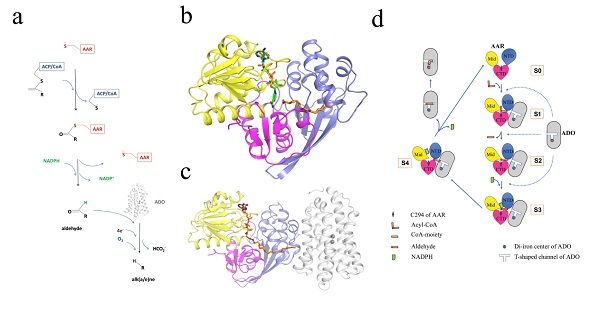
蓝藻中长链脂肪烃合成途径包括两步酶促反应(图a),分别由酰基蛋白还原酶(AAR,acyl-acyl carrier protein reductase)和脂肪醛脱甲酰加氧酶(ADO, aldehyde deformylating oxygenase)催化。其中AAR催化第一步反应,以携带酰基脂肪链的ACP(acyl carrier protein)蛋白或辅酶A(CoA)为底物,将之还原为长链脂肪醛,随后ADO以AAR的产物脂肪醛为底物,催化其生成为少一个碳的脂肪烃。研究表明,这两个酶单独都可完成各自的催化反应,但是之前的研究结果不能解释疏水的脂肪醛分子是如何在亲水环境中在两个水溶蛋白之间进行传递的;最近,有研究表明AAR和ADO可以形成复合物,且复合物的形成有利于催化反应的进行,但复合物的结构和对该途径的具体意义尚不清楚。
中国科学院生物物理研究所李梅/常文瑞课题组2015年解析了蓝藻ADO的晶体结构,继续对该途径进行深入研究,此次报道了蓝藻Synechococcus elongatus PCC 7942来源的AAR的晶体结构,以及AAR结合ADO及不同底物(类似物)、辅因子的三个复合物的晶体结构(图b,c)。通过结构分析和比较,结合相关的生化实验,研究人员揭示了蓝藻AAR结合底物和辅因子的结构细节,阐明了其采取“乒乓机制”在同一位点结合底物和辅因子的结构基础,揭示了AAR-ADO复合物的相互作用方式和关键氨基酸,并发现AAR-ADO复合物中形成了一个贯穿两个蛋白的疏水通道,解释了以前研究中一直困惑的脂肪醛分子是如何在两个蛋白之间进行传递的问题。基于该项最新工作,并结合课题组前期的研究结果(Pro Cell, 2015),研究人员首次从结构生物学角度揭示了蓝藻脂肪烃生物合成途径的催化过程和调控机理(图d),为继续改造优化该途径提供了重要基础。(100yiyao.com)
医药网新闻
- 相关报道
-
- 极限赛事的 "隐形铠甲":北京和睦家多学科协同为1.5万名斯巴达勇士护航 (2025-08-14)
- 《自然·神经科学》:重启病变运动神经元!哥大学者发现,再表达ISL1和LHX3,可以减轻渐冻症表型 (2025-08-14)
- Cell子刊:我国学者研究证实,微塑料/纳米塑料已全面侵入珠峰生态系统的各个部分 (2025-08-14)
- 首届中国-东盟药膳博览会新闻发布会在京隆重召开 (2025-08-13)
- 师恩入海,核美丽助您社交无痕 (2025-08-13)
- 申报:脑机接口技术向理论利用畛域迈进的过程显著提速 (2025-08-13)
- 解读:通过初步模式审查的药品及相关信息的布告 (2025-08-13)
- 房静远团队发现盐酸小檗碱(黄连素) 具有较长期预防结直肠腺瘤切除后复发的作用 (2025-08-13)
- 十大护肝片品牌排行,护肝片哪个牌子效果最好?人群、成分、技术都有哪些? (2025-08-13)
- 你爱用AI看病吗?最新”荒诞“案例:因听从ChatGPT建议,一男子溴中毒,差点闹出人命 (2025-08-13)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















