一批新药将上市:恒瑞、东阳光、正年夜晴和... |
 |
医药网7月20日讯 多款新药上市有新停顿,国际里头部药企均有斩获
23款新药上市有停顿!2款国产1类新药初次获批
6月26日-7月16日时代,23个新药(33个受理号)的上市申请有审评审批状态更新。9款国产新药获批上市,此中2款1类新药初次获批,包含艾迪药业的艾诺韦林片(曾用名ACC007片)、海正药业的海泽麦布片;3个新药获批出口,安进的打针用卡非佐米、萌蒂的盐酸羟考酮缓释片初次获批。
此外,神州细胞的打针用重组人凝血因子(Ⅷ)、北京博康健的打针用重组人特立帕肽、礼来的打针用盐酸吉西他滨、赛诺菲的碳酸司维拉姆片、阿斯利康的奥拉帕利片等7个药品的注册操持状态变革为“在审批”。
(6.26-7.16)新药上市申请审评审批状态更新
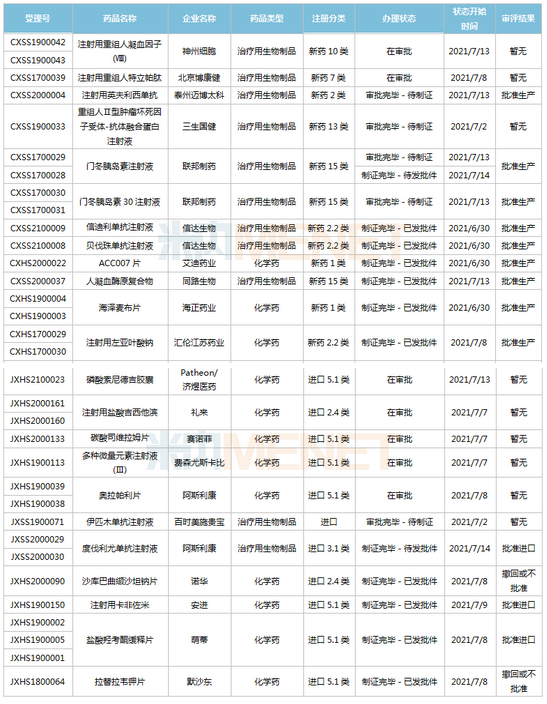
2款国产1类新药初次获批上市。海博麦布片是海正药业首个获批上市的1类新药,这是一款胆固醇排汇克制剂,用于医治原发性高胆固醇血症。同靶点上市药物为默沙东的依折麦布,环球贩卖峰值达26.6亿美元,2020年在中国城市公立病院、县级公立病院、城市社区中间以及州里卫生院(简称中国公立医疗机构)及中国城市实体药店终端共计贩卖额接近10亿元;艾诺韦林片(曾用名ACC007片)是全新构造的非核苷类逆转录酶克制剂,是艾迪药业首个获批的抗艾滋病1类新药。
联邦制药2款胰岛素获批上市,均为国产第2家。门冬胰岛素打针液是一种速效的人胰岛素相似物,门冬胰岛素30打针液是由可溶性门冬胰岛素和精卵白门冬胰岛素按30:70的比例构成的预混胰岛素。米内网数据显示,2020年中国公立医疗机构及中国城市实体药店终端胰岛素及其相似药贩卖规模超过300亿元。
初次在国际获批的打针用卡非佐米是百济神州/安进结合开辟的一款卵白酶体克制剂,结合地塞米松医治复发或难治性多发性骨髓瘤。该产物于2012年在环球初次获批,2020年环球贩卖额超过10亿美元。
英夫利西单抗是强生/默沙东研发的一款特同性阻断肿瘤坏死因子(TNF-α)的人鼠嵌合型单克隆抗体,环球贩卖峰值达92.4亿美元,尽管遭到生物相似药冲击,但2020年仍完成40.77亿美元的贩卖额。泰州迈博太科药业的打针用英夫利西单抗是国际首款获批上市的英夫利西单抗生物相似药,使用CHO表白体系,比原研产物更平安且免疫原性更低。
21款新药申请上市!正年夜晴和、人福......4款1类新药来袭
6月26日-7月16日时代,21个新药(28个受理号)上市申请得到CDE承办。12款为国产新药,此中4款为1类新药,包含正年夜晴和康方的派安普利单抗打针液、银珠医药/长城制药的羧胺三唑软胶囊、光谷人福的广金钱草总黄酮胶囊及乐普生物/鼎康生物的普特利单抗打针液;10款为出口新药,赛生医药的那昔妥单抗打针液、梯瓦医药的醋酸格拉替雷打针液、信达的Pemigatinib片、武田的Mobocertinib胶囊、康哲药业的地西泮鼻喷雾剂、协和麒麟的莫格利珠单抗打针液为初次报产。
(6.26-7.16)获承办的国产/出口新药上市申请
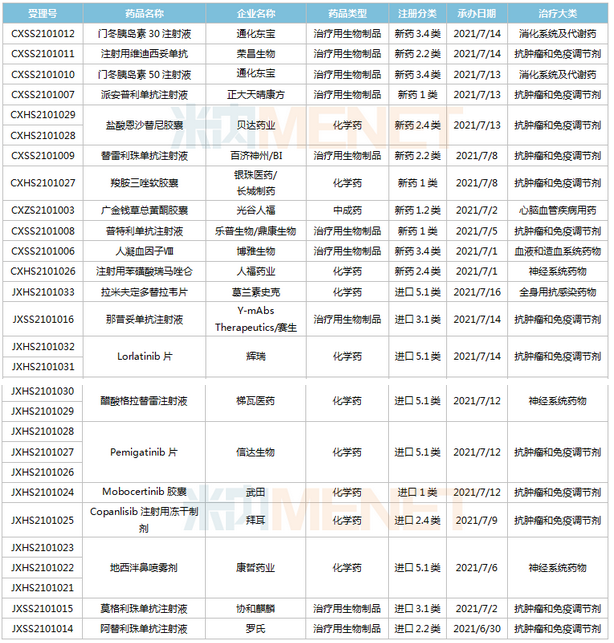
2款PD-1单抗报告上市。乐普生物的普特利单抗打针液属于差别化设计的PD-1抗体,在IgG4的Fc引入S254T/V308P/N434A渐变缩短半衰期;正年夜晴和康方的派安普利单抗打针液具备同类最佳的后劲,与国外已上市PD-1相比抗原联合解离速度较慢。今朝国际已有6款PD-1单抗获批上市,别离为帕博利珠单抗、纳武利尤单抗、信迪利单抗、特瑞普利单抗、卡瑞利珠单抗及替雷利珠单抗。此外,还有5款PD-1的上市申请还在审,包含普特利单抗、派安普利单抗、杰洛利单抗、赛帕利单抗以及斯鲁利单抗。
通化东宝2款预混型门冬胰岛素报告上市。门冬胰岛素50打针液仅原研厂家诺和诺德的产物在售,通化东宝首家报产;甘李药业、联邦制药的门冬胰岛素30打针液已获批,东阳光药、通化东宝的产物已报产。米内网数据显示,2020年中国公立医疗机构及中国城市实体药店终端门冬胰岛素贩卖规模超过80亿元。
pemigatinib片是信达生物引进的一款成纤维细胞成长因子受体(FGFR)1/2/3克制剂,用于有FGFR2交融或重排的早期、转移性或不行手术切除的胆管癌。该产物已于2021年6月21日在台湾获批上市,是信达生物获批的首款小分子新药,也是公司第五款获批上市的立异药。
Mobocertinib(TAK-788)是武田研发的一种新型、高选择性的“first-in-class”口服酪氨酸激酶克制剂(TKI),拟用于医治携带表皮成长因子受体(EGFR)20号外显子拔出渐变的非小细胞肺癌,今朝环球范畴内暂未获批,这次在中国申请上市初次完成了中国与环球的同步递交。
协和麒麟的莫格利珠单抗打针液(Mogamulizumab)属于抗CC趋化因子受体4(CCR4)单克隆抗体,2012年初次在日本获批,2018年得到FDA同意上市。Mogamulizumab无望成为国际首款“first-in-class”的CCR4克制剂,为复发性或难治性皮肤T细胞淋巴瘤患者提供新的医治选择。
康哲药业引进的地西泮鼻喷雾剂联合了基于维生素E的溶剂和Intravail排汇加强剂的共同组合,以期在鼻腔配方中得到突出的排汇性、耐受性和靠得住性。这是国际首款报产的地西泮鼻喷雾剂,用于医治六岁及以上癫痫患者的间歇性、刻板性癫痫频仍发生发火运动。米内网数据显示,2020年中国公立医疗机构终端地西泮贩卖规模超过7000万元。
那昔妥单抗打针液是赛生医药引进的一款神经节苷脂GD2人源化单克隆抗体,通过靶向高表白于神经母细胞瘤的GD2起效。该产物于2020年11月25日初次得到FDA减速同意上市,用于医治复发/难治性高危神经母细胞瘤。今朝环球有3款靶向GD2医治神经母细胞瘤的单抗产物获批,国际市场临时空缺。
梯瓦的醋酸格拉替雷打针液是由谷氨酸、丙氨酸、酪氨酸和赖氨酸四种氨基酸构成一种合成肽类化合物,被以为是通过改动形成多发性软化(MS)发病机制的免疫进程而起作用的,可下降复发性MS患者的复发频率。该产物2020年环球贩卖额为13.37亿美元,可见临床需求之年夜。
多款新药新顺应症报产,包含百济神州的PD-1替雷利珠单抗(局部早期或转移性食管鳞状细胞癌)、荣昌生物的ADC药物维迪西妥单抗(局部早期或转移性尿路上皮癌)、贝达的恩沙替尼(ALK阳性非小细胞肺癌)等。
科伦、东阳光药、恒瑞......69个新药获批临床,国产新药高歌大进
6月26日-7月16日时代,69个新药(波及96个受理号)得到临床实验默示允许。此中,51个种类(70个受理号)为国产新药(42个1类新药),18个种类(26个受理号)为出口新药。从药品类型看,化学药有37个、医治用生物成品有32个。
(6.26-7.16)获批临床的国产/出口新药
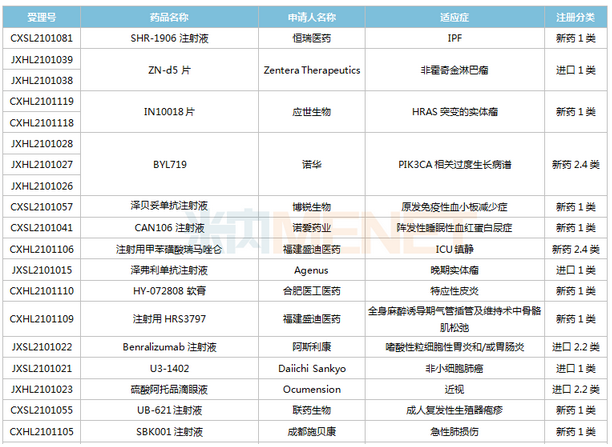
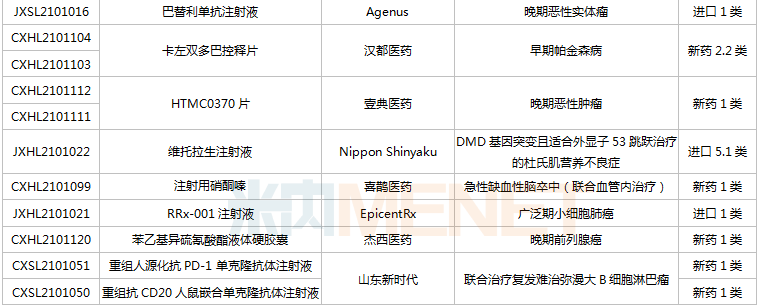
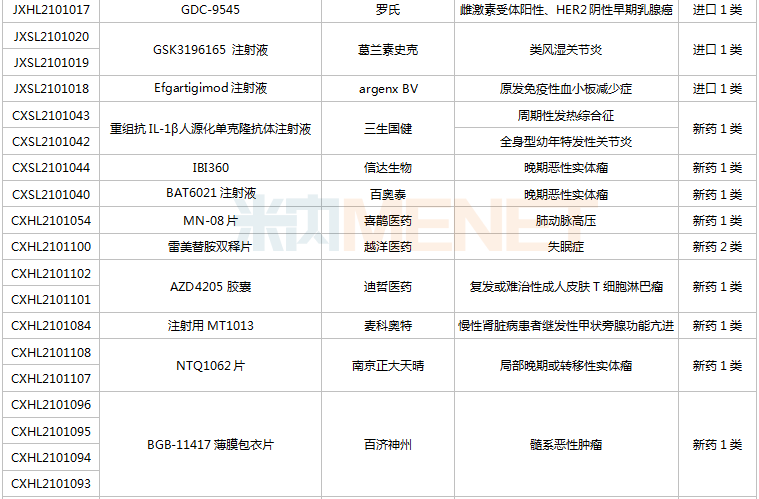
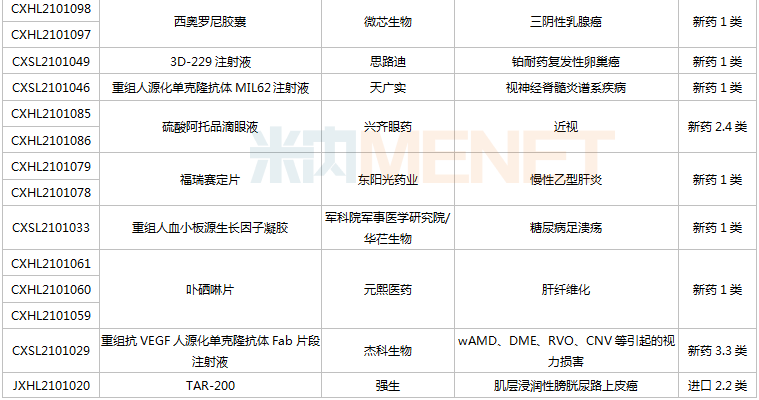
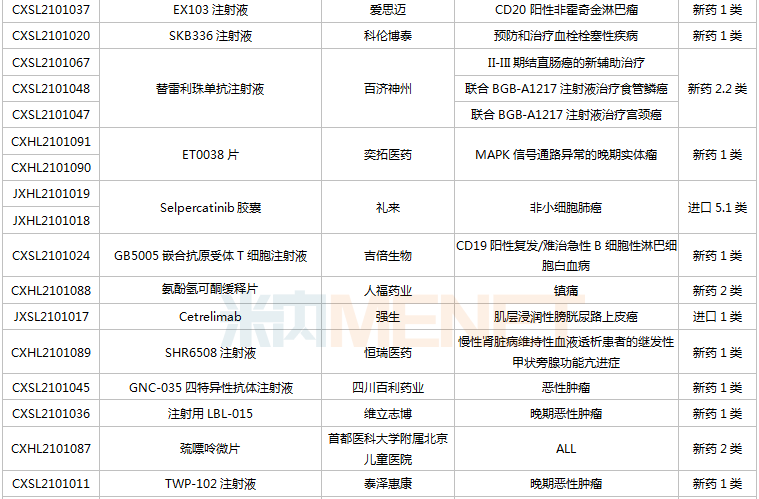
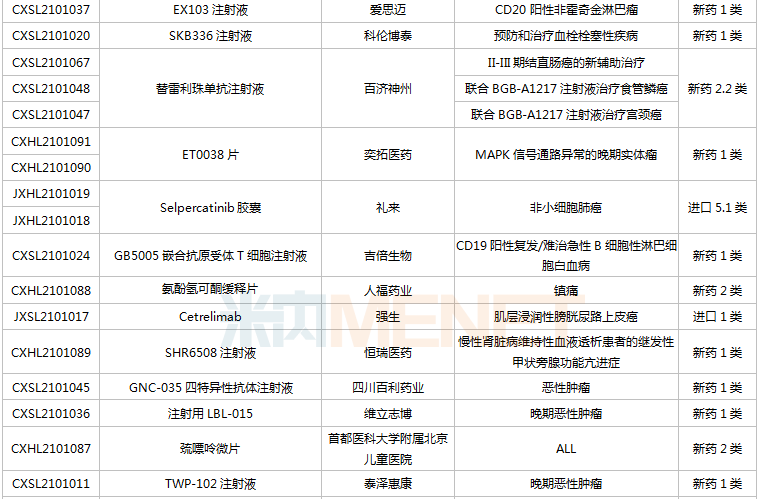
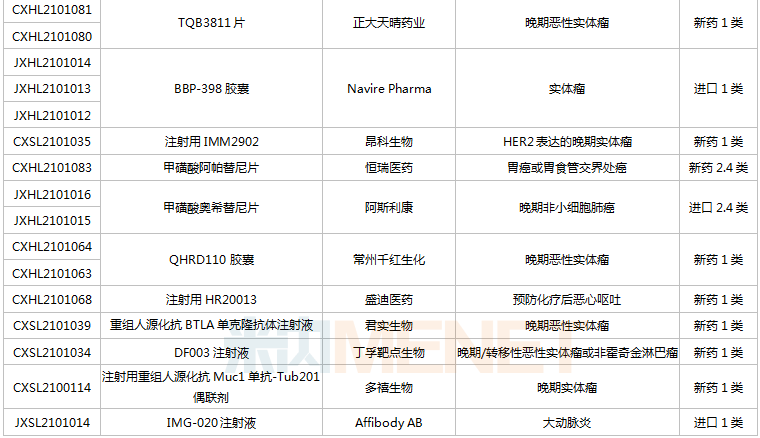
恒瑞医药有6款新药获批临床,包含SHR-1906打针液、打针用甲苯磺酸瑞马唑仑、打针用HRS3797、SHR6508打针液、甲磺酸阿帕替尼片、打针用HR20013。除了甲磺酸阿帕替尼片、打针用甲苯磺酸瑞马唑仑,别的4款1类新药均为初次获批临床。SHR6508打针液拟用于医治慢性肾脏病维持性血液透析患者的继发性甲状旁腺功效亢进,今朝国际尚无同类静脉给药产物上市;打针用HR20013用于预防化疗后恶心吐逆,今朝国际外尚未有同类产物获批上市。
中国生物制药2款1类新药获批临床。南京正年夜晴和NTQ1062片、正年夜晴和的TQB3811片为初次获批临床,均拟用于医治实体瘤,作用靶点暂无具体信息。
科伦药业子公司博泰生物开辟的1类新药SKB336打针液是一款全新的具备自立常识产权的靶向FXIa/FXI因子的人源化单抗,今朝环球尚无同靶点药物获批上市,在研药物包含拜耳的BAY-1213790、诺华的abelacimab(阿贝西单抗),两个产物均处于II期临床。米内网数据显示,2021年至今,科伦药业已有7款新药获批临床(不含弥补申请),此中5款为1类新药。
百奥泰的1类新药BAT6021打针液初次获批临床,这是一款经无岩藻糖基化修饰的mAb候选药物,作用靶点为TIGIT,拟用于医治早期恶性实体瘤。今朝国际暂无同靶点药物获批,在研药物包含百济神州的Ociperlimab(III期临床)、信达的IBI939(I期临床)、君实的JS006(I期临床)等。
豪森、石药、齐鲁……114个新药临床申请获承办
6月26日-7月16日时代,114个新药(波及164个受理号)的临床申请获CDE承办受理。此中,86个种类(113个受理号)为国产新药,28个种类(51个受理号)为出口新药。从药物类型看,化学药有56个、医治用生物成品有52个、中成药有6个。86个国产新药中,1类新药有63个。
(6.26-7.16)获承办的国产/出口新药临床申请
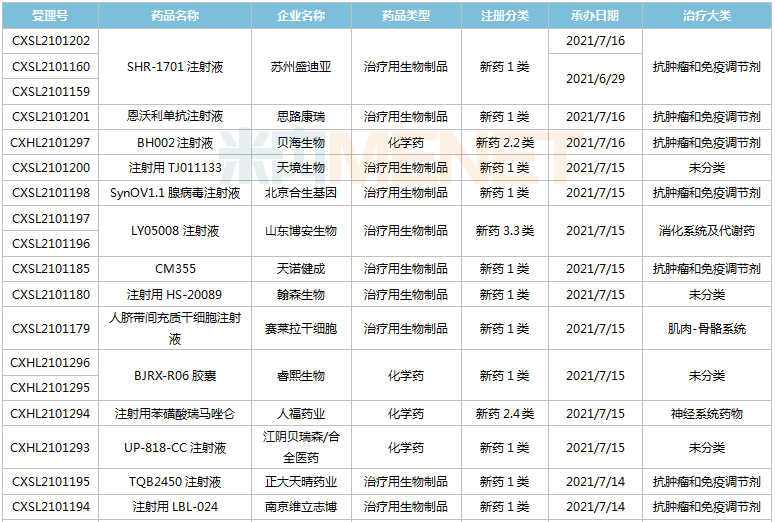
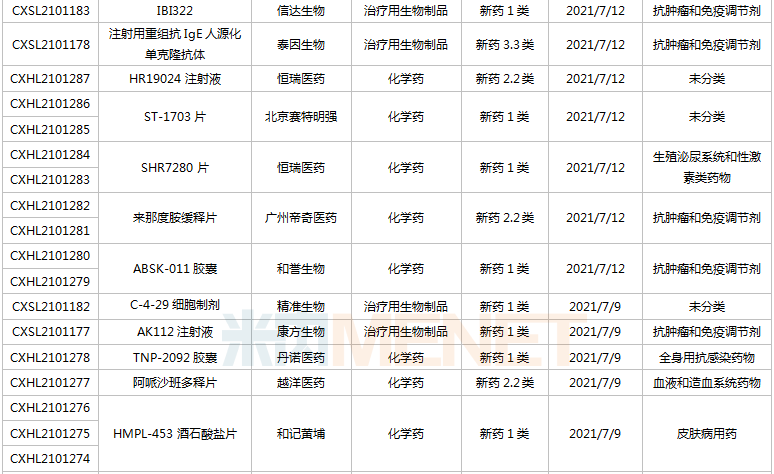
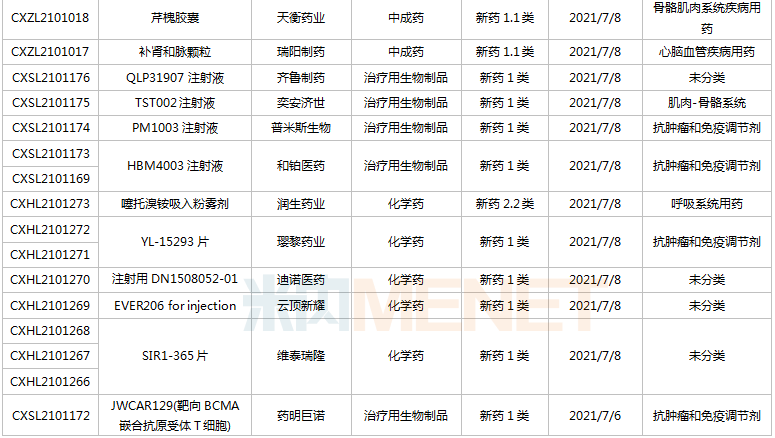
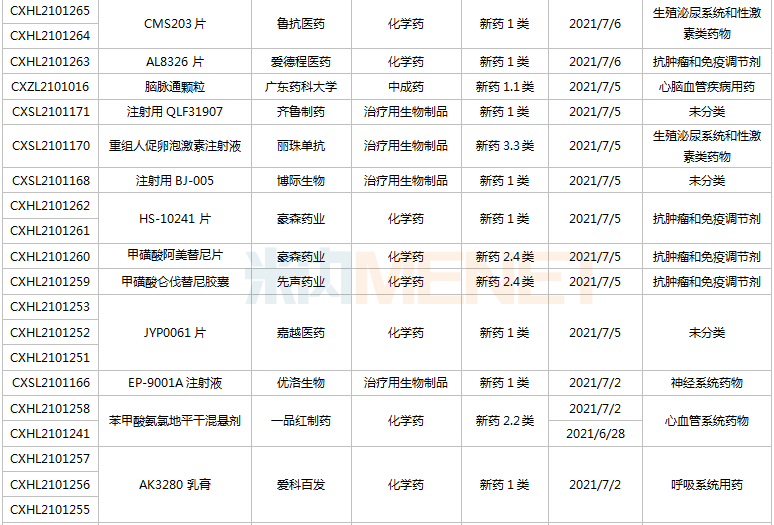
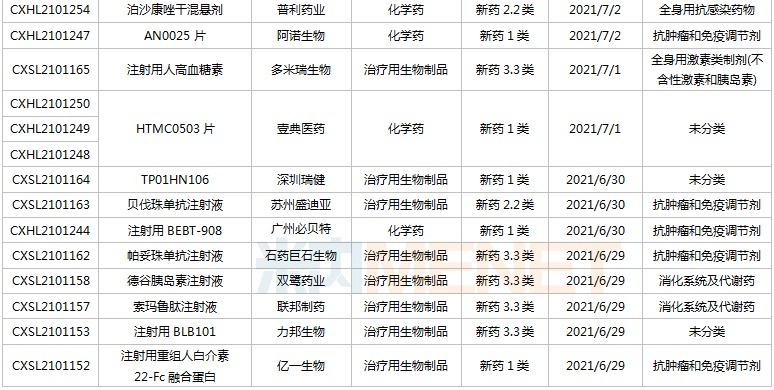
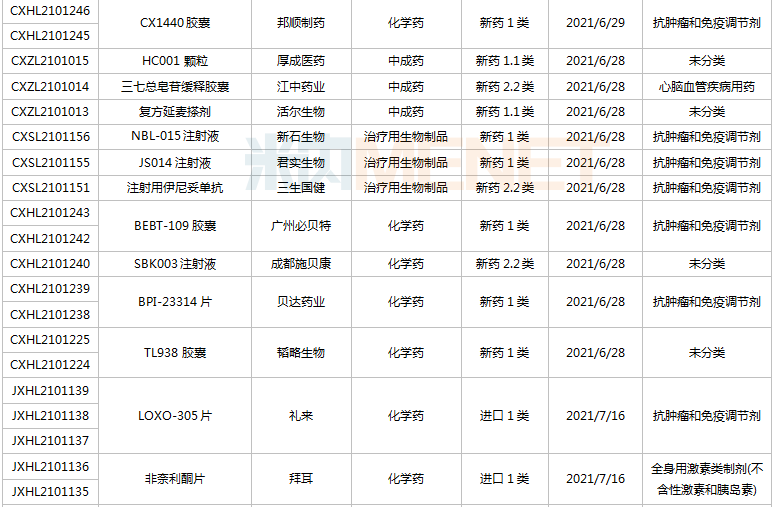
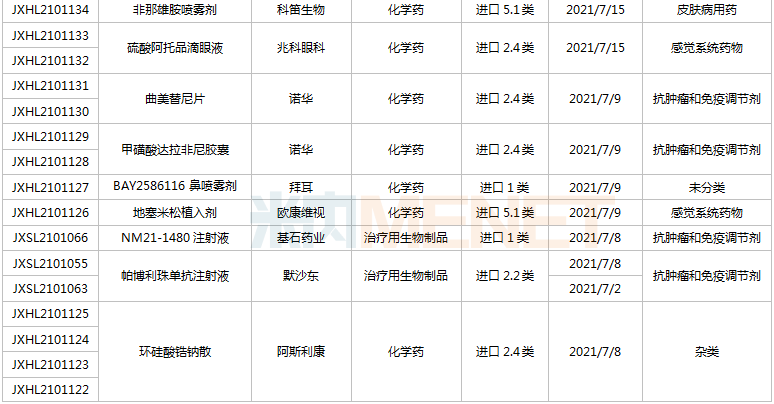
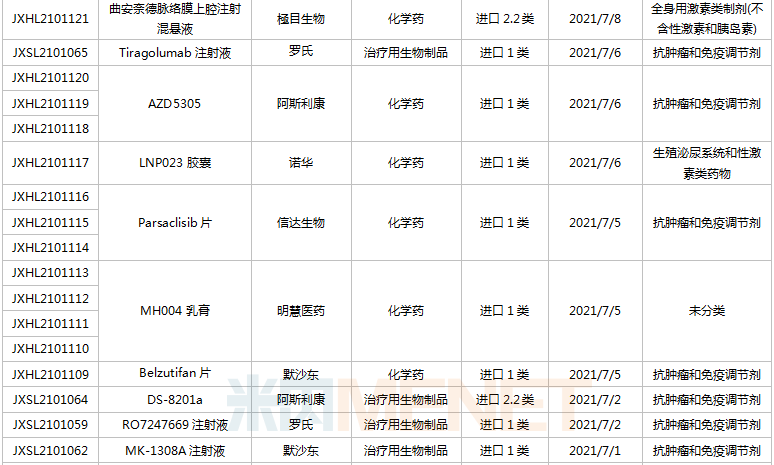
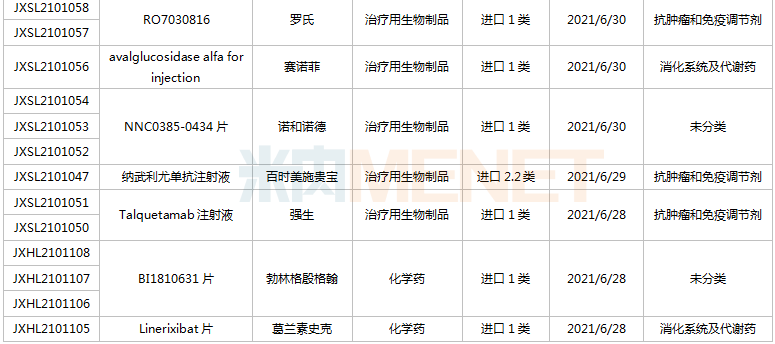
豪森药业有4款新药申请临床,包含HS-10241片、甲磺酸阿美替尼片、打针用HS-20089及打针用HS-20093,此中打针用HS-20089、打针用HS-20093为初次报告,两款新药均为医治用生物成品。
基石药业初次报告临床的NM21-1480打针液(原代号ND021)是一款针对三个靶点的多特同性抗体,可以同时联合PD-L1与4-1BB,而且还可以联合人血明净卵白(HSA),ND021共同的单价构造使其在平安窗和抗癌谱方面具有很年夜的劣势。
君实的JS014打针液属于重组白介素21-抗人血明净卵白(HSA)单域抗体交融卵白,通过交融抗HSA的单域抗体使IL-21的半衰期获得显著缩短,是国际首款报告临床的IL-21交融卵白。
阿斯利康初次报告临床的AZD5305属于第二代PARP克制剂,对PARP1具备高度选择性,同时照样高效的PARP1-DNA捕捉器,解决了第一代PARP克制剂与化疗药物结合使用时的毒反作用。
诺和诺德的NNC0385-0434片是国际第3款报告临床的口服PCSK9克制剂,另外2款为西威埃医药的CVI-LM001和中科院上海药物研讨所的DC371739。今朝国际2款PCSK9克制剂获批上市,均为打针剂,别离是赛诺菲的阿利西尤单抗和安进的伊洛尤单抗,暂无口服PCSK9克制剂获批。
数据起源:米内网数据库、CDE、公司布告。数据统计光阴段为6月26日-7月16日,按药品称号统计(不含预防用生物成品、体外诊断试剂等,不含弥补申请),若有疏漏,欢送指正!
注:米内网中国城市实体药店终端竞争格式数据库是笼罩全国293个地市及以上城市实体药店(不含县农村实体药店),对全品类进行间断监测的缩小版城市实体药店数据库。上述贩卖额以产物在终真个均匀批发价盘算。
医药网新闻
- 相关报道
-
- 颠覆“一胖毁所有”!最新研究:带这种“肥胖基因”缺陷,胖却血脂低、心血管风险降,大脑才是幕后调度官 (2025-10-22)
- Nat Commun:癌细胞也有“作战指挥室”?科学家用纳米炸弹把它炸了! (2025-10-22)
- Cell:黑色素瘤细胞表面的凹陷是肿瘤杀伤热点 (2025-10-22)
- 致敬世界传统医药日,扬子江药业“上新”非遗工艺“中药之冠” (2025-10-22)
- Cell:“细胞风暴”过境,熄灭中枢神经的“燎原之火”——CAR-T疗法为进展性多发性硬化带来新曙光 (2025-10-22)
- Nature Biotechnology:微缩战场!在毫米级芯片上,我们能否洞悉CAR-T细胞与实体瘤的生死对决? (2025-10-22)
- 《自然》:哺乳还有这种好处!科学家发现,生育和哺乳会促进CD8阳性T细胞在乳腺中的积累,可降低乳腺癌风险,尤其是三阴性乳腺癌 (2025-10-22)
- 槲皮素哪个牌子好?2025年十大槲皮素品牌深度解析:肺结节选购指南 (2025-10-22)
- 从结构性洗牌中突围:顾连医疗的十年,与一场康复行业的分化赛跑 (2025-10-22)
- 循证为基,人文为怀:苏州明基医院代谢与减重中心的高质量发展之道 (2025-10-22)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















