【已完成 请管理员审核】细胞:在细菌中发现新的免疫防御机制!它有望成为基因编辑和核酸检测的新工具 |
 |
来源:100医疗网原创2022-04-06 22336008
像人类一样,细菌也有多重免疫系统来抵御病毒等病原体。这些免疫系统通常会降解病原体的DNA,使其无害。在一项新的研究中,荷兰瓦赫宁大学和代尔夫特理工大学的研究人员发现了一种新的用途和一种不同的细菌。
像人类一样,细菌也有多个系统来抵御病毒等病原体。这些免疫系统通常会降解病原体的DNA,使其无害。在一项新的研究中,来自荷兰瓦赫宁大学和代尔夫特理工大学的研究人员发现了一种新的方法,通过在细菌中使用不同的机制来中和入侵者的免疫系统。相关研究成果于2022年4月4日在线发表在《细胞杂志》(Cell Journal)上,标题为短原核氩Aute系统在检测到入侵DNA时触发细胞死亡。这篇论文的作者是瓦赫宁大学生物化学实验室的助理教授金奎大斯沃茨。
在我们的身体深处,一场持续的军备竞赛正在进行。一方面,病毒在不断寻找新的途径来渗透我们的细胞;另一方面,我们的身体也在不断思考更好的防御机制来消灭这些病毒。疾病和健康通常就是这样平衡的。而它的病原入侵者——细菌病毒(即噬菌体)和质粒——也在进行同样的军备竞赛。
在这项新的研究中,Swarts研究小组描述了这场军备竞赛中的一种新的防御机制。他们证实,一种新的细菌Argonaute蛋白在检测到入侵的DNA后,故意分解了所有被称为烟酰胺腺嘌呤二核苷酸(NAD)的分子。
彻底关闭手机。
Argonaute蛋白存在于植物和人类等真核生物中,但也存在于细菌等原核生物中。这些Argonaute蛋白由单链引导RNA(gRNA)或引导DNA(gDNA)重新编程,以寻找具有互补序列的侵入RNA或DNA。在大多数情况下,入侵的RNA或DNA会被切割成更小的无害片段,从而被破坏。这使得真核Argonaute蛋白能够介导RNA干扰,而更长的原核Argonaute蛋白可以干扰入侵的核酸。然而,在自然界的进化树中存在不同的短原核生物Argonaute蛋白,其功能和机制仍知之甚少。
在这项新的研究中,这些作者发现短原核生物Argonaute及其相关的TIR-APAZ蛋白形成了斯巴达异二聚体复合物。虽然这项新研究中的斯巴达也使用gRNA,但它通过一种根本不同的方法进行防御:在检测到入侵的DNA后,它通过分解NAD完全关闭入侵的细胞。
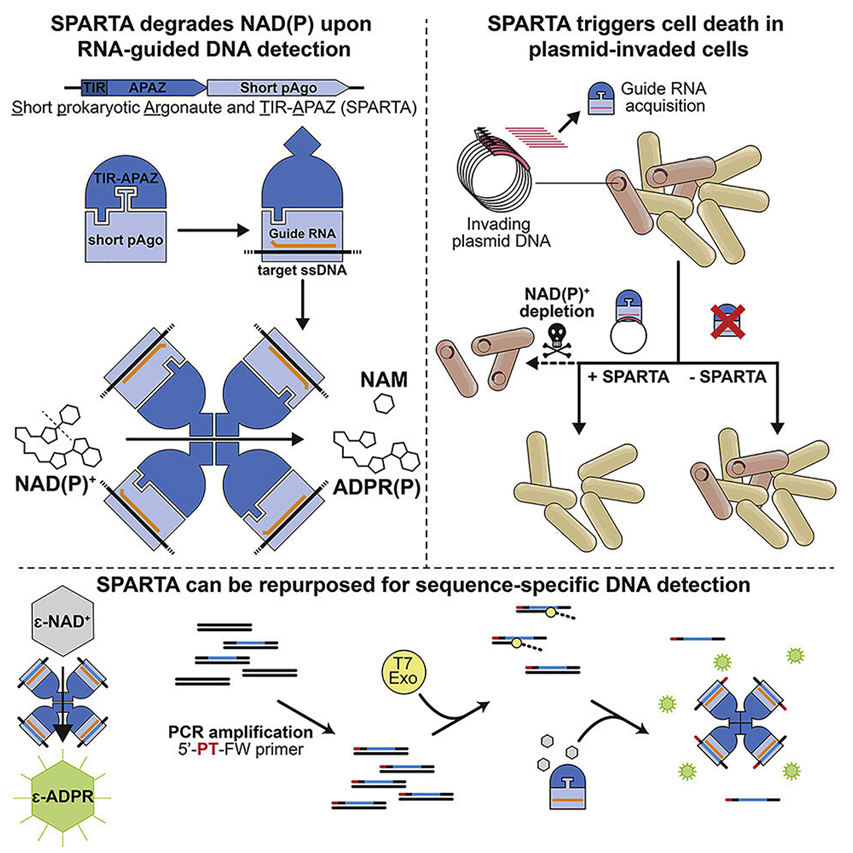
图片来自cell,2022,doi :10.1016/j . cell . 2022 . 03 . 012
一旦gRNA介导的靶DNA结合,四个斯巴达异二聚体形成寡聚体。在该寡聚体中,释放了由TIR结构域介导的NAD(P)酶活性。当在大肠杆菌中表达时,斯巴达在高转录多拷贝质粒DNA的存在下被激活,这导致通过NAD(P)耗竭而被质粒侵入的细菌细胞死亡。这导致从细菌培养物中除去质粒侵入的细菌细胞。此外,这些作者发现斯巴达被重新用于DNA序列的可编程检测。
你的研究证实了斯巴达是一个原核免疫系统,它在gRNA的指导下检测到入侵的DNA后,降低了入侵细胞的生存能力。
被侵入的细胞死亡。
NAD分子在细胞代谢中起着关键作用,让众所周知的引擎保持运转,使细胞得以继续存在。斯沃茨解释说,如果没有NAD,细胞最终会死亡。这听起来可能有些矛盾,但这正是将要发生的事情。通过让入侵的细胞死亡,入侵者就不能增殖或扩散到邻近的细菌。入侵的细菌细胞被牺牲以拯救其他健康细胞。
高级细菌
这种免疫系统存在于不同种类的细菌中。对于这些单细胞生物具有如此复杂的防御机制,Swarts并不感到惊讶。他说,人们经常低估细菌的能力。不管细菌有多小,它们的免疫系统已经进化了数百万年,变得越来越先进。他们必须这么做,因为病毒通常非常复杂。在未来,我们也许可以利用这种基因工具来检测人体内的疾病。
Swarts团队进行这项研究主要是因为对了解Argonaute蛋白质机制的科学愿望。然而,斯沃茨认为,从长远来看,这些新的见解也将有实际应用。例如,他们证明了这种细菌免疫系统可以被分离出来,然后用选定的gRNA重新编程。因为NAD降解很容易被检测到,所以这种细菌Argonaute蛋白可以根据指令识别特定的DNA序列。斯沃茨预计,在未来,我们可能能够使用这种基因工具来检测人类的疾病。但我们还没到那一步。目前,我们被一种基本的好奇心所驱使。(100yiyao.com)
参考资料:
1.巴尔维纳库帕尔等人。细胞,2022,doi :10.1016/j . cell . 2022 . 03 . 012
2.在细菌中发现新的免疫系统
https://phys.org/news/2022-04-immune-bacteria.html
版权声明
本网站所有标注“来源:100医学网”或“来源:bioon”的文字、图片及音视频资料,版权归100医学网网站所有。未经授权,任何媒体、网站、个人不得转载,否则将追究法律责任。获得书面授权转载时,必须注明“来源:100医学网”。其他来源的文章均为转载文章。本网站所有转载文章都是为了传递更多信息。转载内容不代表本站立场。不想被转载的媒体或个人可以联系我们,我们会立即删除。
87%的用户都在使用100医疗网APP随时阅读、评论、分享、交流。请扫描二维码下载-


- 相关报道
-
- 《柳叶刀》子刊:日行七千步,有八大好处!迄今最大规模/最全面研究发现,日行七千步与八种健康风险最高降低47%相关 (2025-08-05)
- 胆固醇研究新进展:上海交大/南昌医学院联合团队揭示食管鳞癌耐药新机制 (2025-08-05)
- Biosensors:新型蓝牙智能生物传感器,唾液检测乳腺癌新突破! (2025-08-05)
- STTT:清华大学董家鸿院士团队发现肝癌治疗新靶点,逆转肝癌耐药性 (2025-08-05)
- 卓悦榜丨德达医疗荣膺"年度健康服务与智慧医疗最佳企业"奖项 (2025-08-05)
- 《自然》:流感唤醒休眠癌细胞!科学家发现,呼吸道病毒感染引发的炎症和IL-6会诱导休眠散播性癌细胞表型转变,诱发乳腺癌肺转移 (2025-08-05)
- 睡眠质量不好?可以试试高钾晚餐!研究发现:晚餐钾摄入与失眠程度显著相关!其利于稳定血压、改善神经-肌肉信号及神经递质平衡 (2025-08-05)
- 黄荷凤院士团队揭示不粘锅涂层微塑料影响男性生育能力的机制,并开发出治疗方法 (2025-08-05)
- 特朗普向 17 家制药巨头发函,强制实施最惠国药价 (2025-08-05)
- 两篇Science论文:冬眠的“超能力”被锁在人类DNA中,解除锁定有望逆转阿尔茨海默病、糖尿病等疾病 (2025-08-04)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















