细胞:硬皮病病因学取得重大进展!表达LGR5的成纤维细胞亚群在疾病早期急剧下降 |
 |
来源:100医疗网原创2022-04-09 06336042
在一项新的研究中,来自魏茨曼科学研究所和其他研究机构的研究人员发现,长期被忽视的称为成纤维细胞的辅助细胞实际上是极其多样和重要的。这些细胞的子集可能是硬皮病的起源。
有时候配角会抢尽风头。在一项新的研究中,来自魏茨曼科学研究所和其他研究机构的研究人员发现,长期被忽视的称为成纤维细胞的辅助细胞实际上是极其多样和重要的。这些细胞的子集可能是硬皮病的起源,硬皮病是一种罕见的自身免疫性疾病。这些结果为这种破坏性和不可治愈的疾病的未来治疗开辟了新的方向。相关研究结果于2022年4月4日在线发表在Cell Journal上,论文标题为LG R5表达皮肤纤维定义硬皮病中受扰的主要细胞中枢。
硬皮病的特征是在手臂、腿和脸上形成异常坚硬和无弹性的皮肤层。其表现在不同的患者之间差异很大。在大约三分之一的病例中,这种主要侵袭30至50岁妇女的疾病进展迅速,扩散到四肢以外,对内脏器官造成威胁生命的损害。通常给自身免疫性疾病患者带来缓解的免疫调节药物对硬皮病的疗效较差,硬皮病的死亡率高于其他风湿性疾病。
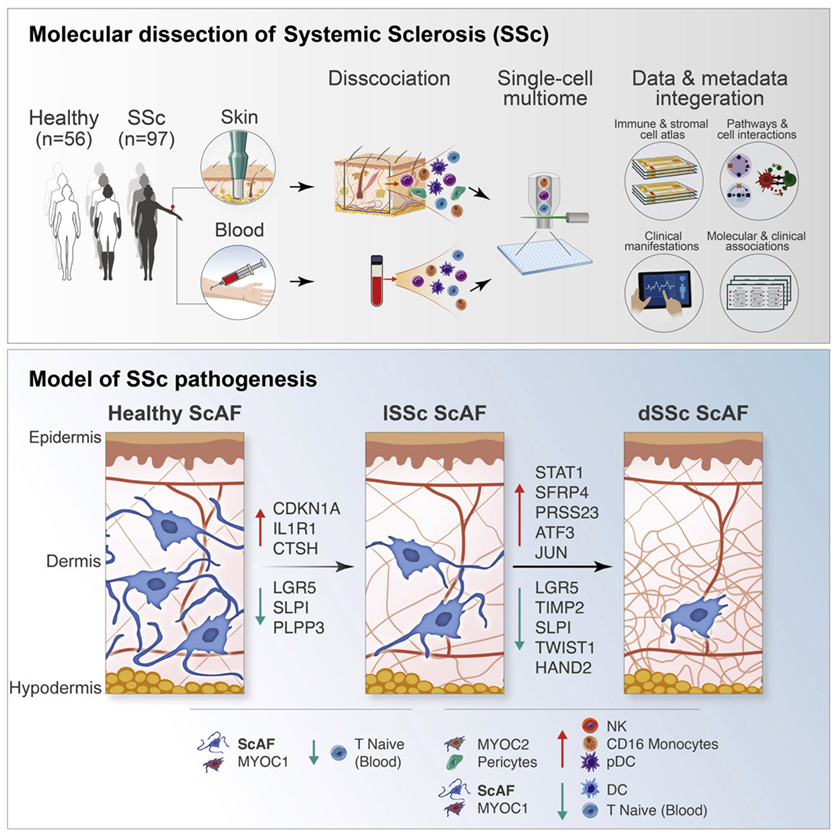
图片来自cell,2022,doi : 10.1016/j . cell . 2022 . 03 . 011。
论文的共同第一作者、魏茨曼科学研究所的Chamutal Gur教授表示,硬皮病是最令人沮丧的疾病之一。我们可以缓解患者的一些症状,但通常我们无法显著影响这种疾病的病因,阻止其进展或逆转其进展。大约三年前,当她作为博士后研究员加入论文合著者魏茨曼科学研究所(Weizmann Institute of Science)的Ido Amit实验室时,她的目标是找到这种令人困惑的疾病的根源。
Gur和他的同事使用Amit实验室开发的技术研究硬皮病,以同时探索数千个细胞的遗传物质。这项技术被称为单细胞RNA测序,揭示了每个细胞的独特身份。
这些作者收集了近100名硬皮病患者和50多名健康志愿者的皮肤样本作为对照组,这是有史以来此类疾病的最大规模研究。在完善样本采集技术的同时,古尔对自己进行了近20次皮肤活检。
因为硬皮病被认为是一种自身免疫性疾病——即免疫系统攻击人体,所以这些作者在对照组和患者组之间寻找免疫细胞的差异。但是与自身免疫性疾病的预期相反,这项分析未能在大多数患者中发现免疫异常的特征性一般模式。相反,令他们惊讶的是,他们发现患者组的成纤维细胞与对照组的成纤维细胞有显著差异。
除了在生长和伤口愈合中的作用外,成纤维细胞被认为是将细胞固定在适当位置的唯一支架。这项新的研究挑战了这种单调的观点:这些作者发现,成纤维细胞可以分为大约10个主要群体,每个群体都执行不同且通常重要的功能,从传递免疫系统信号到影响代谢、血液凝固和形成。这些组可以进一步细分为大约200个亚型。
最重要的是,这些作者成功鉴定了表达LGR5的成纤维细胞亚群,其水平在硬皮病早期急剧下降。他们将这个亚群命名为硬皮病相关成纤维细胞(SCAF)。在健康对照组中,ScAF占所有成纤维细胞的近30%,而在硬皮病患者中,这一比例急剧下降,并随着疾病的进展继续下降。
这些作者标记了ScAF在皮肤组织深处的位置,并使用这些细胞的RNA来确定是什么使功能性ScAF成为硬皮病患者中常见的功能障碍细胞。他们还发现了与特定类型的器官损伤相关的生物标志物;这些生物标志物可以帮助医生进行个性化治疗,以防止危及生命的并发症。这项新研究还揭示了与ScAF相关的信号通路,靶向这些信号通路可能在未来用于治疗硬皮病。
Amit说,关键成纤维细胞亚群数量的减少似乎是硬皮病过程中的早期事件。有可能设计一种疗法来弥补这种损失,并减缓这种疾病的发展。
论文的共同第一作者和共同通讯作者王双印博士在Amit实验室使用人工智能工具领导了这项研究的数据分析,他补充说,我们的方法对其他疾病也有意义。它揭示了涉及先进单细胞技术的详细组织分析在揭示疾病动力学方面的巨大潜力。
Amit总结道,将最新的单细胞基因组研究技术与临床数据相结合,可以给那些目前起源不明的疾病带来新的启示。(100yiyao.com)
参考资料:
Chamutal Gur等人。Cell,2022,doi : 10.1016/j . cell . 2022 . 03 . 011
了解自身免疫疾病的本质
https://medical xpress.com/news/2022-04-皮肤自身免疫性疾病. html
版权声明
本网站所有标注“来源:100医学网”或“来源:bioon”的文字、图片及音视频资料,版权归100医学网网站所有。未经授权,任何媒体、网站、个人不得转载,否则将追究法律责任。获得书面授权转载时,必须注明“来源:100医学网”。其他来源的文章均为转载文章。本网站所有转载文章都是为了传递更多信息。转载内容不代表本站立场。不想被转载的媒体或个人可以联系我们,我们会立即删除。
87%的用户都在使用100医疗网APP随时阅读、评论、分享。请扫描二维码下载-


- 相关报道
-
- 《柳叶刀》子刊:日行七千步,有八大好处!迄今最大规模/最全面研究发现,日行七千步与八种健康风险最高降低47%相关 (2025-08-05)
- 胆固醇研究新进展:上海交大/南昌医学院联合团队揭示食管鳞癌耐药新机制 (2025-08-05)
- Biosensors:新型蓝牙智能生物传感器,唾液检测乳腺癌新突破! (2025-08-05)
- STTT:清华大学董家鸿院士团队发现肝癌治疗新靶点,逆转肝癌耐药性 (2025-08-05)
- 卓悦榜丨德达医疗荣膺"年度健康服务与智慧医疗最佳企业"奖项 (2025-08-05)
- 《自然》:流感唤醒休眠癌细胞!科学家发现,呼吸道病毒感染引发的炎症和IL-6会诱导休眠散播性癌细胞表型转变,诱发乳腺癌肺转移 (2025-08-05)
- 睡眠质量不好?可以试试高钾晚餐!研究发现:晚餐钾摄入与失眠程度显著相关!其利于稳定血压、改善神经-肌肉信号及神经递质平衡 (2025-08-05)
- 黄荷凤院士团队揭示不粘锅涂层微塑料影响男性生育能力的机制,并开发出治疗方法 (2025-08-05)
- 特朗普向 17 家制药巨头发函,强制实施最惠国药价 (2025-08-05)
- 两篇Science论文:冬眠的“超能力”被锁在人类DNA中,解除锁定有望逆转阿尔茨海默病、糖尿病等疾病 (2025-08-04)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















