恒瑞医药一类新药97个 巴平31个品种首次通过审评 |
 |
近日,有“创新药一哥”之称的恒瑞医药动作频频:SHR8554注射液已提交上市申请,HRS-5965片、HR20014注射液、HRS-4642注射液首次获得临床批准。Minenet数据显示,目前,恒瑞医药处于申请临床阶段及以上的创新药(97个一类新药)共有128个,其中13个(6个一类新药)已经/即将申报生产,13个(11个一类新药)处于关键临床三期(含二/三期)。仿制药方面,评价60个品种(31个为第一),7个品种冲刺首仿(4个为独家报产)。
6大重磅首仿获批,创新药大卖超110亿
近日,恒瑞医药接连公布新品上市批文:7月2日,其4个仿制药他克莫司缓释胶囊获批生产,并被视为正在评估,为国内首仿。6月30日,其1类新药利凡拉明片获批上市,成为国内首个新型雄激素受体(AR)抑制剂。
以审评结论日期为准,2022年至今,恒瑞医药首次获批上市,1个新1类药出现新适应症;9个品种被批准生产,并被视为评估,其中6个是第一个模仿者。
2022年起,恒瑞医药获批上市。
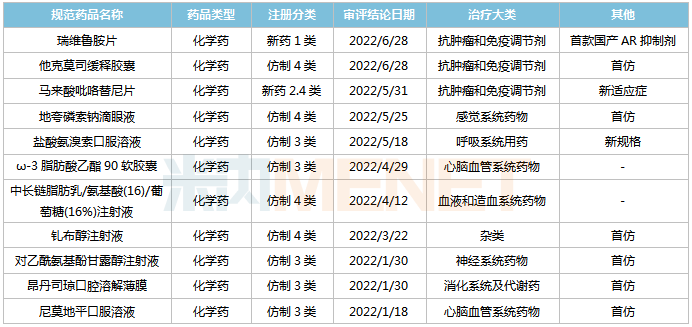
来源:Minenet MED2.0中国药物评价数据库
6个首批仿制品中,尼莫地平口服溶液、昂丹司琼口腔溶解膜、他克莫司缓释胶囊、对乙酰氨基酚甘露醇注射液为新剂型。Minenet数据显示,2021年中国城市公立医院、县级公立医院、城市社区中心、乡镇卫生院(简称中国公立医疗机构)尼莫地平、昂丹司琼、他克莫司销售额分别超过7亿元、10亿元、50亿元。
瑞鲁明片是恒瑞医药在国内批准的第11个创新药(第10个一类新药)。也是中国企业自主研发的首个新型雄激素受体(AR)抑制剂。它适用于治疗具有高肿瘤负荷的转移性激素敏感性前列腺癌(mHSPC)患者。目前,北京、上海、广州、南京、武汉、济南、长沙、贵阳等地开出了第一张地方处方。
Minenet数据显示,2019年及之前恒瑞医药获批的6个创新药,2021年在中国三大终端、六大市场(统计范围见本文末尾)的总销售额超过110亿元,其中卡列珠单抗超过40亿元,阿帕替尼超过20亿元,吡咯替尼和硫非格司汀接近20亿元。
恒医药已被批准为创新药。
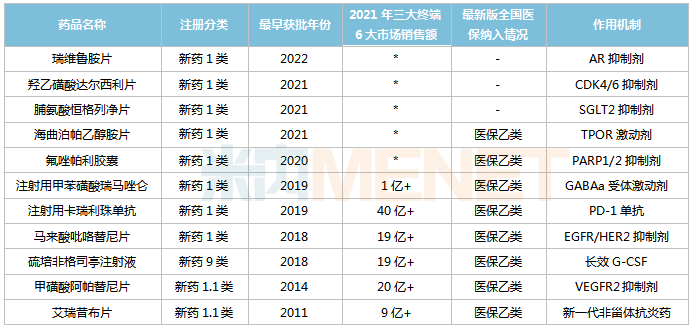
注:未售出或销售额不足1亿元以*号表示。
来源:Minenet数据库
11个创新药中,8个药品通过谈判成功纳入国家医保目录,其中2个及以上适应症纳入医保,如阿帕替尼、卡列珠单抗、氟佐帕利、Herzopopa乙醇胺等。
2022年6月29日,国家医保局公布《2022年国家基本医疗保险、工伤保险和生育保险药品目录调整工作方案》及相关文件,标志着新一轮国家医保目录调整正式开始。预计恒瑞医药的三个1类新药,即利福拉明片、羟乙磺酸达喜片、亨格列奈脯氨酸片将参与谈判。
128款在研新药霸屏,17个1类新药上市可期
作为中国“创新药”之一,恒瑞医药在创新药数量上遥遥领先。最近,该公司的研发;d管道动态频繁:一类新药SHR8554注射液申报生产,HRS-5965片、HR20014注射液、HRS-4642注射液等一类新药首次获得临床批准。
2021年以来,恒瑞医药不仅坚持自主研发,还不断加强对外合作,先后与济世药业、石田光、大连万春、法国Iktos等公司达成协议。2022年6月,公司斥巨资设立私募投资基金,专注于医疗健康行业,尤其是生物医药领域的创新研发。
资。有投资者认为,恒瑞医药又在加强其BD能力,接下来或许会收购更多生物医药公司或新药等。
米内网数据显示,含合作引进的新药在内,恒瑞医药有128款创新药(以药品名称计,不含已上市新药开发新适应症)在国内处于申请临床及以上阶段,其中有97款为1类新药。
从研发进展看,13款新药已/即将申报上市(最高研发进展,下同),其中有6款为1类新药;13款新药步入III期(含II/III期)关键临床,其中有11款为1类新药。
恒瑞医药国内在研创新药
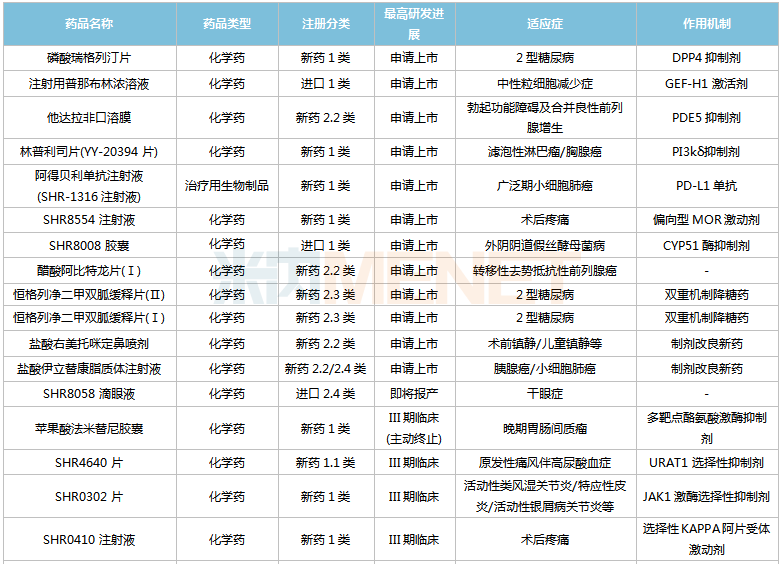
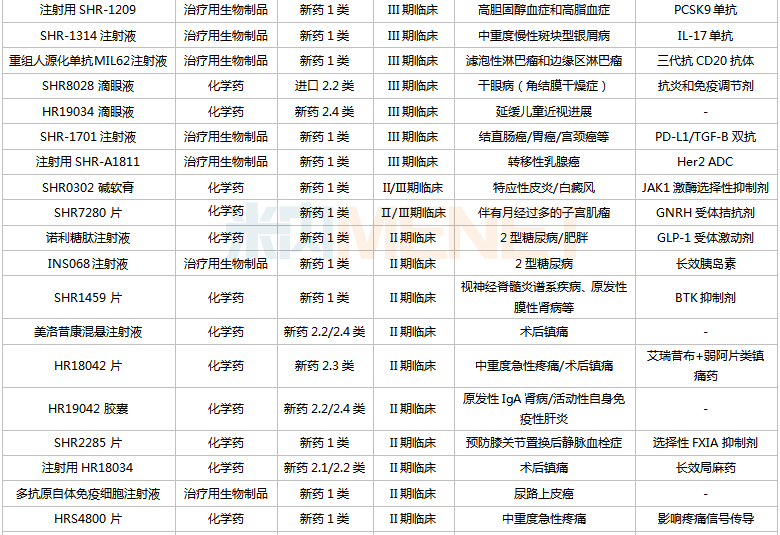
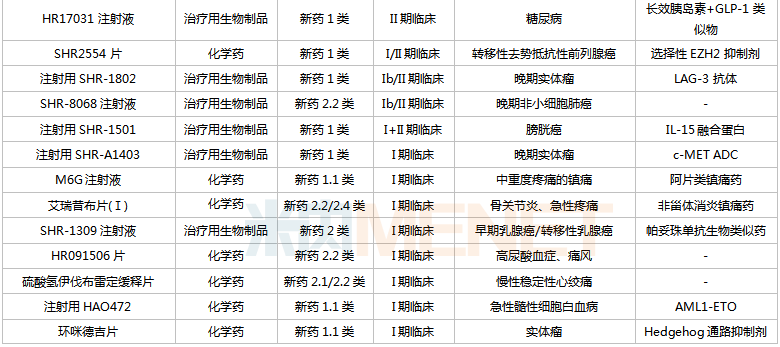
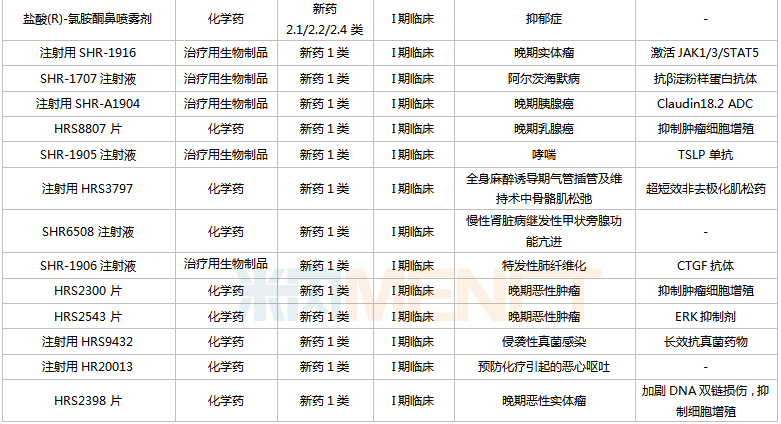
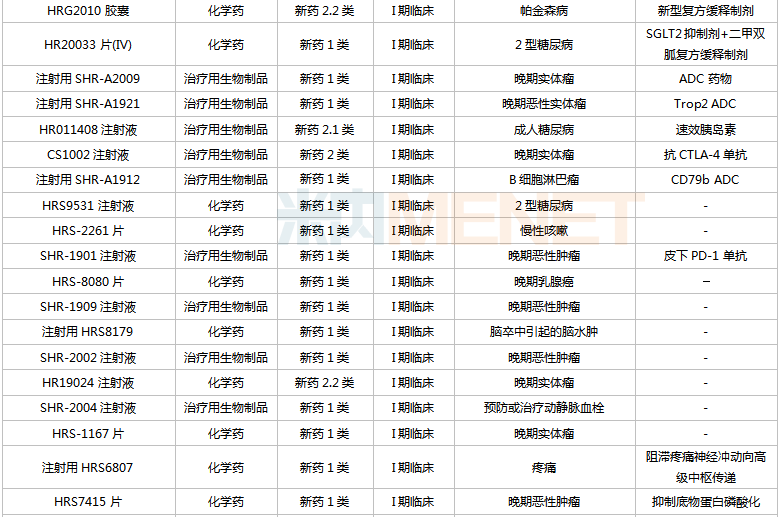
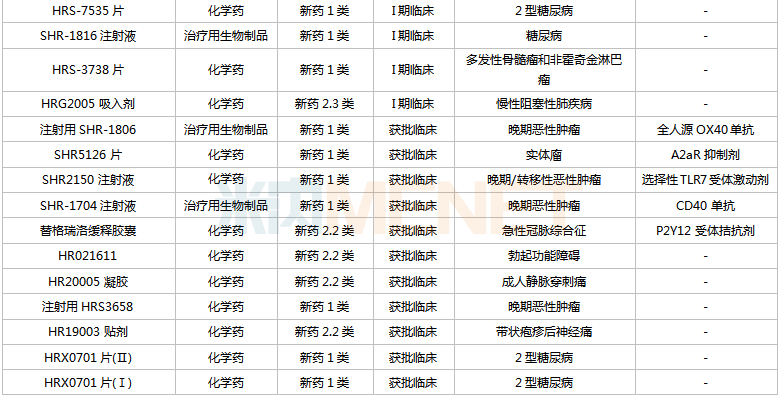
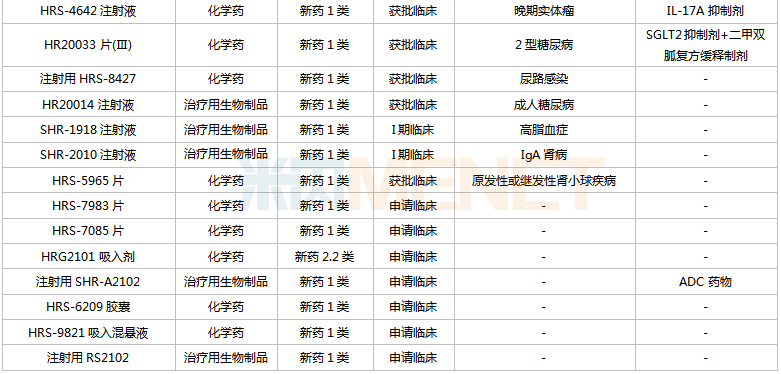
来源:米内网中国药品临床试验公示库
从适应症看,恒瑞医药在研新药集中在抗肿瘤和免疫调节剂(肿瘤、自身免疫性疾病)、消化系统及代谢药(糖尿病、肥胖、止呕等)、神经系统药物(疼痛、抑郁症、帕金森、阿尔茨海默病等)三大治疗领域。
抗肿瘤药占比超4成,涵盖肺癌、乳腺癌、肝癌、胃癌、前列腺癌、结直肠癌、尿路上皮癌、膀胱癌等多个细分病种;消化系统及代谢药以糖尿病用药为主,布局了DPP4、SGLT2、GLP-1等多个热门靶点,涵盖小分子口服药及复方制剂、速效胰岛素、长效胰岛素等;神经系统药物以麻醉止痛药为主,其中1类新药SHR8554(偏向型MOR激动剂)、2类改良型新药盐酸右美托咪定鼻喷剂已报产。
在靶点方面,恒瑞医药布局全球热门靶点和前沿工艺,如PD-(L)1、BTK、CDK4/6、ADC、JAK、CD20等;在CD40(TNFRSF5)、CD47、IL-15、OX40(TNFRSF4)、CTGF、RORC(RZRG)、ROMK、TIM-3、GPR40(FFAR1)等暂无药物获批的靶点上也有布局。
在PD-(L)1靶点上,恒瑞医药的卡瑞利珠单抗已获批上市,目前已成为纳入医保适应症最多的国产PD-1单抗,且还在持续开展联合用药及拓宽新适应症的临床研究。此外,PD-L1单抗阿得贝利单抗已报产,PD-L1/TGF-B双抗SHR-1701步入III期临床,皮下注射PD-1单抗SHR-1901步入了I期临床。
恒瑞医药是目前在研ADC药物最多的国内药企,有8款新药处于申请临床及以上阶段,其中靶向Her2的ADC药物SHR-A1811进展最快,目前正在开展III期临床。此外,有6款ADC药物步入I期临床,1款ADC药物正在申报临床。
60个品种过评,7个品种抢首仿
7月26日,国家药监局官网显示,恒瑞医药的碘化油注射液(罂粟乙碘油注射液)通过一致性评价,为国内首家。
目前恒瑞医药有60个品种过评(31个为首家),涵盖12个治疗大类,集中在抗肿瘤和免疫调节剂(13个品种)、神经系统药物(11个品种)、心血管系统药物(8个品种)等治疗领域;剂型分布较广,除了普通口服常释剂型,还包括注射剂、缓控释制剂、吸入剂、滴眼剂、口溶膜等。
恒瑞医药过评情况
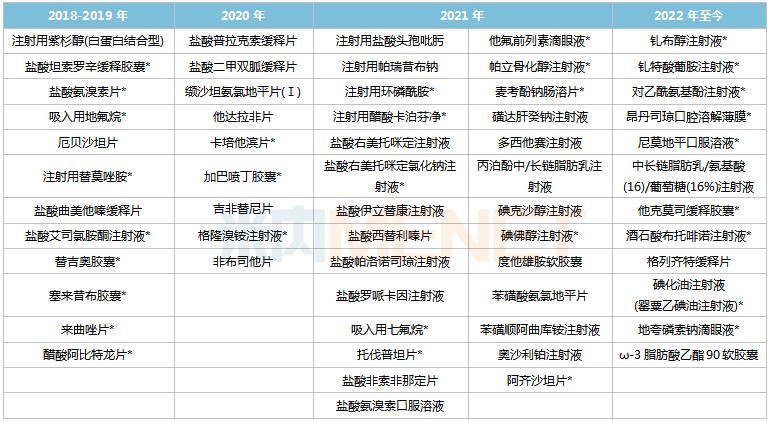
注:带*为首家/独家过评
来源:米内网MED2.0中国药品审评数据库
在政策阵痛面前,恒瑞医药决定“砍掉”部分仿制药项目,只做创新药和有核心价值的高端仿制药。2022年至今,公司仅提交了3个品种的一致性评价补充申请,暂无仿制药提交上市申请。
目前恒瑞医药有8个一致性评价补充申请品种在审,其中注射用奥沙利铂、碳酸氢钠林格注射液、复方醋酸钠林格注射液(钠钾镁钙葡萄糖注射液)、美司钠注射液、罗格列酮片等品种暂无企业过评。新分类申报仿制药中(不含已撤回或不批准品种),有7个暂无首仿(含剂型首仿)获批。
恒瑞医药新分类申报且暂无首仿获批的品种
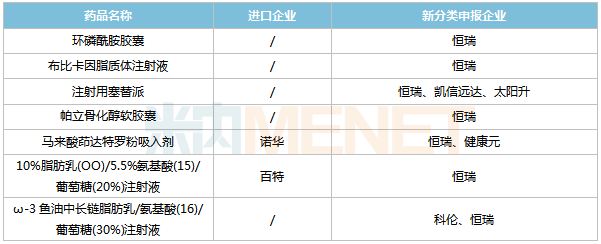
来源:米内网MED2.0中国药品审评数据库
环磷酰胺胶囊、布比卡因脂质体注射液、帕立骨化醇软胶囊、10%脂肪乳(OO)/5.5%氨基酸(15)/葡萄糖(20%)注射液由恒瑞医药独家申报。
来源:米内网数据库、公司公告等注:米内网《中国三大终端6大市场竞争格局》,统计范围是:城市公立医院和县级公立医院、城市社区中心和乡镇卫生院、城市实体药店和网上药店,不含民营医院、私人诊所、村卫生室,不含县乡村药店;上述销售额以产品在终端的平均零售价计算。审评数据统计截至8月10日,如有疏漏,欢迎指正!
医药网新闻
- 相关报道
-
- 中国—东盟卫生官员广西探讨深入疾病防控单干 (2025-09-18)
- 李利在广西调研药品监管“十五五”布局任务 (2025-09-18)
- 国度卫健委提三倡导亲密中国—东盟卫生单干 (2025-09-17)
- 性命“底线”若何守护?我国多措并举增强患者平安治理 (2025-09-17)
- 联袂共倒退!中国医学研讨为环球安康注入力气 (2025-09-16)
- 黑龙江:全面深入药品医疗东西监管改造匆匆进医药家当高质量倒退多少步伐 (2025-09-15)
- 规范生物医学新技术利用 助力安康中国建设 (2025-09-15)
- 国度卫健委:我国建成天下规模最年夜医疗服务系统 (2025-09-12)
- 中国建成天下上规模最年夜疾控系统和医疗服务系统 (2025-09-12)
- 国产九价HPV疫苗首针9月9日在厦门开打 价钱更亲平易近、接种更便捷 (2025-09-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















