第八批集中采集会纳入生物相似药吗?80家企业争夺百亿市场! |
 |
随着第七集的结束,第八集成为了业内的热门话题。其中,广受关注的“生物药集”终于有了新消息。
国家医保局发布《关于政协十三届全国委员会第五次会议第03703号 (医疗卫生类329号)提案答复的函》,回复了朱一龙委员提出的关于引入创新新药准入评价机制的提案。在回复中明确表示,将结合生物药品的特点,不断完善生物药品的采集规则。
第六批国家组织胰岛素集中采购,打响了生物药品集采的“第一枪”。医保局的回函更多的是面向生物药采集。在业内人士看来,生物相似药的采集迫在眉睫,预计今明两年将常态化。
箭在弦上
“国采”蓄势百亿市场涌动
国家医保局在回函中表示,目前已集中采购6批化学药品和1批生物药品(胰岛素专用),取得积极进展。
同时,国家医保局也指出了生物药品集中采集的难点:与化学药品相比,生物药品没有一致性评价作为支撑,命名复杂,产能爬坡慢。因此,国家医保局会同相关部门,在化学药采集的基础上进一步调整完善规则,充分考虑生物药的特点,精心制定了胰岛素采集规则:
一是医疗机构在采集前按品牌提交需求,产生中标结果后,医疗机构按照一定的规则选择中标产品,充分尊重临床选择,保持临床用药的稳定性。
二是将治疗目的和临床机制相似但通用名不同的产品进行组合分组,兼顾了临床使用需求和竞争的充分性。
再次,根据生物药产能约束的特点,通过摸底调查全面掌握企业产能,设定协议采购量不超过企业最大产能的50%,落地时预留足够的生产准备时间,多措并举保障供应。
事实上,国家医保局此前也多次发布消息,意图“将生物相似药品纳入集中带量采购”。这一次,国家医保局已经明确透露了“将生物相似药品纳入集中带量采购”的思路和导向。回函表示,下一步将在现有成功经验的基础上,结合生物药品的特点,不断完善生物药品的采集和采购规则。这也意味着,推进生物药集中采购可能已经进入日程。
去年2月,CDE发布了《生物类似药相似性评价和适应症外推技术指导原则》,专门对生物相似药物的“相似性”进行了定义。这被业内认为是生物相似药的“一致性评价”,也被认为是为生物相似药纳入采集做准备。
胰岛素采集的探索和实践也为生物相似药物的组织采集积累了一些经验。作为典型的生物制药,胰岛素大分子产品不同于小分子化学药物,不能简单评价一致性。然而,与复杂的生物药物相比,多肽胰岛素和胰岛素类似物有其特殊的性质。
2021年11月,胰岛素国家专项集中采购启动。本次药品集中采购包括餐用人胰岛素、基础人胰岛素、预混人胰岛素、餐用胰岛素类似物、基础胰岛素类似物和预混胰岛素类似物,共6个采购组。预计第一年全国胰岛素采购需求2.1亿,涉及170亿元,入选产品价格平均下降48%。
事实上,收集和收集生物相似的d
随着生物类似物的相继获批,国内生物类似物市场不断扩大。根据Frost Sullivan的数据,预计到2030年,中国生物相似药市场规模将达到589亿元,三年内将有近30种国产生物相似药上市。
从国内生物相似药市场的竞争格局来看,很多产品已经满足了三家公司充分竞争的条件,具备了一定的市场规模。随着这一次,医疗保险局已明确采取下一步的规则,生物相似药物的收集,下一批生物相似药物的收集迫在眉睫。
群雄逐鹿
国内生物类似药迅猛发展
仿生药物是指那些在质量、安全性和
有效性方面与已批准生物原研药具有相似性的治疗用生物制品。“相似性”是指候选药与已获批的参照药整体相似,且在质量、安全性以及有效性方面与参照药不存在有临床意义的差别。
生物类似药在欧美已经经历了漫长的发展历程,近年来,国内的生物类似药领域也热潮涌动,处于百花齐发的竞争态势。
目前国内约180家药企已布局生物类似物的产品研发,共涉及约400款药物,在研的生物类似药大多集中在CD20、VEGF、HER2等热门靶点,竞争将不言而喻。国内药企上市的生物类似药,主要是这六款:贝伐珠单抗、阿达木单抗、曲妥珠单抗、利妥昔单抗、地舒单抗和英夫利西单抗。
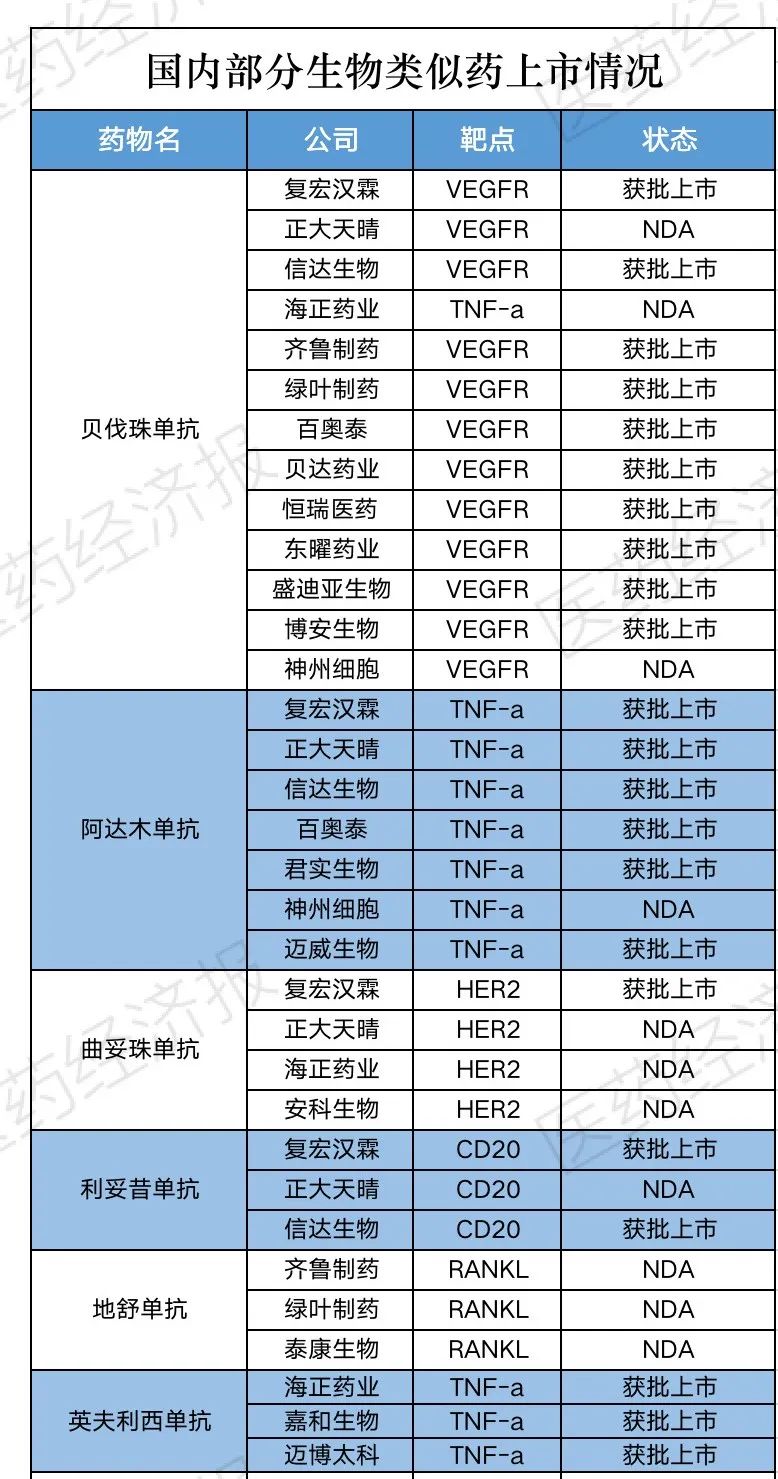
贝伐珠单抗是竞争最为激烈的生物类似药品种之一,超百亿市场已经有40多家药企争相布局。截至目前,国内获批上市的贝伐珠单抗药物共计10种,包括罗氏,复宏汉霖,东曜药业,贝达药业、百奥泰、东博安生物、信达生物、齐鲁制药等,另有多款处于注册申请或临床试验阶段,市场竞争十分激烈。
贝伐珠单抗是由罗氏研发的一款人源化单克隆抗体IgG1,是一种血管生成抑制剂,也是美国第一个获批上市的通过抑制肿瘤血管生成的药物,获批时间为2004年。由于适应症广泛,对多类型肿瘤都有出色疗效,上市后第一个完整销售年收益就超过10亿。
米内网数据显示,2016-2021年贝伐珠单抗在国内样本医院销售终端均呈现稳步增长的态势,每一年都在增长。2020年销售成绩17.31亿元,同比增长18.08%,2021全年销售额25.51亿元,同比增长47.43%。
竞争格局方面,原研厂商罗氏和齐鲁制药占据了市场的绝对地位,合共占比超90%;作为首仿的齐鲁制药,已经在市场上以55.34%份额,后面两年获批的几个厂商目前仅能分得10%不到。
其次是阿达木单抗,国内生产厂家已达6家。原研药企是艾伯维,生物类似药企分别是百奥泰、海正药业、信达生物、复宏汉霖、正大天晴、君实生物。紧盯阿达木单抗生物类似药市场的在研企业至少还有20家。据弗若斯特沙利文报告显示,中国阿达木单抗生物类似药市场将在2023年增至47亿元,并于2030年达到115亿元规模。
根据国家集采规则,纳入医保目录内用量大、采购金额高+临床必需+质量可靠规则,且竞争比较充分的产品。国家集采既要节省医保基金,又要保证质量和供应,让患者获益。由此可见,国内多种生物类似药基本符合条件。
随着我国药企研发水平的提升及政策放开,我国生物类似药近年来发展迅猛,并在一些疾病治疗领域显示出明显的临床优势,因此将生物药纳入集采范围对企业的影响已是不容忽视。
在业内人士看来,集采、医保谈判是近几年中国生物医药行业必谈的话题,也是所有在中国生存的生物医药企业都绕不开的问题。集采困局和之前提到的同质化竞争困难是类似的根源,就是生产同款药的企业太多了,只能降价拼市场。
但国家集采并不是一味地让企业降低价格,而是缓解竞争,让国内制药企业谨慎选择研发药物,不仅避免产品过度集中、竞争过于激烈导致价格过低,也有利于国内头部企业研发更具有临床价值的药物。
医药网新闻
- 相关报道
-
- 上海生物医药家当规模预计本年破万亿元 (2025-10-10)
- 国度药监局对于扶正摄生丸转换为非处方药的布告 (2025-10-10)
- 国度金融监管总局宣布推进安康保险高质量倒退的指导意见 (2025-10-09)
- 慢阻肺病归入根本公卫服务落地追踪:“呼吸之痛”若何缓解? (2025-10-09)
- 若何替行为方便白叟用医保开药?国度医保局解答 (2025-10-09)
- 国度医保目次抗癌药品已超230种 (2025-10-09)
- 收益率达8.1% 2024年全国社保基金取得较好投资业绩 (2025-09-30)
- 山东三部分推进药品运营使用环节全种类信息化追溯系统建设 (2025-09-28)
- 国度药监局对于牙膏立案治理无关事项的布告(征求意见稿) (2025-09-28)
- 新疆医疗程度正迈向智能化、精准化新阶段 (2025-09-26)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















