每月用药1次!痛风新药两项III期研究成功 |
 |
来源:医药魔方 2023-03-24 09:26
3月21日, Selecta Biosciences和Sobi公布了两项III期研究(DISSOLVE I 和DISSOLVE II)的积极关键结果。这两项安慰剂对照、随机临床试验旨在评估两 3月21日,Selecta Biosciences和Sobi公布了两项III期研究(DISSOLVE I 和DISSOLVE II)的积极关键结果。这两项安慰剂对照、随机临床试验旨在评估两个不同剂量水平的SEL-212在成人慢性难治性痛风患者中的安全性和有效性。
痛风属于自身炎症性疾病,患者因为促炎性尿酸钠(MSU)晶体沉积引发剧烈疼痛和衰弱性炎症性关节炎。慢性难治性痛风患者往往存在高组织MSU负担,可导致痛风频繁发作和慢性关节炎。痛风是美国最常见的炎症性关节炎疾病。
Pegsiticase(又名pegadricase,一种可代谢尿酸的重组酶),由三生制药开发,2014年三生制药授权Selecta利用该公司的ImmTOR 耐受平台将其开发成SEL-212。
2020年7月29日,Sobi和Selecta宣布,两家公司已就Selecta研发产品SEL -212达成了战略许可协议。根据合作协议,Sobi负责大中华区(包括中国大陆、香港、澳门、台湾)以外所有市场的开发、注册和商业活动,而Selecta则代表Sobi开展III期研究。
SEL-212具有降低慢性难治性痛风患者血清尿酸和MSU沉积的潜力。重组尿酸酶在人体内具有高度免疫原性,通过Selecta专有的ImmTOR平台,SEL-212具备了减轻抗药物抗体形成的潜力,从而可以方便的每月给药一次,提高尿酸酶的疗效和耐受性。DISSOLVE I(美国研究)达到了主要终点,接受每月0.15mg/kg剂量和0.1 mg/kg剂量SEL-212治疗的患者中,分别有56%和48%达到缓解标准(定义为在第6个月,至少有80%的时间实现并维持血清尿酸(SU) 6mg/dL),而安慰剂组仅4%患者实现缓解。
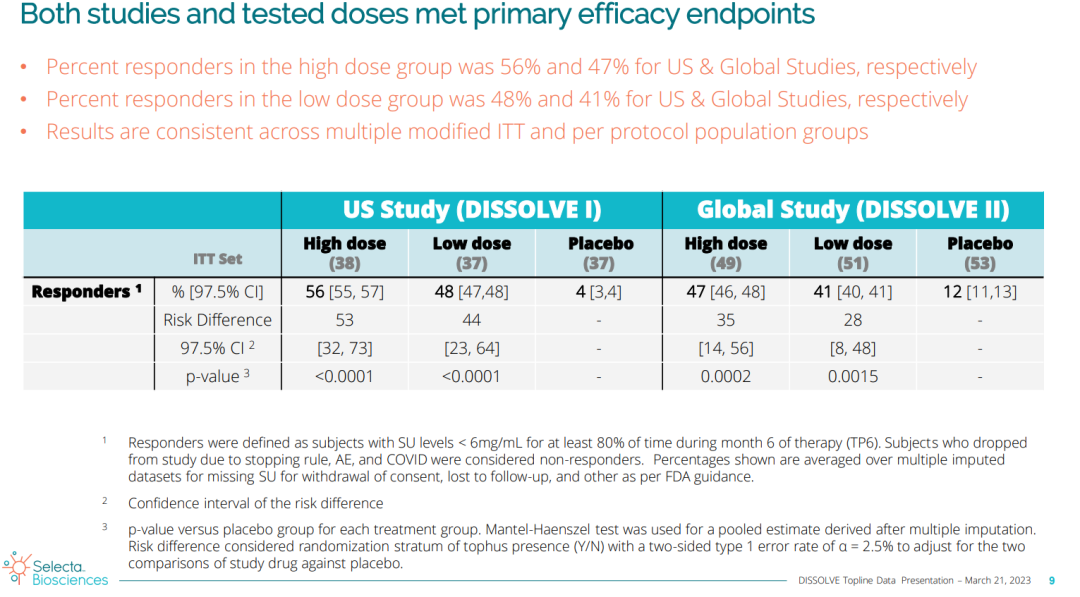
DISSOLVE II(全球研究)同样达到了主要终点,接受每月0.15 mg/kg剂量和0.1 mg/kg剂量SEL-212治疗的患者中,分别有47%和41%达到缓解,而安慰剂组这一比例为12%。
在50岁及以上的患者中,两项试验中SEL-212高剂量组均实现学意义的高应答率;另外,与安慰剂相比,随机接受SEL-212(0.15mg/kg)治疗的患者平均SU水平总体降低69%,具有显著临床意义。
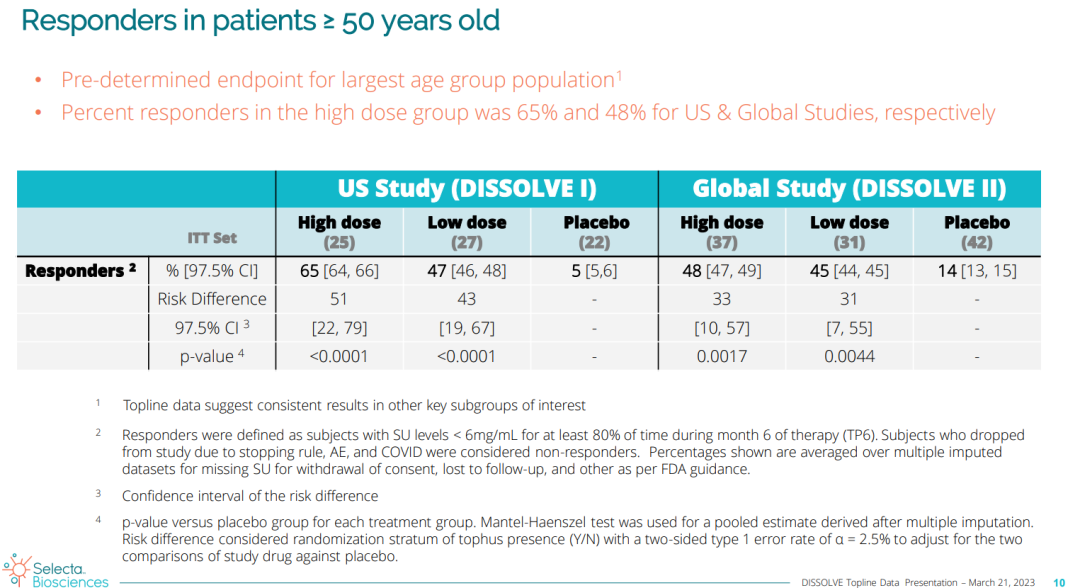
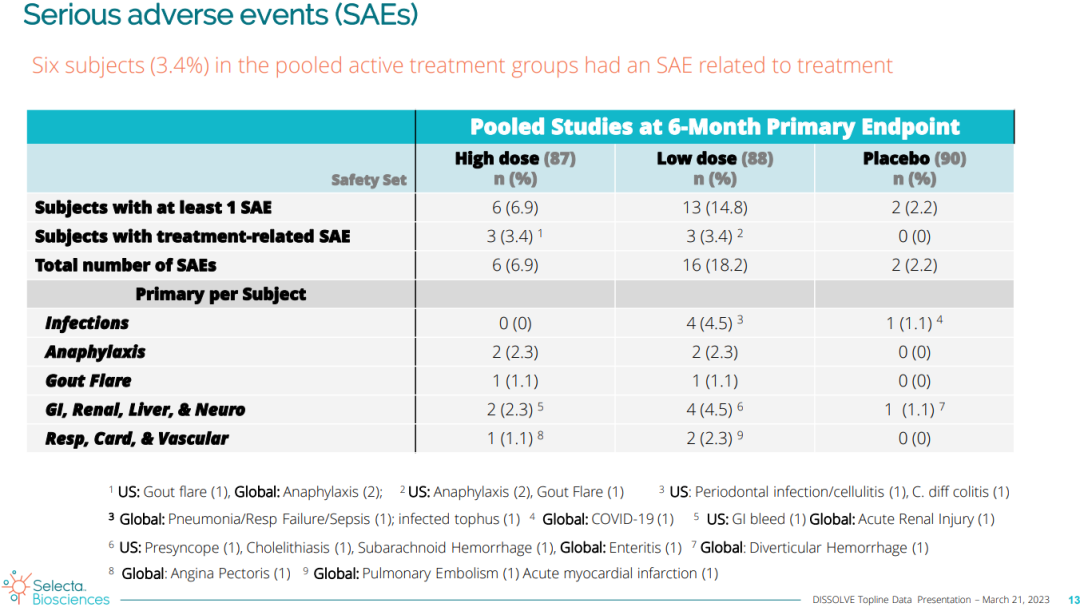
两个剂量的SEL-212均具有良好的安全性和耐受性,试验中出现的不良事件(AEs)是预期内的。在6例患者中观察到与治疗相关的严重不良事件。
 医药网新闻
医药网新闻

- 相关报道
-
- 金赛药业携手全球最大的脱敏治疗药企ALK,有望开启中国脱敏治疗新时代 (2025-09-18)
- Nature Methods:当百年病理学遇见AI——iSCALE赋能H&E图像,预测细胞级空间转录组 (2025-09-18)
- 《健康报》专访上海交通大学医学院海南国际医学中心数智医学研究院院长王慧:人工智能推动健康管理深度重构 (2025-09-18)
- Cell Stem Cell:血癌基因DNMT3A的惊人新角色!科学家解锁造血干细胞长寿的奥秘 (2025-09-18)
- 华人学者发表Nature论文,揭示这种基因突变为何会导致阿尔茨海默病 (2025-09-18)
- 为什么感冒鼻塞时,吃东西会没味道?最新Nat. Commun:原来味道不仅需要味觉,还需要嗅觉! (2025-09-18)
- 《自然·免疫学》:打破传统认知!大坪医院/昆明市延安医院团队从头设计多肽,精准抑制细胞焦亡孔道功能,为炎症治疗开辟新途径 (2025-09-17)
- 流感季不用慌!Sci Adv:“抗体鸡尾酒”抗多种毒株还不怕突变,感染5天给药仍能救命 (2025-09-17)
- 新疆放慢构建当代中药家当系统 (2025-09-17)
- 《免疫》:科学家首次发现,最毒乳腺癌在转移前就拿下了抗癌前哨! (2025-09-17)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















