张锋最新Nature论文:借助AlphaFold,改造出全新蛋白质定向递送系统 |
 |
来源:网络 2023-03-30 14:21
如果把细胞比作是精密的机械钟表,那么蛋白质就是其内部大大小小的齿轮,它们是生命活动的主要执行者,发挥着生命基石般的关键作用。而蛋白质结构是其功能的基础,如果我们能任意改造蛋白质结构如果把细胞比作是精密的机械钟表,那么蛋白质就是其内部大大小小的齿轮,它们是生命活动的主要执行者,发挥着生命基石般的关键作用。而蛋白质结构是其功能的基础,如果我们能任意改造蛋白质结构,那么就能自由控制其功能,其潜在应用无疑非常巨大。
要想实现这一点,准确预测或解析蛋白质的三维空间构象是关键第一步。在过去,想要确定蛋白质结构不仅困难而且耗时耗力。而随着人工智能(AI)技术的发展,DeepMind公司开发的AlphaFold,能够仅依据蛋白质序列信息,就能快速准确预测蛋白质三维结构,其强大的能力受到越来越多的关注和应用。
3月29日,CRISPR基因编辑先驱张锋教授及其团队在《Natrue》期刊发表了题为 Programmable protein delivery with a bacterial contractile injection system 的研究论文。
在这项最新研究中,张锋团队通过AlphaFold辅助蛋白质设计开发了一种蛋白质递送系统 改造、利用独特的细菌 注射器 将蛋白质注射到人类细胞中。这种新型蛋白质递送方式或将改变基因治疗、癌症治疗等前沿疗法格局,具有强大的应用前景。

内共生细菌是一类特殊的细菌,它们可以寄生在宿主细胞的内部,并已然进化出复杂的传递系统使其分泌调节宿主细胞的生物因子。例如,细胞外可收缩注射系统(eCIS),正是这样一种类似于 注射器 的大分子复合物。eCIS通过驱动一个 针头 结构穿透细胞膜,然后将携带的蛋白质有效载荷注入到真核细胞中。
eCIS广泛分布在细菌和古菌中,并已被证明具有多种天然功能,包括调节宿主细胞骨架、DNA切割,诱导变形运动和产生宿主毒性。最近,有研究发现eCIS可以靶向小鼠细胞,这就提高了eCIS作为蛋白质递送工具的可能性。
然而,eCIS的活性尚未在人类细胞中得到证实,如果想要将eCIS开发为靶向递送系统,就要先阐明eCIS识别靶细胞的机制。
在这项最新研究中,张锋团队首先选定了eCIS的一个亚型 Photorhabdusvirulence cassette(PVC)。PVC由一个约20kb的操纵子组成,包含16个核心基因(pvc1-16),以及下游的有效载荷Pdp1和Pnf。研究团队发现,PVC有效载荷蛋白的N端高度无序区域是其 包装结构域 ,只要将其与想要递送的蛋白(例如GFP)融合,就能将其加载到PVC复合体中。
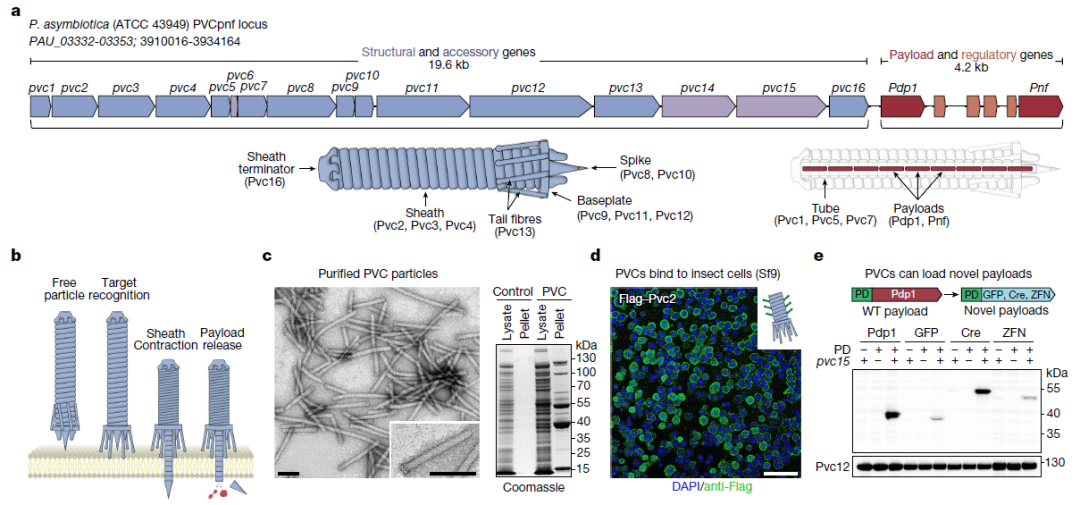
PVC系统可以被重新编程以在真核细胞中定制蛋白递送
值得注意的是,除了N端高度无序区域之外,Pvc13(尾纤维蛋白)和Pvc15(一种ATP酶)也是该递送系统成功的关键。其中,Pvc13可能参与了PVC复合体的靶标识别,并可用于操纵PVC复合体的靶标特异性。
基于此,研究团队使用AlphaFold预测Pvc13的三维结构,当将其作为三聚体时,Pvc13的C端形成了一个预测的螺旋管结构和一个球状的尖端结合结构域。研究团队由此假设,改变Pvc13的这个尖端结合域的结构特征可能会导致PVC的靶向性发生可预测的变化。
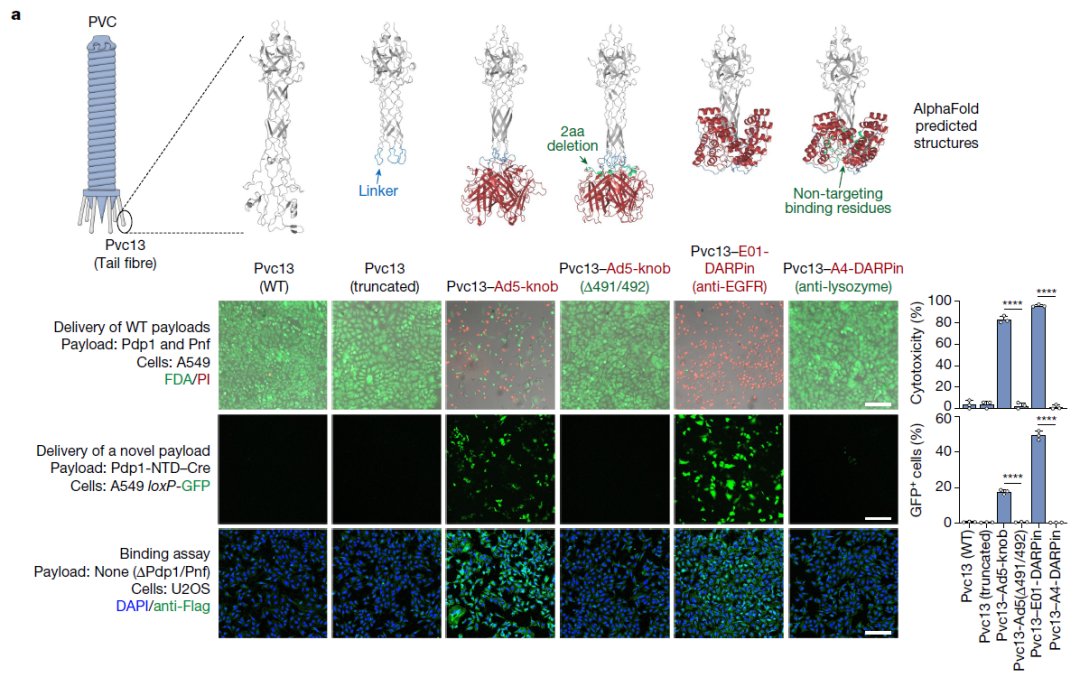
AlphaFold预测和改造Pvc13,以改变PVC系统的宿主细胞靶向性
为了验证这一点,研究团队将针对人类细胞的结合结构域(Ad5-knob和E01-DARPin)插入到Pvc13的C端结合域,并测试由此产生的PVC复合体是否可以靶向人类细胞。结果显示,改造后的PVC可以有效杀死A549细胞(携带毒性基因)或高效表达GFP(融合蛋白)。
这些结果表明,Pvc13是PVC复合体的一个靶向性决定元件,该蛋白可以被修饰,从而靶向特定的细胞系。
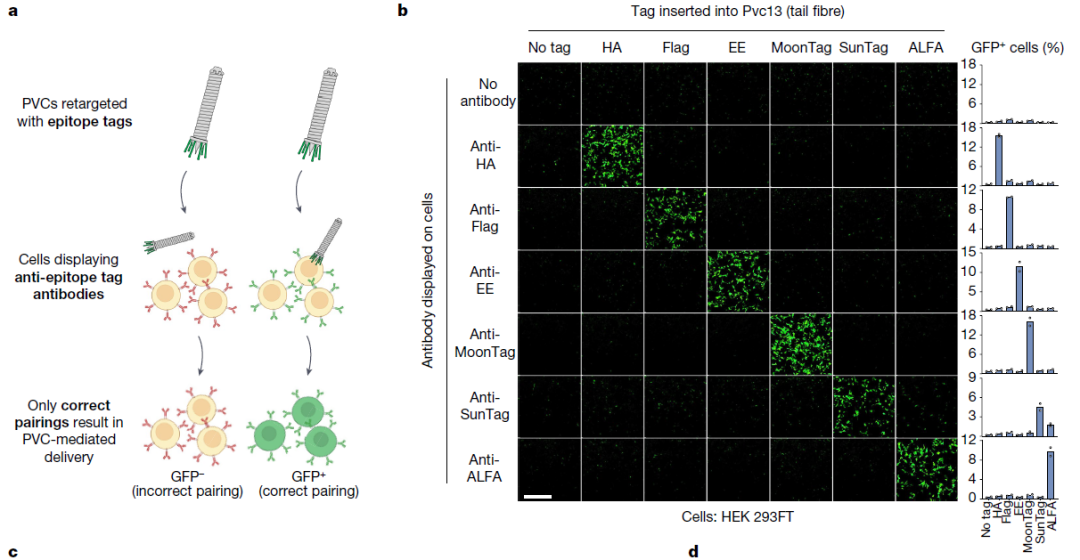
PVC介导的蛋白递送具有高度特异性
进一步研究显示,改造后的PVC复合体还可以自由装载spCas9、锌指脱氨酶(ZFD)以及细胞毒素等不同的效应元件,前两者分别实现对靶细胞DNA的基因编辑和不依赖RNA的基因编辑,后者则可以靶向清除癌细胞、衰老细胞等有害细胞。
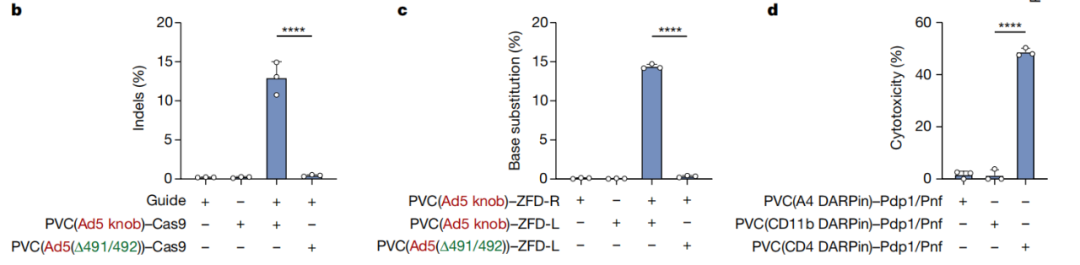
改造后的PVC系统可以靶向递送多种效应元件
不仅如此,为了验证PVC递送系统在活体动物中的效果,张锋团队再次使用AlphaFold引导Pvc13的工程化设计,并筛选到两种靶向小鼠细胞的PVC系统 Pcc-13-Ad5-knob(RGD/PK7)和Pvc13-Anti-MHCII Nb。与预期一致,前者表现出较为广泛的趋向性(正如Ad5 RGD/PK7病毒感染那样),而后者则对MHC+细胞表现出强烈的偏好性。
张锋团队还发现,PVC治疗没有产生任何显著的免疫细胞激活、炎症细胞因子产生、体重损失或细胞毒性,这表明PVC治疗在实验过程中没有产生免疫原性或毒性。此外,PVC治疗七天后就无法从小鼠大脑中检测到PVC相关蛋白,这表明PVC递送系统仅在大脑中短暂停留,不会持续太长时间。
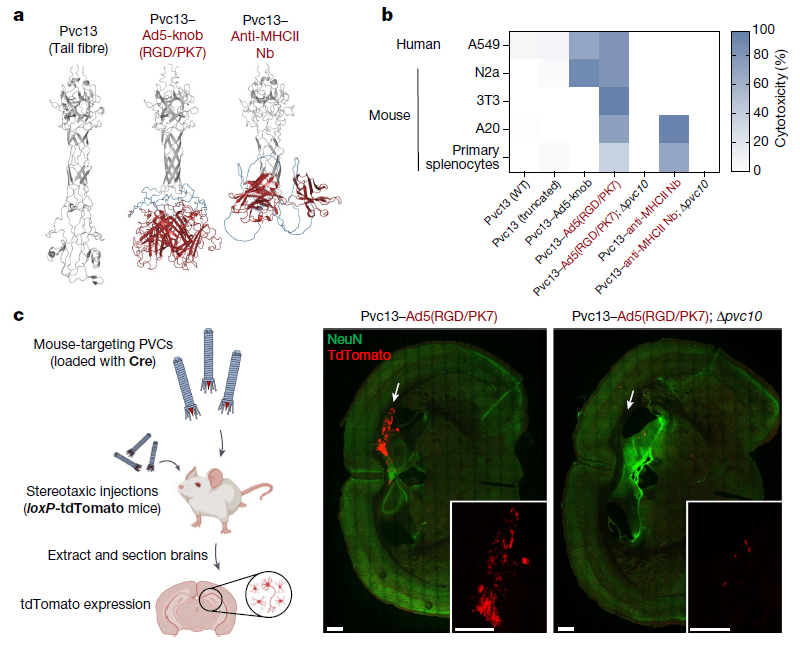
重编程的PVC系统在小鼠体内实现靶向递送
总的来说,这些结果表明,PVC系统经过改造后可以在细胞和体内靶向递送蛋白质,并在基因编辑、癌症治疗和临床靶向递送等领域展现出广阔的应用前景,未来可能成为许多生物疗法的关键递送工具。
论文链接:
https://www.nature.com/articles/s41586-023-05870-7
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- PNAS:精子也“飙车”?科学家发现能量开关,有望颠覆不孕与避孕未来 (2025-10-16)
- Cell:小胶质细胞-星形胶质细胞交谈调节突触重塑 (2025-10-16)
- 香港西医病院开院首年将提供门诊及日间住院等服务 (2025-10-16)
- 国度药监局对于刊出氯雷他定片等80个药品注册证书的布告 (2025-10-16)
- 《自然·神经科学》:从身到心,一次改善!单剂量裸盖菇素可快速且持续地缓解慢性疼痛小鼠痛觉异常和情绪障碍 (2025-10-16)
- 山东优化养老服务网络 变“养老”为“享老” (2025-10-16)
- Nature Medicine:当新生儿筛查遇上基因组测序,我们准备好了吗? (2025-10-16)
- 颜宁团队连发两篇论文:解析“酷寻”策略发现的全新糖纤维结构,并开发绝对手性判定新算法 (2025-10-16)
- Cell:里程碑式突破!I/IIa期临床试验证实hESC衍生细胞移植可安全并有效地重建帕金森病患者的多巴胺能系统 (2025-10-16)
- 抑郁不只是“情绪感冒”!Science 子刊揭密:大脑糖链“脱落”才是关键,靶向修复或破治疗困局 (2025-10-15)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















