CRM:中国科学家首次发现,放疗会让肿瘤微环境“先扬后抑”! |
 |
来源:奇点糕 2023-09-07 10:54
总体来说,这项研究系统地揭示了放疗后肿瘤微环境组成和动态变化,为优化放疗与免疫治疗的联合策略提供了新的见解。接下来,需要进一步研究来验证CD39抑制剂+放疗或VISTA抑制剂+放疗在临床上的可行性和有近日,天津市肿瘤医院陶振团队和华中科技大学同济医学院附属同济医院谌科团队合作完成的最新研究成果,发表在Cell Reports Medicine期刊上,首次全面描述了放疗后肿瘤微环境的动态变化。
他们发现,Lewis小鼠接受放疗后的初始阶段,肿瘤微环境表现为免疫激活状态,但随着时间的推移转为免疫抑制状态。使用放疗+CD39抑制剂,或放疗+VISTA抗体联合治疗,可以改善放疗后的免疫细胞浸润,与单一治疗相比显著延长多种癌症模型小鼠的总体生存期。
天津市肿瘤医院的张玉涵和华中科技大学同济医学院附属同济医院胡俊逸是论文的共同第一作者。

论文首页截图
先前的研究表明,放疗对肿瘤微环境的影响可能具有两面性,能够同时诱发免疫刺激效应(如激活原位疫苗效应和招募T细胞)和免疫抑制效应(如造成缺氧和调节性T细胞扩增)。但受限于肿瘤微环境的异质性和复杂性,我们对放疗后免疫微环境的变化尚未获得全面的认知。
在这项研究中,研究者们构建了Lewis肺癌小鼠模型并进行放疗(20Gy)。为描述放疗后微环境的动态变化,他们利用单细胞RNA测序(scRNA-seq)、单细胞T细胞受体测序(scTCR-seq)等技术,在小鼠接受放疗后第0天、第4天、第10天时,对其肿瘤中的不同类型免疫细胞的数量、分化状态和功能进行分析。
结果显示,放疗后第4天,肿瘤内细胞毒性CD8+T细胞(CTL)和自然杀伤细胞(NK)的浸润数量和增殖能力提升,终末耗竭CD8+T细胞比例减少;而在放疗后第10天,终末耗竭CD8+T细胞的比例明显增加,高表达Pdcd1、Lag3、Tigit等耗竭特征基因,低表达Tcf1、Sell、Gzma等与免疫记忆或细胞毒性相关的基因。
也就是说,CD8+T细胞介导的抗肿瘤免疫在放疗后早期被激活,随后表现出衰竭的趋势。
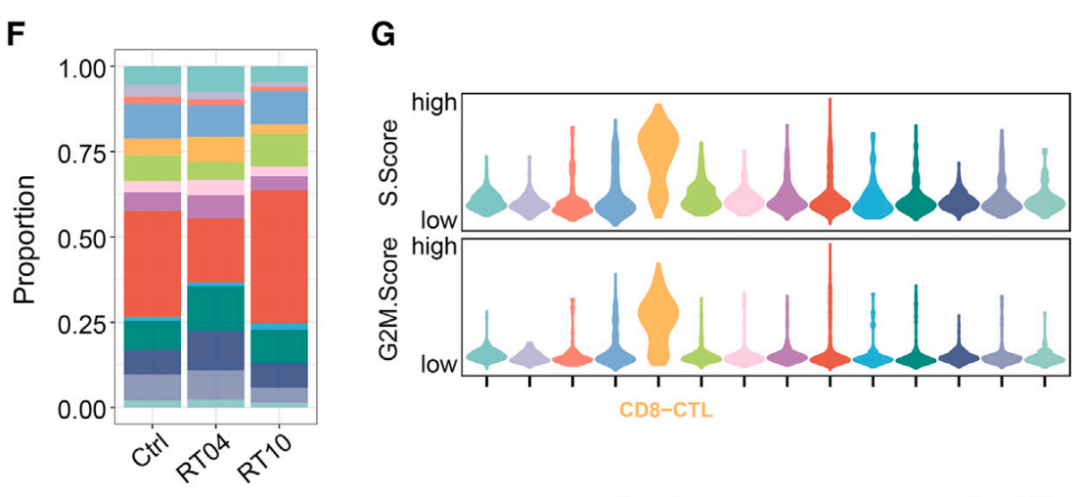
放疗后CTL浸润情况
不仅如此,研究者们发现,负责唤醒T细胞的树突状细胞(DCs),其成熟过程在放疗后被限制,导致无法有效激活CD4+T细胞或CD8+T细胞,加剧T细胞的功能障碍。
进一步分析表明,放疗还能够驱动巨噬细胞向促生成方向的分化。根据转录组学数据显示,放疗后巨噬细胞中的缺氧因子HIF-1 持续激活,暗示这个作用是通过HIF-1 来实现的。在这里,研究者们对患者的单细胞数据进行分析表明,Macro-HK2、Macro-HSP、Macro-MT等巨噬细胞亚群具有缺氧和促血管生成活性,它们或是NSLCL患者的潜在治疗靶点,尤其是在接受放疗后。
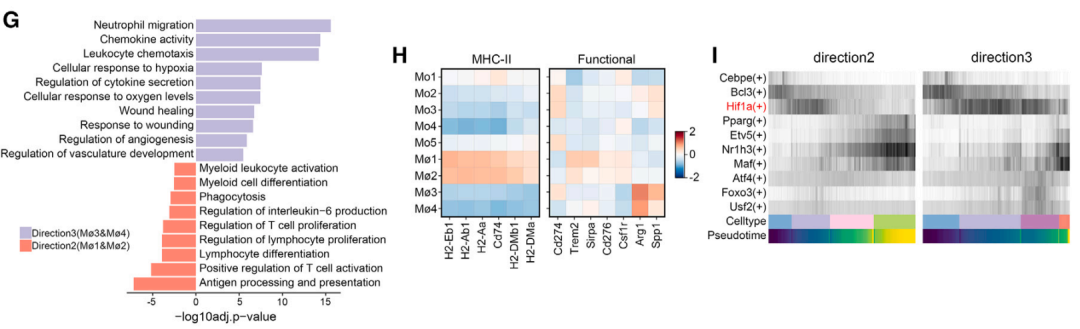
放疗后肿瘤内的巨噬细胞分化方向
另外,他们还观察到,相较于其它分化方向的巨噬细胞,这些向促血管生成方向分化的巨噬细胞表达有更多趋化因子,从而在放疗后招募大量的免疫抑制性中性粒细胞聚集在肿瘤内。
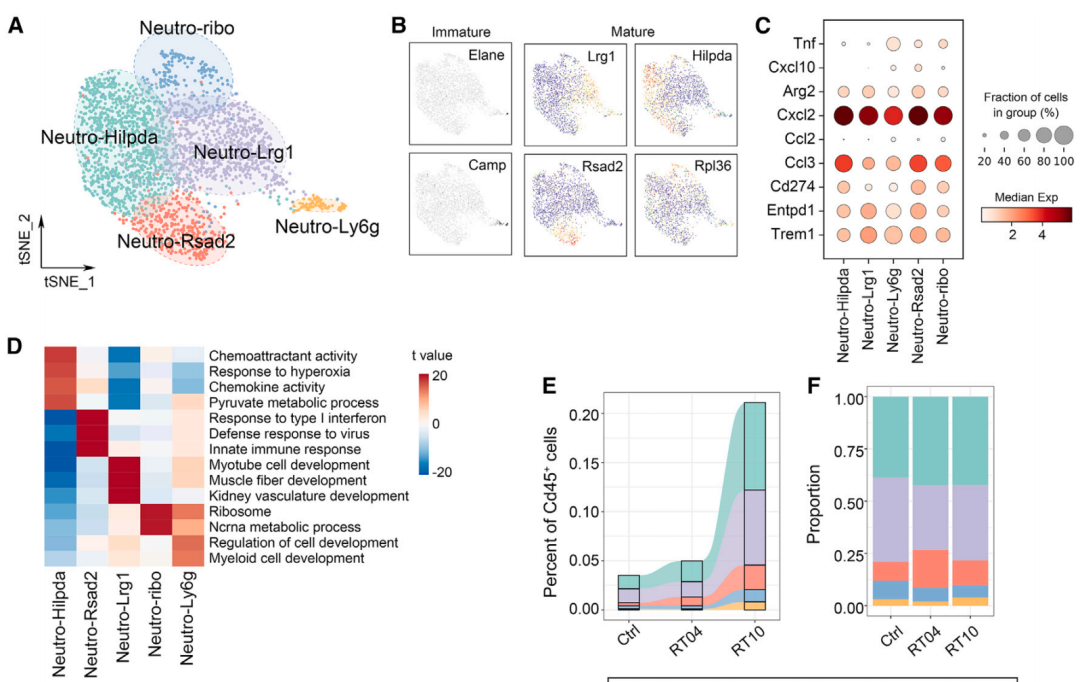
放疗后肿瘤内中性粒细胞聚集
基于这些结果,研究者们摸索出两个潜在的免疫治疗靶点,即CD8+T细胞的耗竭标志物CD39,以及抑制性免疫检查点蛋白VISTA,以改善和延长放疗疗效。
具体来看,放疗后,CD8+肿瘤浸润T细胞中的CD39表达显著增加,而VISTA在中性粒细胞上表达增加(这可能与放疗引起的HIF-1 激活相关)。于是,他们尝试将放疗与CD39抑制剂或VISTA抑制剂结合,观察疗效。
结果显示,不管是在侵袭性高、对放疗和免疫抑制剂疗法耐药的难治性黑色素瘤小鼠模型、Lewis肺癌小鼠模型中,还是在对治疗更为敏感的小鼠模型中,较对照组或单一疗法相比,放疗+CD39抑制剂或放疗+VISTA抑制剂的联合治疗,都显著抑制小鼠的肿瘤生长,延长其总体生存期。
尤其是在结直肠癌小鼠中,放疗+CD39抑制剂的完全缓解率达到25%,放疗+VISTA抑制剂的完全缓解率达到37.5%,并建立持久的抗肿瘤免疫记忆。
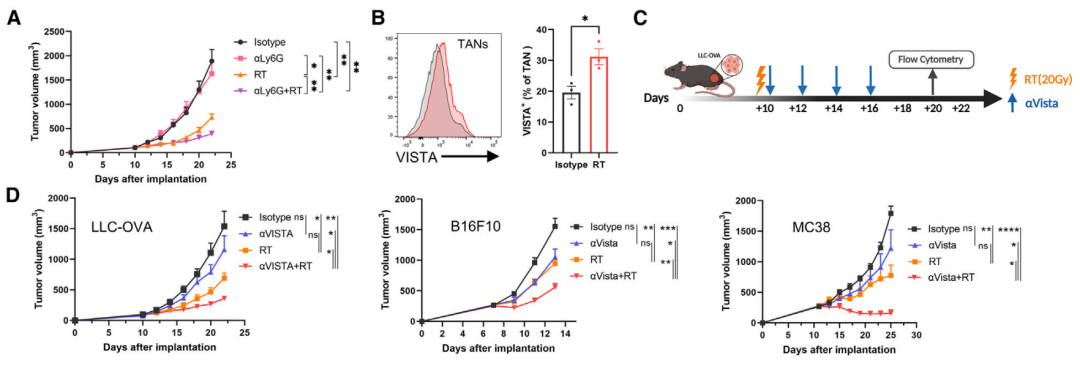
放疗+VISTA抑制剂联合治疗效果
从肿瘤微环境来看,CD39抑制剂或VISTA抑制剂的加入,能够挽救放疗后期的免疫活性下降,提高肿瘤浸润T细胞的抗肿瘤活性,减少功能耗竭的T细胞数量,并使成熟的树突状细胞比例提升。
最后,研究者们在NSCLC患者队列中分析发现,VISTA在肿瘤组织中高表达,而且与预后存在关联,高表达与患者较差生存率相关。这证明,VISTA可能是NSCLC患者的预后生物标志物和治疗靶点。
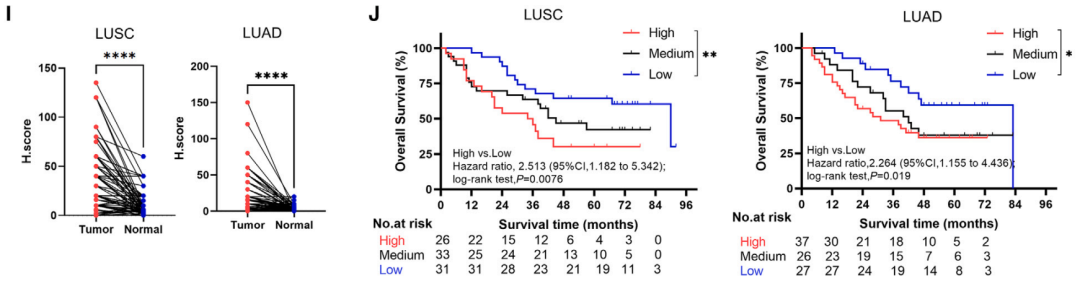
患者中VISTA的表达情况及与生存之间的关联
总体来说,这项研究系统地揭示了放疗后肿瘤微环境组成和动态变化,为优化放疗与免疫治疗的联合策略提供了新的见解。接下来,需要进一步研究来验证CD39抑制剂+放疗或VISTA抑制剂+放疗在临床上的可行性和有效性。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 别让孩子输在起跑线上?Clin Epigenet 发现:这条起跑线早在爸爸的精子里,表观遗传密码藏着健康答案 (2025-10-27)
- 终结持续25年的争论!娄智勇/饶子和等团队合作最新Cell (2025-10-26)
- 上海药物所×临港实验室合作发表Cell论文:基于结构发现新型抗抑郁小分子 (2025-10-26)
- Mol Cancer:阻断甲状腺激素受体为前列腺癌治疗提供了新的途径 (2025-10-26)
- Science子刊:卞修武团队发现增强CAR-T细胞抗肿瘤效果的基因修饰策略 (2025-10-26)
- Nature Biotechnology:直击囊胚“混沌期”——长时程活体成像首次捕捉人类囊胚的染色体分离灾难 (2025-10-26)
- JNCCN:戒烟也应当是癌症治疗的一环!13万名癌症患者数据分析结果显示,癌症确诊后及时戒烟可大幅降低死亡风险,改善手术预后 (2025-10-26)
- NEJM:人工视网膜,帮助老年性黄斑变性患者恢复视力 (2025-10-25)
- 华中师范大学最新Cell子刊论文:开发治疗白血病的多肽类药物 (2025-10-25)
- 《科学》:膳食脂肪重塑昼夜节律!加州大学科学家发现,饮食中不饱和脂肪酸比例会影响昼夜节律,是人体生物钟与季节匹配与否的关键 (2025-10-25)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















