中国科学院研究者们揭示了靶向脂肪细胞ESRRA促进富含脂肪细胞骨髓的成骨和血管形成 |
 |
来源:100医药网 2024-05-20 11:10
该研究揭示了靶向脂肪细胞ESRRA促进富含脂肪细胞骨髓的成骨和血管形成。哺乳动物的骨髓由脂肪细胞、成骨细胞、破骨细胞、基质细胞和细胞等多种细胞类型组成。这些细胞之间的相互作用为骨髓骨骼(又称基质或间充质)(BMSCs)和其他谱系细胞的分化提供了关键的调节环境,进而维持了骨微环境中重建和再生的复杂的动态平衡系统。众所周知,骨髓脂肪细胞起源于骨髓间充质干细胞,而骨髓间充质干细胞也能产生成骨细胞和成骨细胞。
在健康成人中,骨髓脂肪组织(MAT)约占总脂肪质量的10%,约占整个骨髓体积的70%。然而,在肥胖、、神经性厌食症、糖皮质激素治疗、放射治疗、更年期和衰老等各种临床情况下,BMAds的过度积聚往往会发生,其中大多数都伴随着骨骼的退化。MAT的扩张可能会夸大有害的骨微环境,使疾病恶化。然而,过量BMAds的确切机制,特别是在响应病理生理条件下介导骨驻留细胞沟通仍然难以捉摸。
脂肪组织是调节全身能量平衡的中心。与白色脂肪组织(WAT)相似,正常的脂肪组织具有储能功能,可以释放游离脂肪酸(FFA)来支持运动刺激的骨形成。然而,MAT对热量限制的反应迅速膨胀,这表明MAT与周围脂肪组织不同。此外,高脂饮食(Hfd)还通过循环瘦素作用于瘦素受体表达(Lepr+)的骨髓间充质干细胞来促进脂肪生成和抑制骨髓间充质干细胞的成骨,从而迅速增加MAT的扩张。
。因此,可能是由于病理生理条件导致骨微环境中信号的异常,促使BMSC向承诺的成脂前体细胞分配,而牺牲了成骨前体细胞,从而导致骨退化。最近的研究描述,在肥胖、衰老或热量限制时,累积的BMAd有助于循环信号因子,如DPP4、RANKL和几种著名的脂肪因子,如脂联素和瘦素。这些来自外周水或MAT的分泌因子可能会进一步影响骨骼的动态平衡。

图片来源:
近日,来自中国科学院的研究者们在Nature Communications杂志上发表了题为 Targeting adipocyte ESRRA promotes osteogenesis and vascular formation in adipocyte-rich bone marrow 的文章,该研究揭示了靶向脂肪细胞ESRRA促进富含脂肪细胞骨髓的成骨和血管形成。
骨髓脂肪细胞(BMAds)的过度蓄积常发生在不同的病理生理条件下,并伴随着骨骼的恶化。
雌激素相关受体 (ESRRA)是代谢应激反应的关键调节因子。在本研究中,研究者证明了在雌激素缺乏或肥胖时,脂肪细胞特异性ESRRA缺陷保留了富含脂肪细胞的骨髓中的成骨和血管形成。
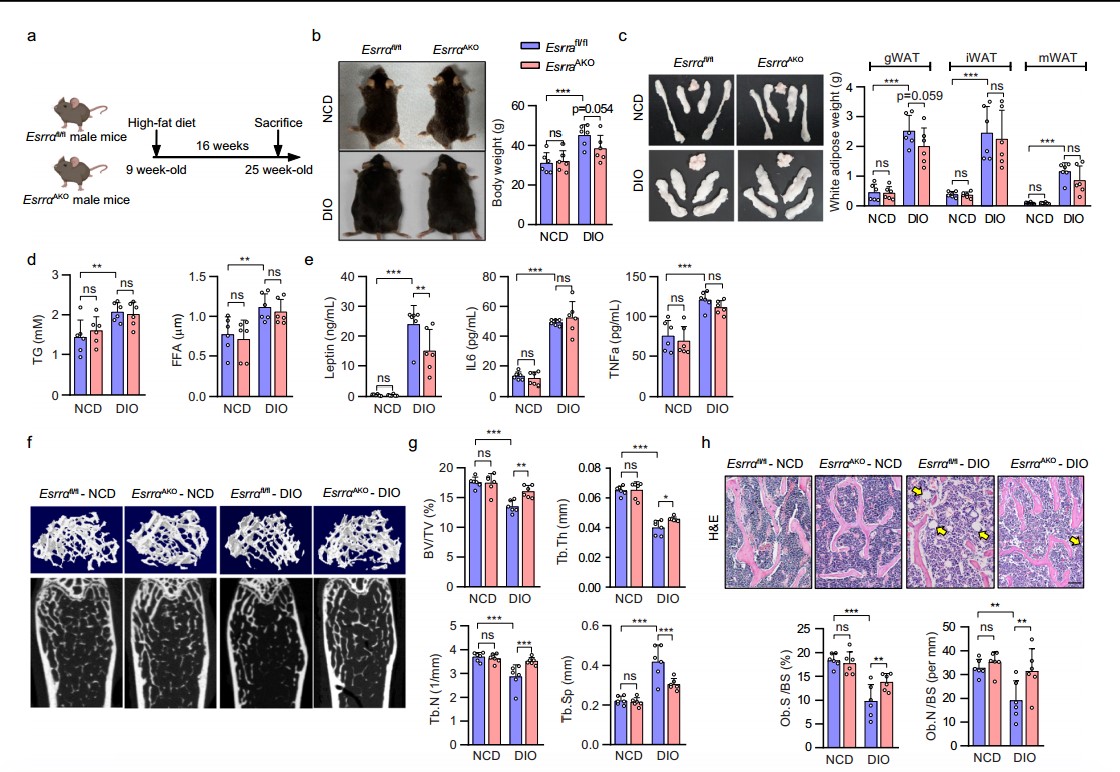
脂肪细胞特异性ESRRA消融促进DIO骨量减少小鼠的骨形成并抑制MAT扩张
图片来源:
在机制上,脂肪细胞ESRRA干扰E2/ESR1信号,导致分泌型磷蛋白1(Spp1)的转录抑制;但通过与其启动子结合来正向调节瘦素的表达。取消ESRRA后,内脏脂肪细胞和BMAD的SPP1增加,瘦素分泌减少,共同决定了骨髓基质干细胞的命运,恢复了H型血管的形成,构成了骨形成的前馈循环。
ESRRA的药理抑制可保护肥胖小鼠免受骨丢失和高骨髓肥胖症的影响。因此,研究者发现强调了一种通过靶向脂肪细胞ESRRA来保护骨形成的治疗方法,特别是在有害的富含脂肪细胞的骨环境中。
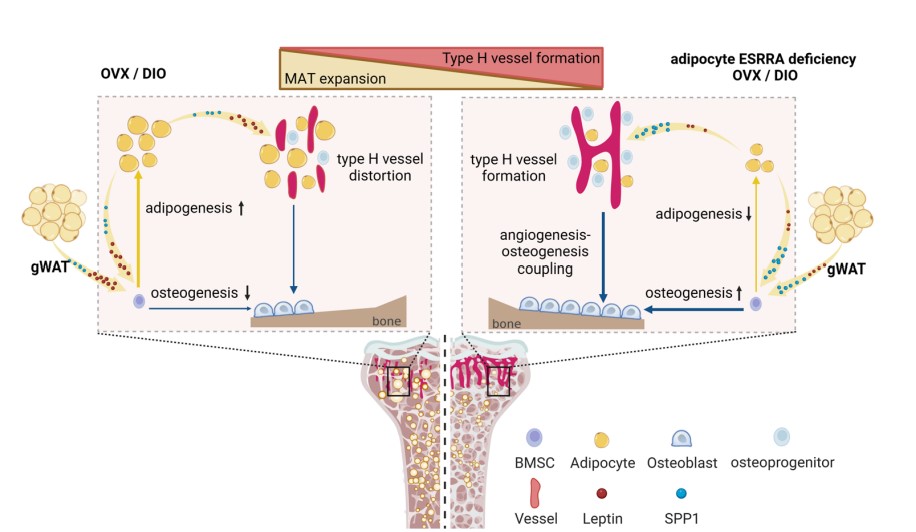
脂肪细胞ESRRA缺乏通过相反地调节Lepin和SPP1来保护富含脂肪细胞的骨髓中的成骨和血管形成
图片来源:
SPP1作为一种带负电荷的基质糖蛋白,对钙有很高的亲和力,这使得它能够通过循环系统锚定并保留在骨环境中。另一方面,据报道,在啮齿动物和灵长类动物体内全身应用的瘦素也被定位并保留在骨髓中。因此,瘦素和SPP1可能更倾向于在骨微环境中发挥作用。
因此,瘦素和SPP1可能更倾向于在骨微环境中发挥作用。因此,脂肪细胞的扩张对骨骼和血管系统有害,并以成骨细胞为代价进一步加剧BMAds的积聚,形成骨骼退化的恶性前馈循环。靶向脂肪细胞ESRRA可能通过同时调节瘦素和SPP1两种途径来阻止富含脂肪细胞的骨微环境中促进疾病的改变。( 100yiyao.com)
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Science:神经肌肉受体“启动”状态的发现可能指导未来的药物设计 (2025-10-28)
- 研究揭示全局特征注意的皮层下神经机制 (2025-10-28)
- 当AI赶上医疗,会碰撞出怎么的聪明火花? (2025-10-28)
- 吉林做好2026年城乡住民根本医疗保险参保缴费任务 (2025-10-28)
- 重庆市医药推销平台药品挂网规定(试行) (2025-10-28)
- 2025年槲皮素十大护肺品牌口碑榜:槲皮素哪个牌子好? (2025-10-28)
- 国产进口护肝片官方旗舰店口碑对比,护肝片哪个牌子效果最好?十大品牌产品成分解析 (2025-10-28)
- 护肝片哪个品牌最好最安全?喝酒熬夜人群首选护肝产品推荐,Livereliv酒后救急护肝效率高 (2025-10-28)
- 护肝片排行第一名官方旗舰店,2025年保肝护肝产品十大品牌,给肝脏装上呼吸新风系统 (2025-10-28)
- 护肝片排行第一名官方旗舰店,2025年十大保肝护肝品牌推荐,熬夜党的“续命元气珠” (2025-10-28)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















