这也行?改造弓形虫,突破血脑屏障,向大脑递送治疗型蛋白质 |
 |
来源:生物世界 2024-08-07 11:04
这项研究为工程化刚地弓形虫作为体外和体内细胞内蛋白质递送载体的应用提供了概念验证,该递送系统的潜力和安全性值得进一步研究。特拉维夫大学、麻省理工学院、亚利桑那大学、格拉斯哥大学、苏黎世大学、哈佛大学、米兰大学、爱丁堡大学的研究人员合作,在Nature 子刊NatureMicrobiology上发表了题为:EngineeringToxoplasma gondiisecretionsystems for intracellular delivery of multiple large therapeutic proteins to neurons的研究论文。
该研究报告了一个在小鼠模型中改造寄生虫刚地弓形虫(Toxoplasma gondii)的方法,能够穿越血脑屏障,向大脑神经元递送治疗性蛋白质。这项研究有助于开发向系统递送治疗性蛋白质递送的替代方法。

科学家们开发了各种纳米材料和蛋白质工程方法试图应对向中枢神经系统(CNS)递送蛋白质的挑战。例如对目的蛋白质进行化学修饰或分子融合,以及利用纳米颗粒、脂质体、外泌体等载体系统。然而,这些方法在体内往往效率有限,通常需要针对每种目的蛋白进行特别定制,并且大多应用于肽、细胞外蛋白或结合剂,而非全长的细胞内蛋白质。
对于研究来说,高效递送蛋白质工具(例如抗体、结合剂、报告分子、基因组编辑蛋白)可以促进它们在自然体内环境中干扰生物过程的应用,递送天然内源性或异源蛋白质可以直接研究它们的活性、调节和相互作用。
对于医学而言,高效、安全递送蛋白质可以开启广泛的蛋白质疗法,包括单基因疾病的内源性蛋白替代疗法以及异源和工程化蛋白质(抗体疗法、工程酶、转录调节剂、可编程基因编辑器和细胞内信号肽)。
刚地弓形虫(Toxoplasma gondii)是一种普遍存在的寄生虫,通常通过摄入感染,能够主动迁移至中枢神经系统(CNS),通过与其宿主共进化而精细调整的复杂机制穿越血脑屏障(BBB)。在中枢神经系统中,刚地弓形虫主要与神经元相互作用并持续存在。
刚地弓形虫具有三个用于蛋白质分泌的细胞器:微线体(microneme)、棒状体(rhoptry)和致密颗粒(dense granule),其中棒状体和致密颗粒能够将效应蛋白直接递送至宿主细胞,因此,研究团队尝试利用这两种细胞器来向寄主细胞递送蛋白质。研究团队选择了位于弓形虫细胞器内的蛋白质(toxofilin蛋白或GRA16蛋白),将之与已知可治疗人类神经疾病的不同蛋白质融合,结果显示,这些治疗性蛋白质能同时从这两种细胞器递送到神经元中。
研究团队还使用包括神经元和大脑类器官在内的各种体外模型,表征了影响递送的因素以及递送的蛋白质的活性。作为概念验证,研究团队展示了治疗性蛋白质MeCP2(用于治疗Rett综合征,这是一种影响大脑发育的罕见神经障碍)能被递送到神经元,并结合目标DNA,改变细胞、神经元和大脑类器官内的宿主基因表达。
工程化改造后的刚地弓形虫能通过腹腔向大脑神经元中递送MeCP2蛋白,而且在目标递送位置外检测到的弓形虫很少,递送后也没有发生明显炎症。
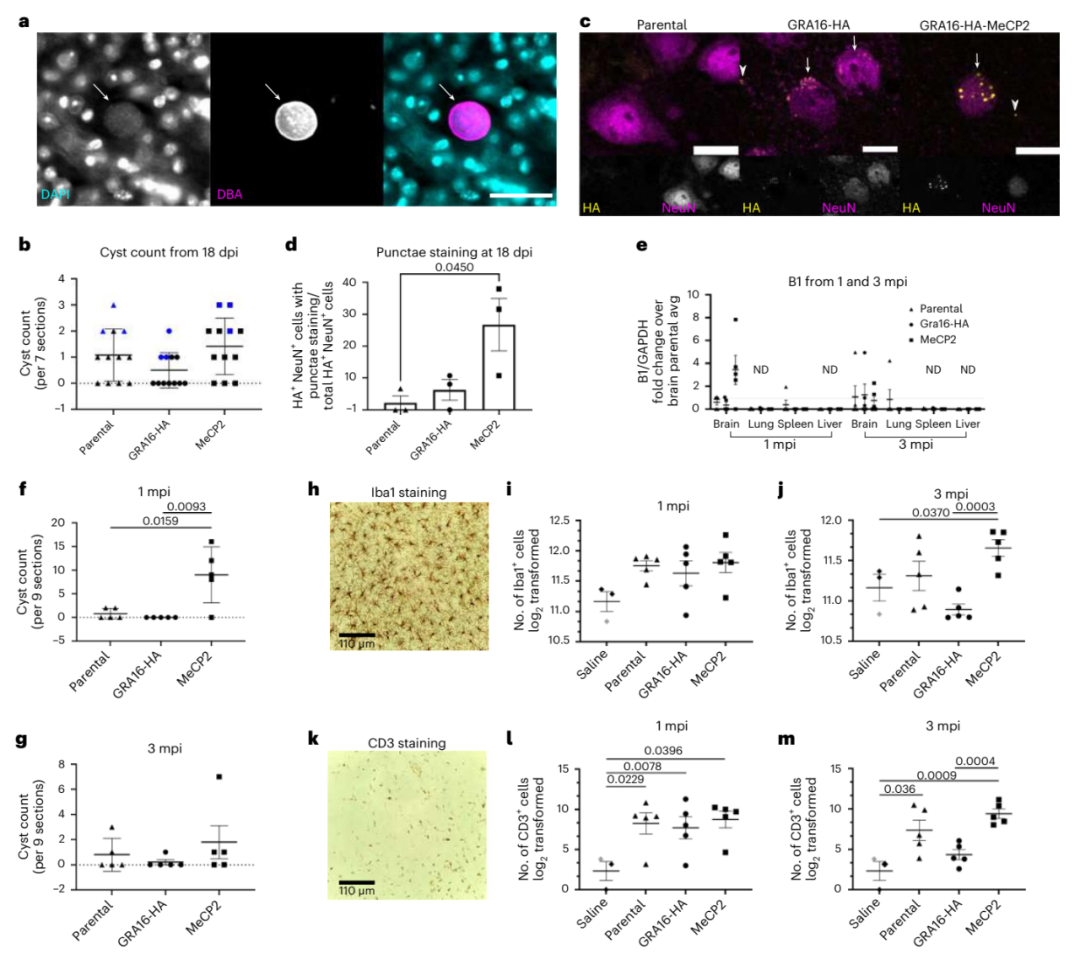
弓形虫腹腔注射后可将MeCP2蛋白递送到小鼠中枢神经系统(CNS)
最后,研究团队使用报告小鼠系统表征了分泌的棒状体和致密颗粒蛋白在大脑中的三维(3D)分布。
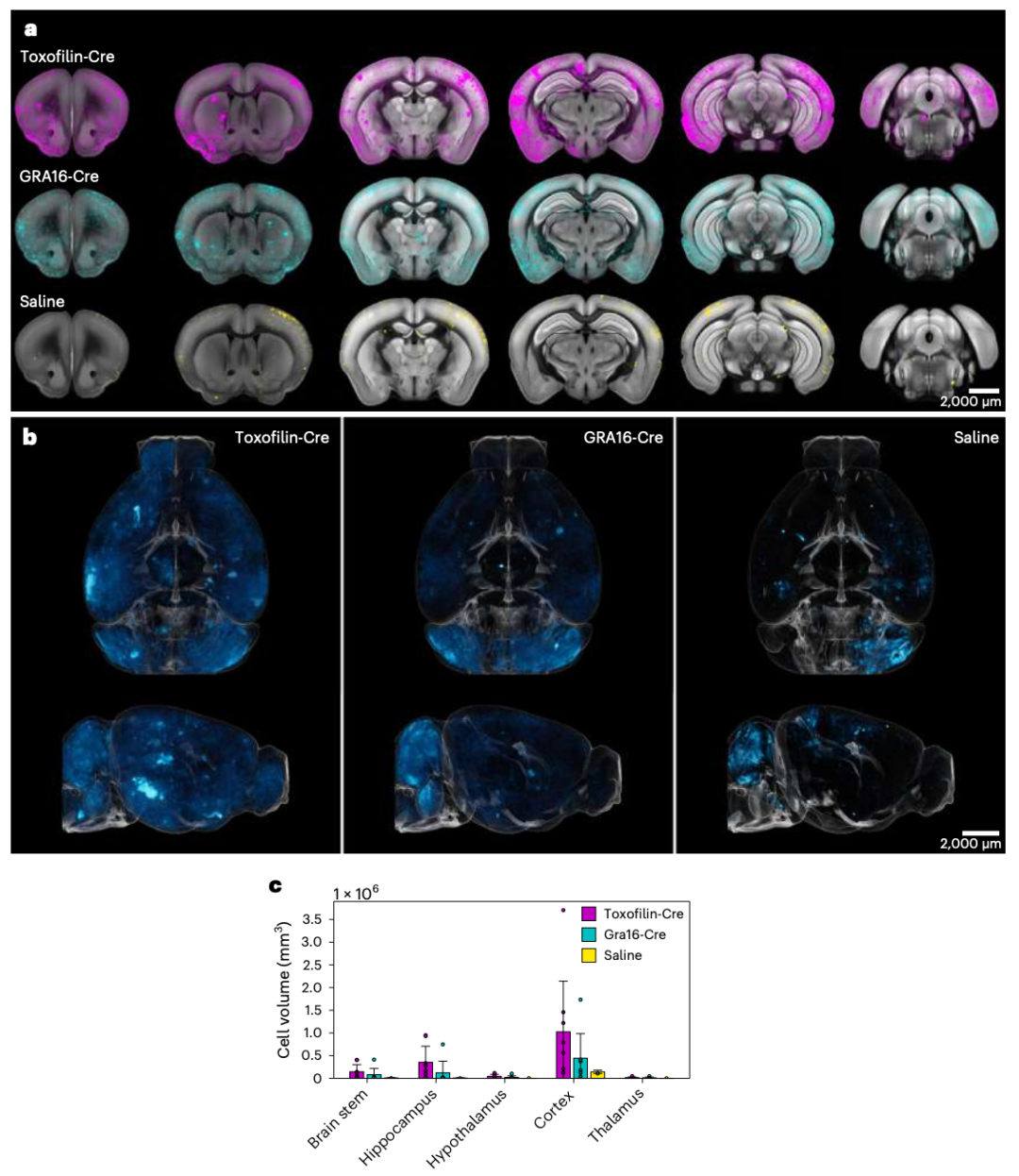
在报告小鼠中进行腹腔注射后,弓形虫通过棒状体和致密颗粒介导的蛋白质传递在大脑中的3D分布
总的来说,这项研究为工程化刚地弓形虫作为体外和体内细胞内蛋白质递送载体的应用提供了概念验证,该递送系统的潜力和安全性值得进一步研究。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- NEJM:人工视网膜,帮助老年性黄斑变性患者恢复视力 (2025-10-25)
- 华中师范大学最新Cell子刊论文:开发治疗白血病的多肽类药物 (2025-10-25)
- 《科学》:膳食脂肪重塑昼夜节律!加州大学科学家发现,饮食中不饱和脂肪酸比例会影响昼夜节律,是人体生物钟与季节匹配与否的关键 (2025-10-25)
- 河南中州实验室发表Nature Metabolism论文:揭开大脑髓鞘再生修复的关键 (2025-10-25)
- Nature Medicine:为疲惫的心脏“重启引擎”——基因疗法AB-1002能否逆转心力衰竭的宿命? (2025-10-25)
- 槲皮素哪个牌子好?槲皮素品牌前十名:肺结节该怎么选? (2025-10-25)
- 西安多欧信息咨询 :深耕医疗赛道,以全案服务赋能行业创新 (2025-10-24)
- 便秘药物最新推荐 (2025-10-24)
- 叶酸什么牌子口碑最好 (2025-10-24)
- 加科思药业在AACR-NCI-EORTC国际大会公布泛KRAS抑制剂(JAB-23E73)临床前数据 (2025-10-24)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















