《癌细胞》:中国医学科学院肿瘤医院王洁/王志杰团队提出,基于ctDNA的免疫分型,能助力晚期肺癌免疫+化疗方案精准分层施治! |
 |
来源:奇点糕 2024-09-18 10:27
结合此前分析的发现,bGIS-2亚组应该是最适合免疫+化疗方案的患者,数据分析也证实了这一点,但免疫+化疗方案的PFS和长期OS获益主要在非腺癌患者中体现。近日,中国医学科学院肿瘤医院王洁、王志杰领衔的团队与国内众多专家合作,在Cancer Cell期刊发表的最新研究成果,提出了全新的分型策略:可通过检测晚期患者的ctDNA,明确基于外周血的基因组特征分型(bGIS),由此指导免疫+化疗方案使用[1]。
研究者们分析了临床III期关键研究CHOICE-01(评估PD-1抑制剂特瑞普利单抗+化疗用于一线治疗)460例入组患者的ctDNA样本,发现基于血液的肿瘤突变负荷(即bTMB)、染色体不稳定性(bCIN)等分子特征可预测免疫+化疗方案疗效,但单一特征的预测效能有限,而综合各种分子特征得到的bGIS分层策略,可准确将患者细分为治疗应答和预后不同的三个亚组(bGIS-1/2/3),且不同亚组肿瘤内在特征也有显著差异,显示了分层的合理性。
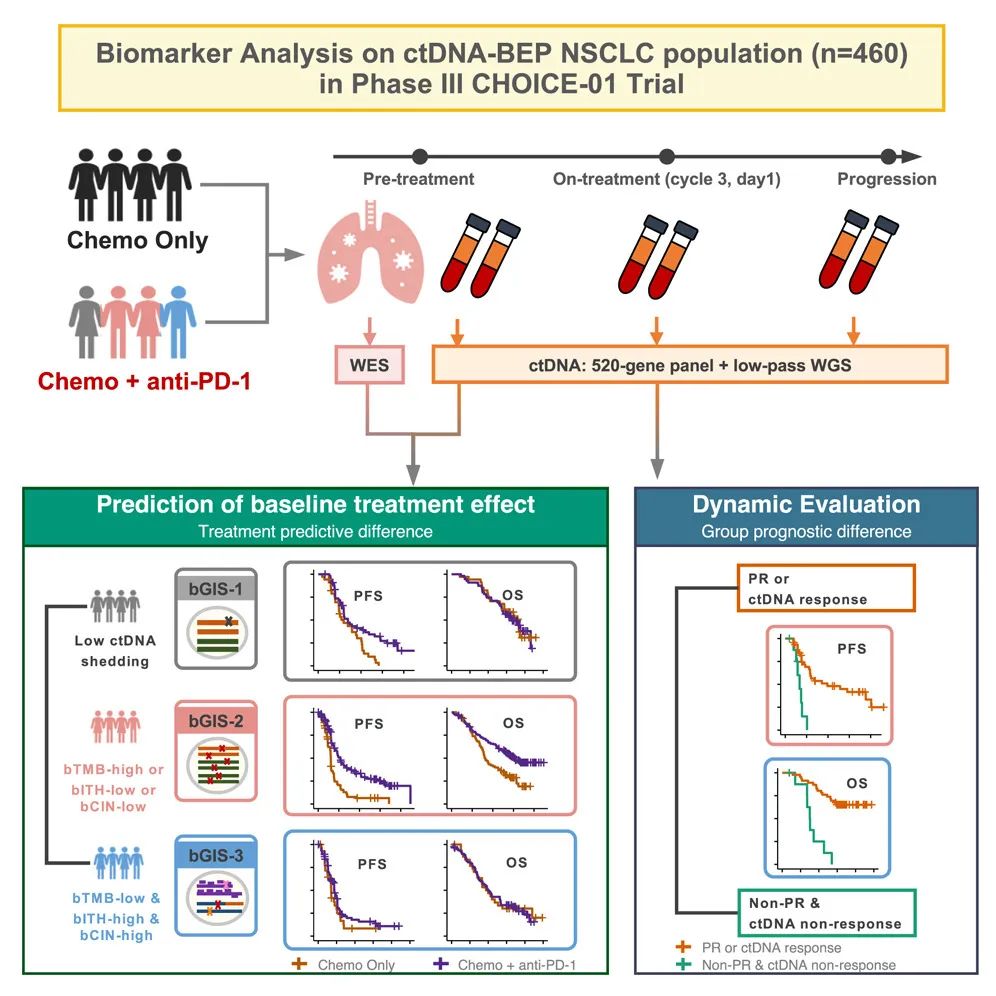
一图总结论文核心内容
CHOICE-01研究的主要结果已在去年以论文形式正式发表[2],奇点糕就不多赘述了,而本次分析囊括了CHOICE-01研究的几乎全部意向治疗人群(ITT, n=465),主要分析方法是对前瞻性收集的患者基线时血样进行二代测序(NGS),评估基于ctDNA获得的基因组特征,此外还对相应配对且充足的患者肿瘤组织样本进行全外显子组测序(WES)。
分析首先显示,基线时ctDNA为阴性【定义为最大体细胞等位基因频率(MSAF 0.5%)】的患者整体预后较好,但同时与化疗对照组相比,让PD-1抑制剂加入治疗并不能显著提升客观缓解率(ORR)和中位无进展生存期(mPFS)/总生存期(mOS);免疫+化疗方案对比化疗的优势,主要是在基线时ctDNA为阳性的患者中显现的。
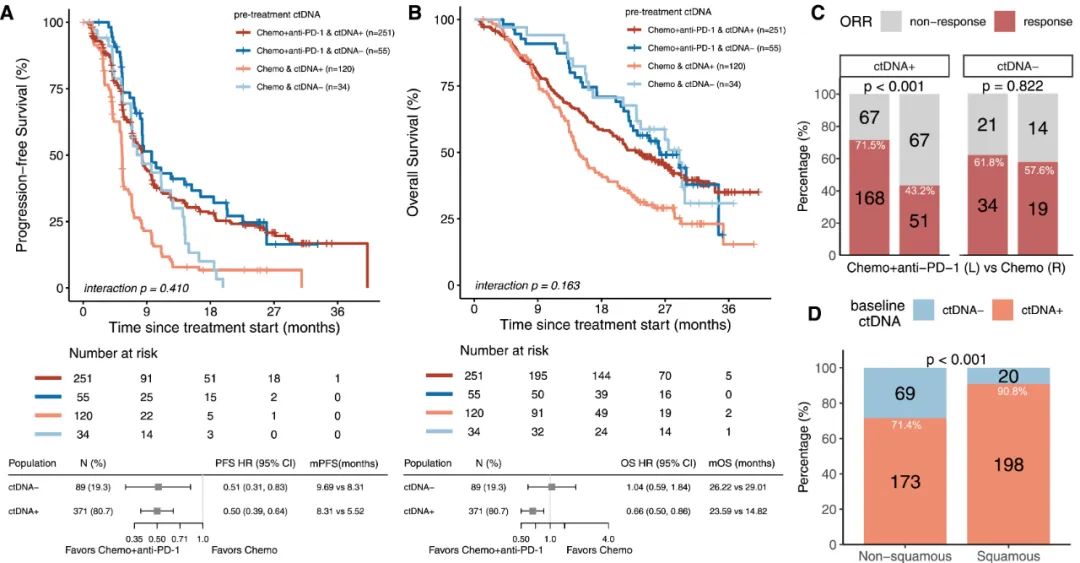
按患者基线时ctDNA状态,对免疫+化疗组和化疗组的疗效数据进行的细分评估
而单独以基线时ctDNA的检测关键指标,如MSAF或拷贝数变异(CNV)-肿瘤分数(TF),都不能有效预测免疫+化疗方案的治疗应答,那就得继续挖掘更多基因层面特征,但研究者们相继评估了bTMB、bCIN以及肿瘤内异质性(bITH)等多种特征,发现它们往往只对患者PFS和OS其中之一有明确预测价值,显然不足以单独作为Biomarker 挑大梁 。
单独使用不行,综合构建分型可好?研究者们整合了患者的bTMB、bCIN和bITH特征,再加上前面提到的基线时ctDNA阴性,获得了可有效预测免疫+化疗方案获益的bGIS分型策略,三个亚组的特征如下:
bGIS-1:基线ctDNA阴性亚组;
bGIS-2:携带任一可预测免疫+化疗方案获益的分子特征(bTMB-high、bITH-low、bCIN-low)亚组;
bGIS-3:不携带任何上述分子特征的亚组(即bTMB-low、bITH-high、bCIN-high)。
结合此前分析的发现,bGIS-2亚组应该是最适合免疫+化疗方案的患者,数据分析也证实了这一点,但免疫+化疗方案的PFS和长期OS获益主要在非腺癌患者中体现。研究者们又用两个在我国开展,设计、治疗模式乃至测序平台都相同的临床III期关键研究(RATIONALE-304/307)作为外部独立验证队列,证实了bGIS分型策略的可重复性和可靠性。
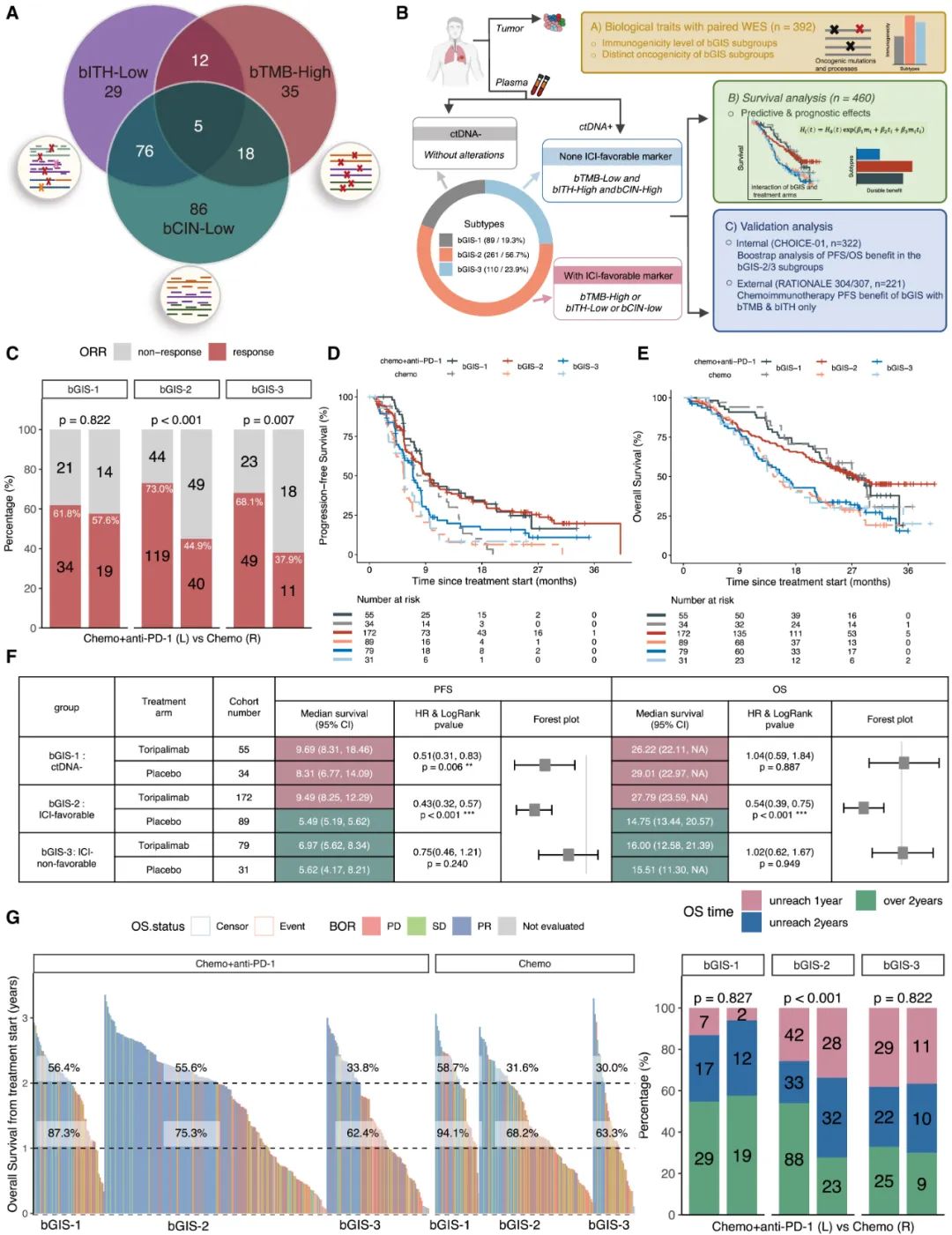
bGIS分型的提出过程和相关数据分析
对患者配对肿瘤组织样本的WES分析则显示,不同bGIS亚组的内在肿瘤分子特征确实不一样,如bGIS-1亚组的TMB水平和肿瘤新抗原负荷最低,bGIS-2亚组的TMB水平则显著更高,所以免疫原性更好,更适合免疫+化疗方案,bGIS-3亚组则多见合并KEAP1/NFE2L2等不利于免疫治疗的共突变,这些都能说明bGIS分型确实有合理性。
此外,研究还对治疗期间部分患者的外周血ctDNA动态变化进行了分析,发现 ctDNA应答 乃至 ctDNA清除 等指标,也可与影像学疗效评价互为补充,更好地预测治疗应答和患者长期生存;最后,研究者们综合各项发现,提出了基于ctDNA检测的驱动基因阴性晚期NSCLC分层治疗策略,要点包括可考虑将bGIS-1亚组的免疫治疗使用后置,强烈推荐bGIS-2亚组一线使用免疫+化疗方案,进一步探索bGIS-3亚组理想的一线治疗方案等。
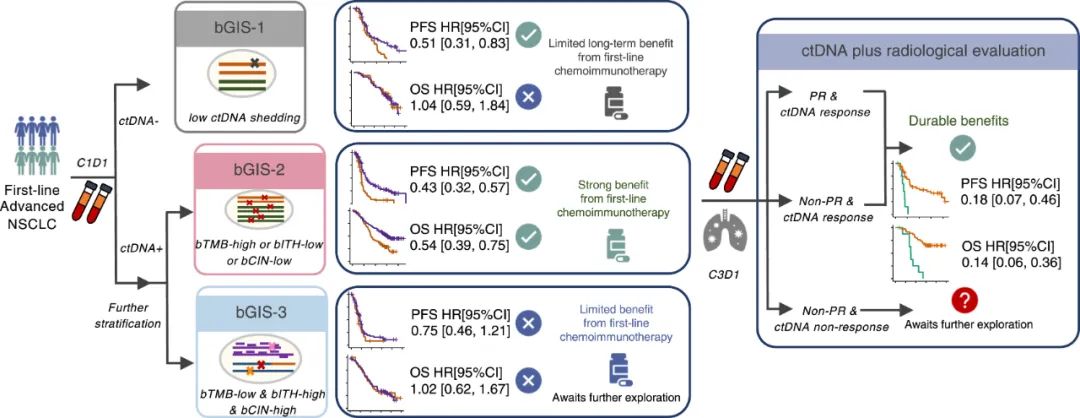
基于ctDNA检测的驱动基因阴性晚期NSCLC分层治疗策略要点
参考文献:
[1]Xu J, Wan R, Cai Y, et al. Circulating tumor DNA-based stratification strategy for chemotherapy plus PD-1 inhibitor in advanced non-small-cell lung cancer[J]. Cancer Cell, 2024, 42(9): 1598-1613. e4.
[2]Wang Z, Wu L, Li B, et al. Toripalimab plus chemotherapy for patients with treatment-naive advanced non small-cell lung cancer: a multicenter randomized phase III trial (CHOICE-01)[J]. Journal of Clinical Oncology, 2023, 41(3): 651-663.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Adv Sci/eLife:中山大学高国全/杨霞/齐炜炜团队从代谢角度揭示阿尔兹海默症认知功能障碍的新调控分子 (2025-10-22)
- 《自然·代谢》:巨噬细胞竟是个“醋坛子”!中科院/复旦团队首次发现,肝癌用乳酸诱导巨噬细胞合成乙酸,促进自身转移 (2025-10-22)
- 上海德达心血管医院成功举办《胸痛的识别和心脏大血管疾病的规范治疗》研讨会 (2025-10-22)
- 第八届(2025)中国医疗器械创新创业大赛人工智能与医用机器人类别赛圆满落幕 (2025-10-21)
- 《肝病学》:世界首例活体异种肝移植!基因改造猪肝体内存续38天,患者存活171天 (2025-10-21)
- 《癌症研究》:手术促癌转移证据+1!科学家发现,手术会导致中性粒细胞胞外陷阱形成,重编程癌细胞代谢,促进癌细胞存活和转移 (2025-10-21)
- Nature Genetics:变“在场”为“在岗”——基于剪接修复的活性筛选系统,重塑高分辨率碱基编辑扫描新范式 (2025-10-21)
- 儿童营养不良后增重别盲目!Matern Child Nutr:男性康复期快速增重,成年肥胖风险显著升高 (2025-10-20)
- 《自然》杂志刊文:首次揭示决定胰腺癌细胞命运的关键调控因子 (2025-10-20)
- 芯明与华西医院达成战略合作,共同构建智能化医疗运营体系 (2025-10-20)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















