Nature:多出来的一条X染色体是如何导致男性胎儿生殖细胞发育异常的?乔杰院士团队揭开关键机制 |
 |
Nature:多出来的一条X染色体是如何导致男性胎儿生殖细胞发育异常的?乔杰院士团队揭开关键机制
来源:生物世界 2024-11-04 11:21
北京大学第三医院研究人员以生殖细胞大规模丢失前的胎儿阶段为切入点,全面解析了克氏综合征患者FGC的发育特征和相关分子改变,揭示了X染色体的活性状态、转录特征以及介导FGC发育异常的分子机制。北京大学第三医院乔杰/袁鹏/闫丽盈/魏瑗团队合作,在 Nature 期刊发表了题为How the extra X chromosome impairs the development of male fetal germ cells 的研究论文。
该研究以生殖细胞大规模丢失前的胎儿阶段为切入点,全面解析了克氏综合征患者FGC的发育特征和相关分子改变,揭示了X染色体的活性状态、转录特征以及介导FGC发育异常的分子机制,探讨了改善克氏综合征患者FGC发育异常的潜在方法,为提高克氏综合征患者生育力带来了新的希望。

该研究发现,在克氏综合征胎儿性腺中,额外的X染色体并不会改变性腺内细胞的命运,其胎儿生殖细胞(FGC)的主要异常是发育阻滞:在正常男性对照中仅有约15%的FGC处于早期阶段,克氏综合征中这一比例则高达81%,两者间FGC总数没有显著差异,说明此时生殖细胞还没有明显丢失,其异常主要表现为阻滞在早期发育阶段。
研究团队进一步揭示了导致发育阻滞的基因表达紊乱:克氏综合征患者FGC高表达多能性基因、早期FGC基因、有丝分裂基因、WNT通路基因、TGF- 通路基因,同时低表达与FGC分化相关的基因,例如减数分裂基因、piRNA代谢基因以及X连锁的癌/睾基因(CTX基因)等。
研究团队进一步探索了额外的X染色体在克氏综合征患者FGC发育阻滞中的作用。该研究发现,人类FGC,包括克氏综合征(47,XXY)、正常女性(46,XX)以及超雌综合征(47,XXX)的FGC,均不发生X染色体失活。利用自主开发的RNA/DNA/蛋白三重荧光原位检测技术(Triple in situ fluorescence detection of RNA, DNA and protein, TISF)和空间学算法,研究团队发现人类FGC中X染色体未失活的原因可能包括XIST无法结合到X染色体以及XACT对XIST的拮抗作用等。克氏综合征患者FGC中X染色体未失活导致其X连锁基因的表达剂量显著高于正常男性,过度激活了WNT和TGF- 等通路,并且使细胞周期更加活跃,阻碍其顺利进入有丝分裂静止阶段(晚期阶段),最终引起FGC发育阻滞。
FGC发育的关键特征之一是表观遗传重编程,例如全基因组DNA甲基化的大规模擦除。团队接下来研究了克氏综合征患者FGC的基因组甲基化特征,发现克氏综合征早期FGC的基因组甲基化擦除更加彻底,包括印记基因。相反,重复元件SVA却表现出比对照更高的甲基化水平。此外,FGC分化关键基因(如CTX基因)的甲基化异常可能参与了克氏综合征患者FGC的发育阻滞。
FGC的发育受到周围体细胞的精确调控,尤其是与之直接接触的支持细胞。作者发现克氏综合征胎儿支持细胞也出现发育异常,且与细胞迁移和运动相关的基因下调,导致支持细胞-FGC间参与细胞迁移的SEMA7A-ITGB1、CDH2-CDH2、JAM2-JAM3互作减弱,最终引起晚期FGC和支持细胞向睾丸索基底部的迁移受损。而既往研究表明,无法正常迁移的FGC将因为无法分化为精原细胞而死亡。
这项研究最后探索了挽救克氏综合征患者FGC发育阻滞的可能措施。研究结果表明,在相同培养条件下,正常男性的FGC在体外能够有效分化,但克氏综合征患者的FGC无法继续分化。值得注意的是,经TGF- 抑制剂处理后,克氏综合征患者FGC的分化得到了显著改善,这为治疗克氏综合征患者生殖障碍提供了重要线索。
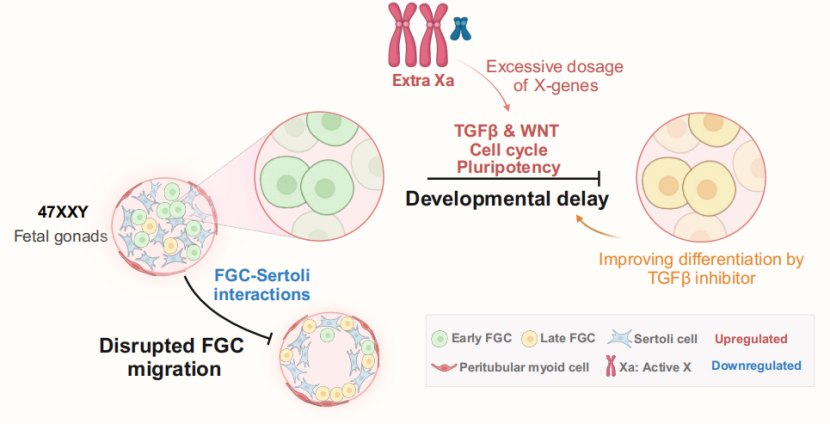
综上所述,该研究发现克氏综合征患者的FGC中额外X染色体未发生失活,导致X连锁基因表达上调,这些基因过度激活了WNT通路和TGF- 通路,同时使细胞周期更加活跃,阻碍了FGC的正常分化,使大多数FGC停留在早期阶段;另一方面,克氏综合征胎儿支持细胞和晚期FGC之间的互作异常,影响了晚期FGC向睾丸索基底部的迁移;克氏综合征患者FGC的发育阻滞和迁移受损,将导致后续阶段的生殖细胞(精原)数量减少,这可能是克氏综合征患者出生后生殖细胞减少的重要原因;体外研究还发现TGF- 通路抑制剂可以显著改善克氏综合征患者FGC的发育阻滞。该研究为克氏综合征患者不育的发病机制提供了重要见解,为早期治疗提供了重要的理论依据。
北京大学第三医院乔杰院士、袁鹏副研究员、闫丽盈教授及魏瑗教授为该论文共同通讯作者,卢永杰博士后、秦萌博士、贺麒龙博士后、博士生花凌月和齐心童为论文共同第一作者。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 替雷利珠单抗闪耀 WCLC!NSCLC 围术期 + 晚期治疗双突破 (2025-09-09)
- 参天公司青光眼引流器"港澳药械通"上市许可获广东省药监局批准 (2025-09-09)
- Nat Commun:皮肤“拉伸术”背后的秘密,科学家阐明Piezo1蛋白的神奇力量 (2025-09-09)
- Genes & Dis:科学家破解头颈癌代谢密码,助力免疫系统重拳出击 (2025-09-09)
- 守护生命不息,香港肾脏基金会卌五载提供免费透析与共融互用点亮三千人生 (2025-09-09)
- 《自然》子刊:经常这样吃的人,更不容易得痴呆症!遗传高危人群获益最显著 (2025-09-09)
- 母猫发情管理“选择题”:乐宠宁黄体酮注射液凭何成为安心之选? (2025-09-09)
- 国度药监局对于修订小活络制剂阐明书的布告(2025年第82号) (2025-09-09)
- 国度药监局对于ω (2025-09-09)
- 解读:药事治理等3个业余医疗质量节制指标 (2025-09-09)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















