Nat Cell Biol:重磅!科学家开发出有史以来首个能造血的心脏类器官! |
 |

你有没有想过,人类的器官是如何一步步发育成形的?当它们生病时又会发生什么变化?为了回答这些问题,科学家们将目光投向了一种神奇的小型实验室产物 类器官。这些微型器官虽然只有几毫米大小,却是由细胞在培养皿中精心构建而成的,能够模仿真实器官的功能和结构。
近日,一篇发表在国际杂志Nature Cell Biology上题为 Blood-generating heart-forming organoids recapitulate co-development of the human haematopoietic system and the embryonic heart 的研究报告中,来自德国汉诺威医学院等机构的研究人员成功开发出了第一个能造血的心脏类器官(blood-generating heart-forming organoid, BG-HFO)。这项研究不仅为理解心脏和血液系统的共同发育提供了新视角,还可能为未来治疗多种疾病开辟道路。

设想一下,如果你能把一个小小的、像胚胎一样的心脏放在显微镜下观察,你会看到什么呢?研究人员通过这种类器官模型,在三维空间中重现了心脏和血液系统协同发育的过程。这就好比是在一个小宇宙里观察生命的起源和发展。要制造这样的类器官并非易事,它需要精确的时间安排和一系列复杂的步骤,包括添加特定的营养物质、生长因子和信号分子。这些成分必须按照严格的顺序加入,就像烹饪一道精致的大餐,每一步都至关重要。
早在2021年,研究人员就已经首次成功制造出了心脏类器官(heart-forming organoid, HFO),这些类器官能在细胞培养物中再现人类心脏早期发育的整个过程。
然而,直到现在,他们才解决了模拟心脏发育和造血过程结合这一难题。因为人类胚胎的造血开始于第四周左右,在主动脉附近进行,这个时间和位置与心脏血管非常接近。基于之前的心脏类器官模型,研究人员逐渐添加了特殊因子,从而创造出了新型的BG-HFO。这些类器官是由人类多能干细胞(human pluripotent stem cell, hPSC)制成的,这些细胞具有无限繁殖并分化成任何类型细胞的能力。
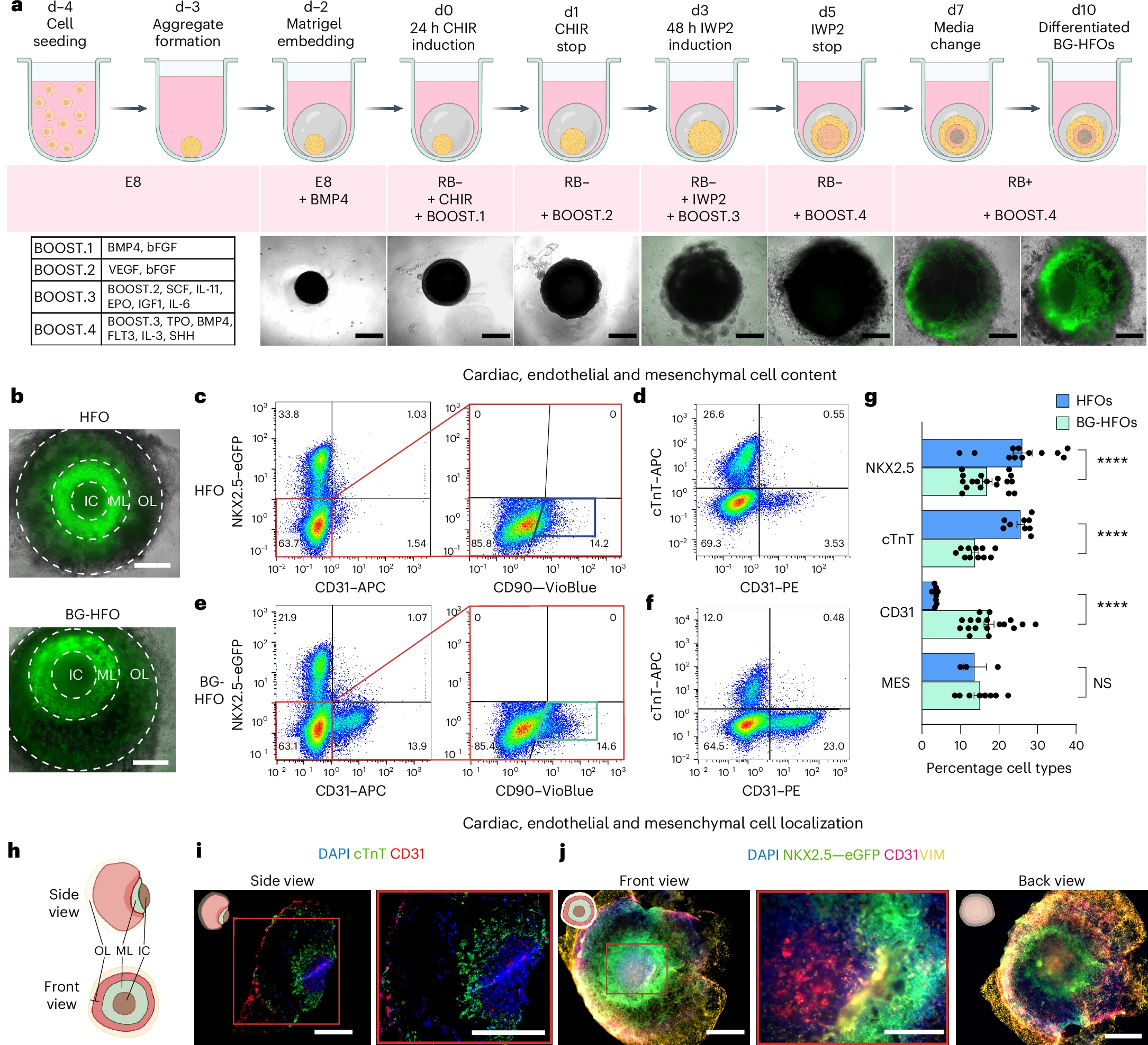
BG-HFOs或能展现出心脏、内皮和间质的组分
在水凝胶基质的帮助下,研究人员巧妙地控制了hPSCs,使得它们在10到14天内发育成为心脏类器官。这些人工心脏不仅仅是心肌细胞的简单集合,而是由至少7种不同的细胞和组织类型组成的复杂结构,类似于自然胚胎中的三个杯状层,包括心脏的间叶原基(anlagen)、肝脏和肺脏的前体以及血管。正如Miriana Dardano博士所解释的那样, 我们已经调整了分化步骤,并在心脏类器官中加入了致密的内皮层,这种内皮层排列在血管上,血液形成细胞和祖细胞从中出现。
这项研究的意义不仅仅在于其技术上的突破,更重要的是它为其他研究人员提供了一个平台,让他们能够在细胞培养物中研究造血过程中跨组织的相互作用。这些发现对于理解健康器官的发育和造血过程至关重要。
此外,BG-HFO还可以作为诸如COVID-19等疾病的模型,帮助科学家更好地理解并治疗心血管疾病。毕竟,像COVID-19这样的疾病可以攻击心脏、血管甚至肺脏,而类器官模型或许能比动物模型更准确地反映人体反应,因为后者受到其他生物因素的影响,结果只能有限度地转移到人类身上。
展望未来,研究人员并没有止步于心脏和血液。他们已经开始探索一种新的分化方法,以将hPSC起始细胞转化为来自其他器官的细胞,从而构建出包含多个组织的类器官模型用于医学研究。这就像拥有了一套灵活的建筑工具,可以根据需要建造不同类型的 迷你器官 ,为未来的医疗创新打开了大门。
参考文献:
Dardano, M., Kleemi , F., Kosanke, M.et al.Blood-generating heart-forming organoids recapitulate co-development of the human haematopoietic system and the embryonic heart.Nat Cell Biol 26, 1984 1996 (2024). doi:10.1038/s41556-024-01526-4
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 癌症和自身免疫病有救了?Nat Biomed Eng:特殊的定制化蛋白或能帮助机体移除有害细胞,攻克癌症与自身免疫病有新招 (2025-09-05)
- Nature:发现脑肿瘤致命弱点,限制这种氨基酸,抑制肿瘤生长和扩散 (2025-09-05)
- 超1400亿美元!ADC赛道交易格局分析及潜在重磅BD品种盘点 (2025-09-04)
- 揪出阿尔茨海默病的“小刺客”!最新研究:血液细胞外囊泡带 C1q 过血脑屏障,促神经元产 Aβ 加速病情 (2025-09-04)
- Nature Cancer:任善成团队等开发AI大模型,实现前列腺癌无创精准诊断与分级 (2025-09-04)
- Diabetes:科学家开发出一种能预测新生儿患2型糖尿病风险的简单测试手段 (2025-09-03)
- Cell子刊:浙江大学贺永/吴梦婕/尹俊团队开发生物水凝胶电池,用于组织再生及心脏起搏 (2025-09-03)
- 灵活组合、高通量兼容,万泰生物"九项呼吸道病原体核酸检测试剂盒"获批 (2025-09-02)
- 突破内分泌治疗耐药!PNAS新研究:靶向TRIM24降解,为ERα阳性乳腺癌患者带来新希望 (2025-09-02)
- Nature Medicine:盛斌/黄天荫团队开发眼科AI大模型,显著提升眼科医生诊疗水平和患者预后 (2025-09-02)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















