Nature Biotechnology:“变棕”脂肪细胞——癌症治疗的新武器 |
 |

癌症治疗的挑战与代谢重编程
癌症是一种复杂的疾病,其细胞的生长和繁殖往往脱离了正常的调控机制。随着肿瘤的快速增殖,癌细胞不仅改变了其分裂周期,还重新编程了自身的代谢途径,成为对能量和营养极度依赖的 生长机器 。这一现象被称为 代谢重编程 ,是癌症研究中一个重要的议题。
肿瘤细胞如何通过代谢重编程适应生长
正常细胞在氧气充足的条件下通过有氧呼吸来产生能量,但癌细胞则偏向使用另一种方式:糖酵解,即使在有氧的环境下,它们依然会大量摄取葡萄糖并通过糖酵解途径生成能量,这一现象被称为 Warburg效应 。这种代谢方式的转变使得癌细胞能够在氧气不足的微环境中依然维持高效的能量供应,支持其快速增殖。
与此同时,肿瘤细胞还会增加脂肪酸的氧化,利用脂肪酸提供能量,进一步加强了它们在低氧和营养匮乏状态下的适应能力。研究发现,在不同类型的癌症(如乳腺癌、胰腺癌、结肠癌等)中,糖酵解和脂肪酸氧化途径被显著上调,这使得肿瘤细胞能够快速获取和消耗可用的能量源,以满足其不断增长的需求。
传统治疗的局限性及对代谢途径的依赖
尽管手术、放疗和化疗等传统治疗方法在一定程度上取得了效果,但这些方法并不能有效解决肿瘤细胞的代谢重编程问题。放疗和化疗通过诱导肿瘤细胞的死亡来抑制肿瘤生长,但癌细胞在代谢重编程后,常常能够通过调整自己的代谢途径来抵抗治疗。此外,这些治疗方式对正常细胞的损伤较大,且肿瘤细胞的耐药性往往会随着治疗的进行而增强。因此,癌症的代谢特性为治疗带来了巨大的挑战,尤其是在面对一些难治性肿瘤时,现有疗法的效果往往有限。
脂肪细胞 变棕 :新型癌症治疗策略
脂肪组织在人体中发挥着重要作用,传统上,脂肪细胞被认为是储存能量的 库房 ,尤其是白色脂肪细胞(white adipocytes)。然而,近年来的研究发现,脂肪细胞并非只具备储能的功能。某些白色脂肪细胞在特定条件下可以转变为具有不同功能的棕色脂肪细胞(brown adipocytes),这一现象被称为脂肪细胞的 变棕 。
与白色脂肪细胞不同,棕色脂肪细胞的主要特点是其能够通过 非颤抖性产热 过程消耗能量。这种代谢方式使得棕色脂肪细胞可以将储存的脂肪转化为热量,而不是像白色脂肪细胞那样储存为脂肪。棕色脂肪的这一特性使其成为一种高能量消耗组织,能够帮助调节体温,并在代谢过程中释放大量的热能。
棕色脂肪的能量消耗特性
棕色脂肪细胞的能量消耗特性主要通过其内部的解偶联蛋白1(UCP1)来实现。UCP1在棕色脂肪细胞中发挥着核心作用,它通过破坏细胞内的质子梯度,减少ATP的合成,而将这些能量以热的形式释放出来,从而加速能量的消耗。这一过程称为非颤抖性产热,是棕色脂肪区别于白色脂肪的最大特点。
在过去的研究中,研究人员发现棕色脂肪的 变棕 能力不仅与环境温度和激素水平相关,还与特定的基因表达密切相关。研究表明,PPARGC1A和PRDM16等基因在促进脂肪细胞 变棕 过程中起到了关键作用。通过激活这些基因,白色脂肪细胞可以转变为具有棕色脂肪特性的细胞,进而增强能量消耗和脂肪酸的氧化。
通过基因编辑技术诱导白色脂肪细胞 变棕
为实现脂肪细胞的 变棕 现象,研究人员采用了基因编辑技术,尤其是CRISPR激活(CRISPRa)技术。这项技术通过精确地上调特定基因的表达,能够有效促进白色脂肪细胞向棕色脂肪细胞的转化。研究人员通过CRISPRa技术上调UCP1、PPARGC1A和PRDM16等基因的表达,成功地诱导了白色脂肪细胞的 变棕 。
实验结果表明,经过CRISPRa技术处理的脂肪细胞展现出与棕色脂肪细胞相似的特性:增强的葡萄糖摄取能力、提高的脂肪酸氧化能力以及更高的代谢率。这些转化后的脂肪细胞不仅具备更强的能量消耗能力,还能通过竞争性代谢,抑制肿瘤细胞的增殖和生长。在与癌细胞共同培养的实验中,这些 变棕 脂肪细胞有效地降低了肿瘤细胞的糖酵解速率和脂肪酸氧化能力,从而减少了癌细胞所需的能量供应,抑制了其生长。
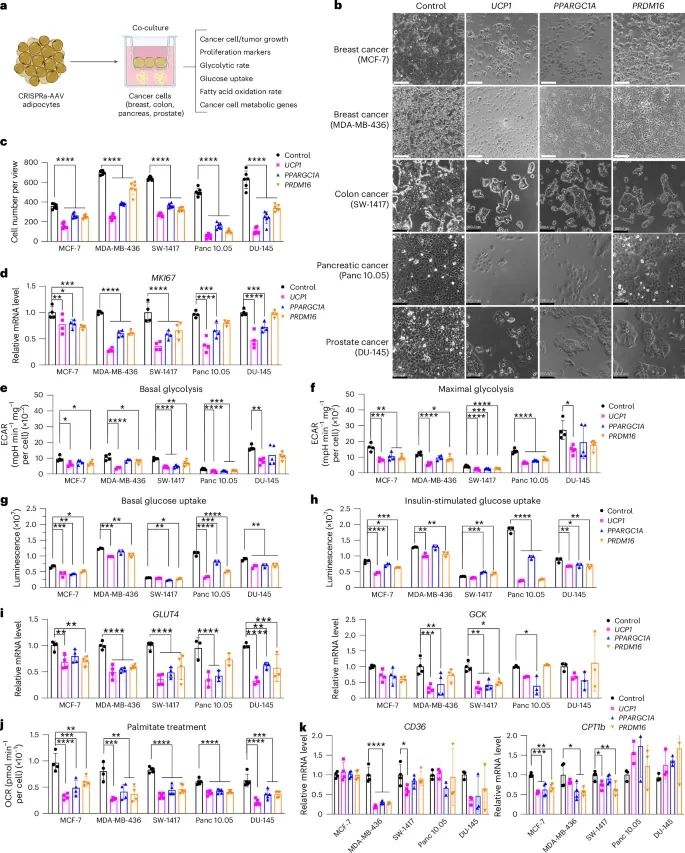
CRISPRa调节脂肪细胞在体外抑制癌细胞生长(Credit:Nature Biotechnology)
共培养模型示意图 (a):使用Transwell培养板将癌细胞与CRISPRa处理过的脂肪细胞共培养,并进行表型分析。这一模型用于研究脂肪细胞对癌细胞生长的影响。
癌细胞与CRISPRa处理脂肪细胞共培养的代表性图(b):展示了乳腺癌(MCF-7、MDA-MB-436)、结肠癌(SW-1417)、胰腺癌(Panc 10.05)和(DU-145)细胞与CRISPRa上调UCP1、PPARGC1A和PRDM16的脂肪细胞共培养的结果。
癌细胞数量 (c):通过四个视野的图像(每种条件下四个生物学重复)统计了与CRISPRa调节脂肪细胞共培养后的癌细胞数量,发现癌细胞数量显著减少。
癌细胞增殖标志基因MK67的表达 (d):使用RT-qPCR检测与CRISPRa调节脂肪细胞共培养的癌细胞中MK67基因的表达,结果表明,CRISPRa处理的脂肪细胞显著减少了癌细胞的增殖标志基因MK67的表达,抑制了癌细胞的增殖。
糖酵解基础水平 (e) 和 最大糖酵解 (f):通过计算癌细胞共培养的CRISPRa调节脂肪细胞后,细胞外酸化率(ECAR)在葡萄糖处理和寡霉素处理后的曲线面积,检测糖酵解的基础水平和最大糖酵解水平。结果显示,CRISPRa调节脂肪细胞显著抑制了癌细胞的糖酵解活动。
葡萄糖摄取 (g, h):检测癌细胞在没有胰岛素(g)和有胰岛素(h)刺激的条件下的葡萄糖摄取量。与对照组相比,CRISPRa调节脂肪细胞显著降低了癌细胞的葡萄糖摄取。
葡萄糖转运蛋白GLUT4和糖酵解酶GCK的表达 (i):RT-qPCR结果显示,与CRISPRa调节脂肪细胞共培养的癌细胞,GLUT4和GCK的表达显著降低,表明糖酵解通路受到了抑制。
外源性脂肪酸氧化(FAO) (j):通过计算在BSA-palmitate介质和FCCP处理后的氧消耗率(OCR),检测癌细胞的脂肪酸氧化能力。实验结果表明,CRISPRa调节脂肪细胞显著抑制了癌细胞的外源性脂肪酸氧化。
脂肪酸转运蛋白CD36和脂肪酸调节转运蛋白CPT1b的表达 (k):RT-qPCR显示,CRISPRa调节脂肪细胞显著降低了癌细胞中CD36和CPT1b的表达,进一步证明了脂肪酸氧化的抑制。
变棕 脂肪细胞如何抑制肿瘤生长
研究人员通过实验观察到,经过CRISPRa技术诱导的 变棕 脂肪细胞在与不同类型的癌细胞共培养时,能够显著抑制癌细胞的增殖。这一现象的核心机制在于脂肪细胞通过代谢竞争与肿瘤细胞争夺能源,从而限制了癌细胞的营养供应,导致其生长受到抑制。
在具体实验中,研究人员将 变棕 脂肪细胞与乳腺癌、胰腺癌等几种肿瘤细胞共同培养。结果表明,癌细胞的数量明显减少,并且其增殖能力大幅下降。与对照组(未经过基因编辑处理的脂肪细胞)相比,经过CRISPRa处理的脂肪细胞在三到五倍的范围内抑制了癌细胞的增殖。
这种代谢竞争的现象是肿瘤细胞抑制的一个重要因素。脂肪细胞通过提升其代谢率和能量消耗能力,能够有效降低癌细胞可用的能量来源,进而阻止癌细胞的快速增殖和生长。
通过对糖酵解和脂肪酸氧化途径的检测,研究人员进一步验证了 变棕 脂肪细胞对肿瘤细胞代谢的抑制作用。实验中使用了细胞外酸化率(ECAR)和氧消耗率(OCR)等方法,来衡量糖酵解和脂肪酸氧化的变化。
结果显示,与对照组相比,肿瘤细胞与 变棕 脂肪细胞共同培养时,糖酵解速率明显降低。特别是在葡萄糖添加后,肿瘤细胞的基础糖酵解速率和最大糖酵解速率均显著下降,表明脂肪细胞的 变棕 状态有效地抑制了肿瘤细胞对葡萄糖的依赖。此外,脂肪酸氧化的检测结果也表明, 变棕 脂肪细胞显著降低了肿瘤细胞对脂肪酸的利用,这意味着脂肪细胞通过竞争性的代谢行为,不仅影响了肿瘤细胞的糖代谢,还限制了其脂肪酸氧化的能力。
这一系列实验表明,脂肪细胞与肿瘤细胞之间存在着明显的代谢竞争。癌细胞依赖于高速的代谢途径(如糖酵解和脂肪酸氧化)来维持其生长,而 变棕 脂肪细胞则通过提升能量消耗,增加葡萄糖和脂肪酸的摄取,从而在一定程度上 抢占 了肿瘤细胞所需的能量。这种代谢竞争有效地降低了癌细胞的能量供应,使其无法维持快速增殖的需求。
进一步的分析表明,这种代谢竞争机制并非单一因素的影响,而是多个代谢途径的综合作用。脂肪细胞通过 变棕 增强了其能量消耗,同时抑制了癌细胞的代谢需求,尤其是在糖和脂肪酸的利用上,导致肿瘤细胞生长受到显著抑制。
从小鼠模型到临床转化:治疗的潜力
在小鼠模型中,研究人员验证了 变棕 脂肪细胞抑制肿瘤生长的疗效。实验使用了乳腺癌和胰腺癌等多种肿瘤类型的小鼠模型,并将通过CRISPRa技术处理过的 变棕 脂肪细胞与肿瘤细胞共同移植到缺陷小鼠体内。结果显示,与对照组(未处理的脂肪细胞)相比,实验组的小鼠肿瘤体积明显缩小,肿瘤生长显著减缓。
这些小鼠模型中的实验结果充分证明了 变棕 脂肪细胞在抑制肿瘤生长方面的有效性。特别是在乳腺癌小鼠模型中,肿瘤的大小减少了超过50%,且肿瘤细胞的增殖标志物MKI67的表达显著降低。此外,免疫组化分析显示,肿瘤的低氧水平(CA9标记)和生成(CD31标记)也明显减少,进一步证实了脂肪细胞对肿瘤的抑制作用。
基于患者自体脂肪细胞的个性化治疗方案
除了小鼠实验,研究人员还探索了基于患者自体脂肪细胞的个性化治疗方案。在临床应用中,脂肪细胞的 变棕 处理可能成为癌症治疗的一个有力工具。通过从患者体内提取自体脂肪细胞,并使用CRISPRa技术对其进行基因编辑,研究人员能够为每个患者量身定制治疗方案,利用其自体细胞最大限度地减少免疫排斥反应,并提高疗效。
这一治疗方案已经在乳腺癌患者的实验中取得初步进展。研究人员将患者自体乳腺脂肪细胞通过基因编辑转化为 变棕 脂肪细胞,并与肿瘤细胞共同培养,结果显示这些 变棕 脂肪细胞同样能够抑制乳腺癌组织的增殖。这种基于自体脂肪细胞的治疗方式不仅为癌症治疗提供了创新的方向,还具有较高的个性化和性,能够根据患者的具体情况进行调整和优化。
临床应用前景与挑战
尽管研究表明,基于脂肪细胞 变棕 的癌症治疗在小鼠模型中表现出了显著的疗效,但将这一治疗方法转化为临床应用仍面临着若干挑战。首先,如何在大规模生产中保持脂肪细胞的稳定性和效能是一个关键问题。脂肪细胞的 变棕 过程需要精确的基因编辑和培养条件,这在临床应用中需要进一步优化。
其次,临床应用中的个性化治疗方案虽然具有很大潜力,但也面临着患者细胞处理的复杂性和时间要求。在一些患者中,提取足够数量的自体脂肪细胞可能会成为一个挑战,尤其是对于体重较轻或脂肪量较少的患者。因此,如何高效、低风险地获取并处理患者的脂肪细胞,是实现这一治疗方案的另一大障碍。
最后,尽管这种疗法在小鼠模型中已取得积极成果,但其长期疗效和潜在副作用仍需要在临床试验中进一步验证。癌症治疗涉及多方面的复杂机制,单一疗法可能无法解决所有问题。因此,未来的研究可能需要将这种脂肪细胞 变棕 疗法与其他疗法(如化疗、免疫疗法等)结合使用,以实现更好的治疗效果。
尽管面临这些挑战,基于脂肪细胞 变棕 的治疗方法无疑为癌症治疗开辟了新的可能性。随着技术的不断发展和优化,这一方法有望在未来的临床实践中发挥重要作用,为癌症患者带来更多治疗选择和希望。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- HICOOL 2025峰会聚焦:签约央企国家队、首发新品、启动国际联合体,国典医药奏响再生医学“三重奏” (2025-10-23)
- 2025年福建省药品检验技能比武圆满收官 (2025-10-23)
- 引领医药项目管理迈向新高度--第二届中国医药企业项目管理大会定于11月在京召开 (2025-10-23)
- 牙周炎伴牙龈萎缩:8款医用级修复解决方案权威推荐 (2025-10-23)
- 辽宁:2025年11月1日起全面完成生养津贴发放至团体 (2025-10-23)
- 放射科与分研院联合研究成果发表于Science子刊,为动脉粥样硬化诊疗开辟新路径 (2025-10-23)
- 用药更少、服用更不便:我国幽门螺杆菌根除医治研讨取得新突破 (2025-10-23)
- 醉酒后光止吐没用!GFX 护肝胶囊用实力护肝脏 (2025-10-23)
- Nat Biotechnol:给免疫细胞“写记忆”!科学家发明不伤DNA的基因开关,抗癌能力有望持久升级 (2025-10-23)
- 《神经病学年鉴》:评估一个简单的转身动作,或可提前8.8年预测帕金森病! (2025-10-23)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















