《自然》子刊:让PD |
 |
《自然》子刊:让PD-L1“内耗”!中南大学团队揭示,增强琥珀酰化修饰可使癌细胞PD-L1加速降解,激活免疫应答
来源:奇点糕 2025-03-14 10:26
中南大学团队本次研究就是以线粒体代谢为出发点,但相信大家也能猜到,琥珀酰化修饰真要不影响抗肿瘤免疫应答,那才叫做怪事。中南大学陈翔、刘洪、刘静等研究者合作在Nature Genetics期刊发表的最新研究成果[1]就揭示,PD-L1蛋白的琥珀酰化修饰(succinylation)可导致其加速被降解,而调控琥珀酰化修饰的关键酶是线粒体代谢酶CPT1A,它有着成为治疗疗效预测标志物和干预靶点的价值,例如针对CPT1A进行抑制,就有望与PD-1/L1抑制剂协同增效。
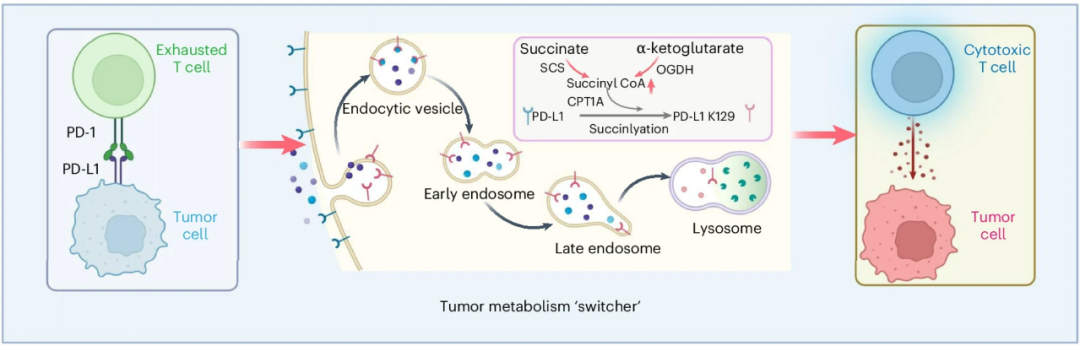
一图总结论文发现的核心作用机制
此前学界已经发现,琥珀酰化修饰往往在癌症中参与调控代谢重编程[2],中南大学团队本次研究就是以线粒体代谢为出发点,但相信大家也能猜到,琥珀酰化修饰真要不影响抗应答,那才叫做怪事[3]。对瘤患者蛋白组学数据的分析显示,三羧酸循环及氧化磷酸化通路活跃,与患者预后较好和对免疫治疗有应答相关,其中最突出的就是三种可桥接三羧酸循环及氧化磷酸化、并参与琥珀酸产生的关键酶(OGDH、SCS、SDH)。
小鼠实验也证实,补充上述三种关键酶高表达可增加的相应代谢物(如 -酮戊二酸和琥珀酸),就能通过改善免疫浸润和CD8+T细胞激活状态,增强抗肿瘤免疫应答来抑制肿瘤生长,但这些代谢物的直接影响对象都主要是,它们均会使癌细胞内的琥珀酰辅酶A(succinyl-CoA)水平上升,抑制琥珀酰辅酶A合成路径就会使抑癌作用消失。
进一步分析显示,癌细胞内的琥珀酰辅酶A水平上升,会与PD-L1蛋白水平下降同步发生,但与PD-L1 mRNA水平变化不匹配,PD-L1蛋白的半衰期明显缩短,这就说明琥珀酰辅酶A是在蛋白质层面通过转录后修饰,加速了癌细胞内PD-L1蛋白的降解,免疫荧光染色也确认了PD-L1蛋白经内体-溶酶体途径被降解的路径。
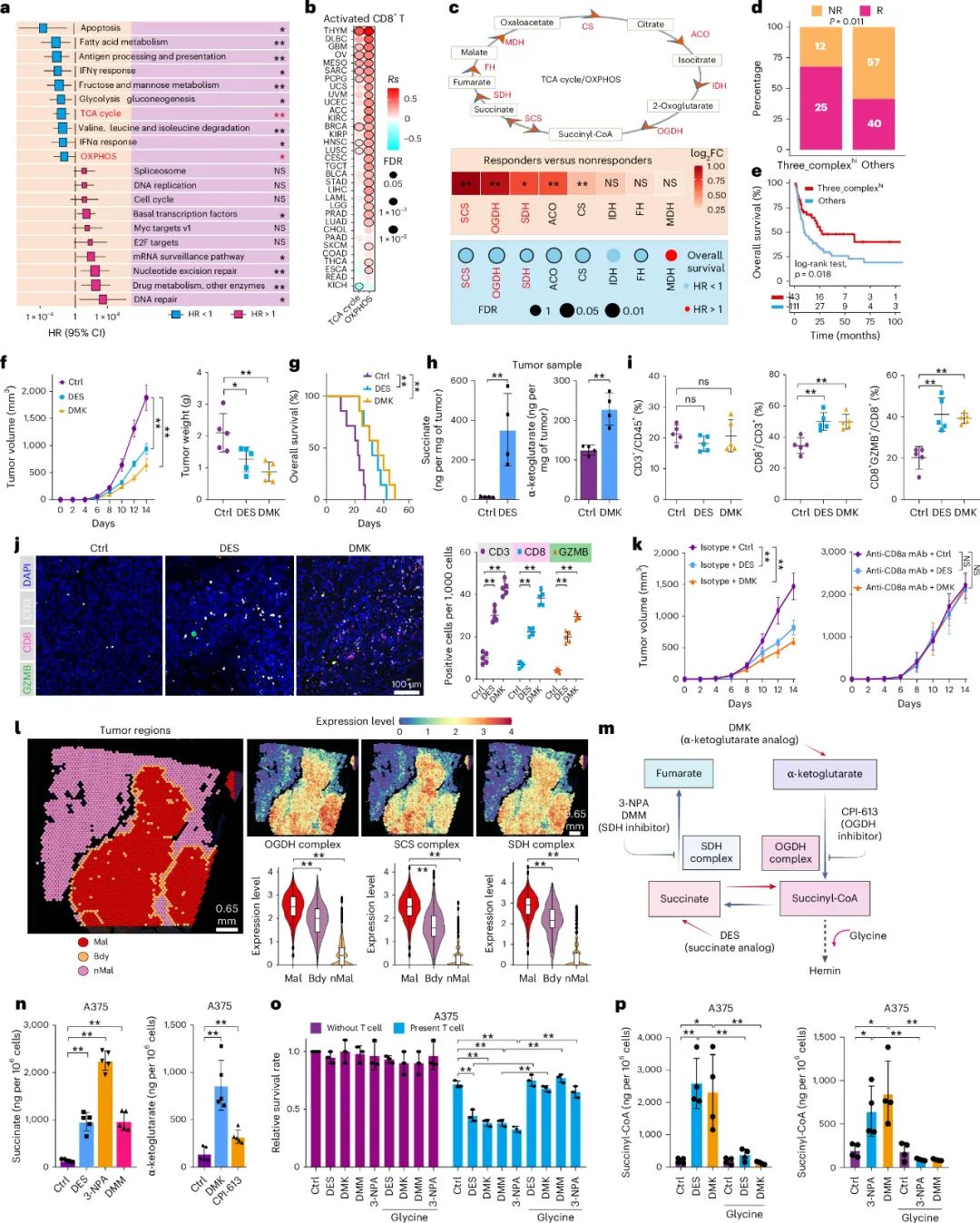
琥珀酰辅酶A水平上升与免疫应答增强同步发生
又是琥珀酰辅酶A又是转录后修饰,那调控机制具体到琥珀酰化修饰就很顺理成章了:质谱分析证实,PD-L1蛋白的Lys129和Lys136位点会发生琥珀酰化修饰,但只有前者会导致PD-L1被加速降解,而调控该过程的就是CPT1A,它虽然主要位于线粒体,但可以与暴露到胞质的PD-L1细胞外结构域结合,作为琥珀酰转移酶促进PD-L1降解。
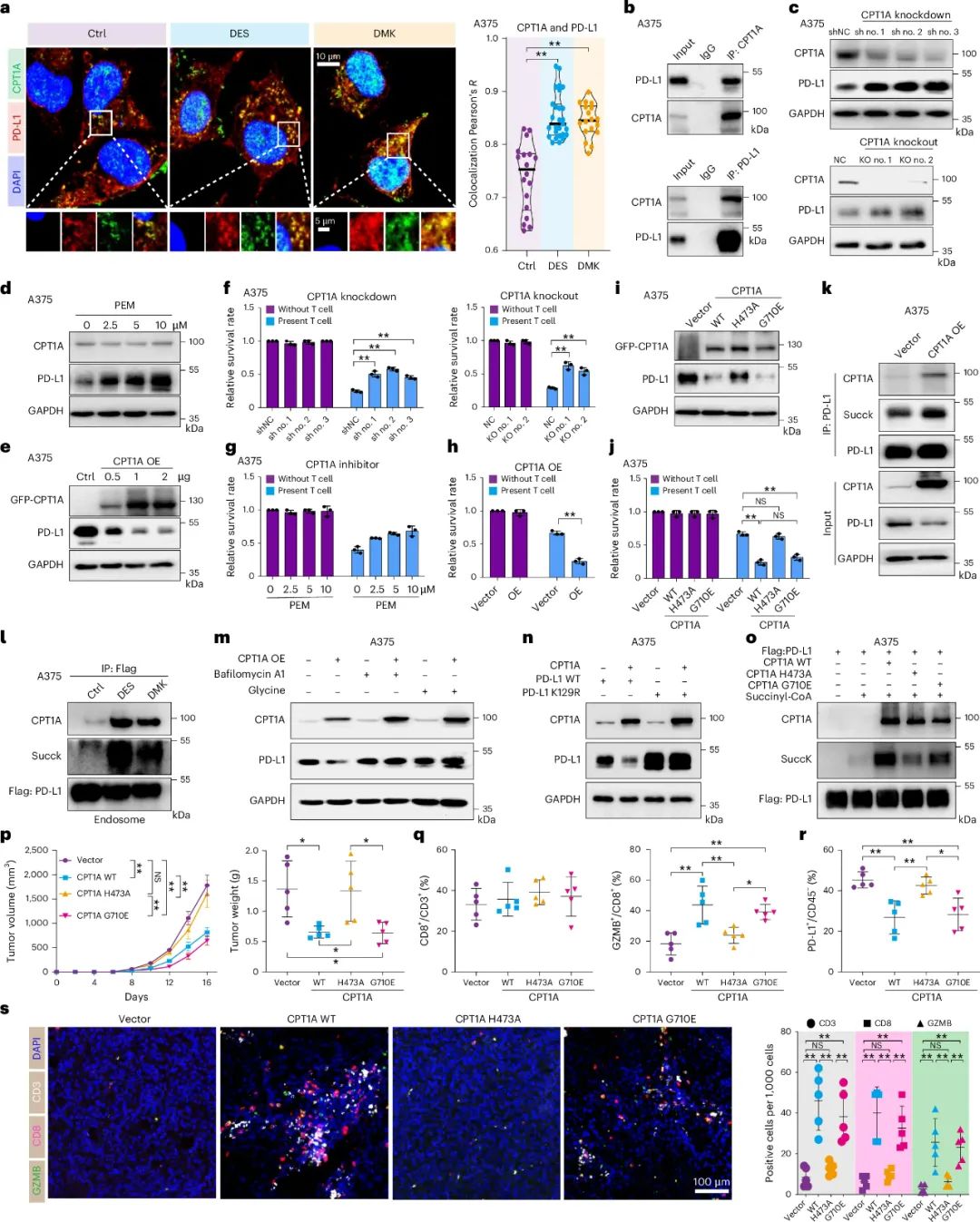
CPT1A是调控PD-L1琥珀酰化修饰、使其加速降解的关键酶
也就是说,CPT1A多了PD-L1就会少,而既往研究已经显示,激活PPAR/PGC-1 通路可上调CPT1A表达[4],研究者们也证实现有降脂药苯扎贝特就可通过该通路降低癌细胞PD-L1表达,进而为抗肿瘤免疫应答 松绑 ,与CTLA-4抑制剂协同增效。此外,CPT1A表达水平也可作为预测免疫治疗效果的标志物,但CPT1A低表达使癌细胞PD-L1上调,或许更利于PD-1/L1抑制剂起效,抑制CPT1A也可能是研究成果的主要转化方向。
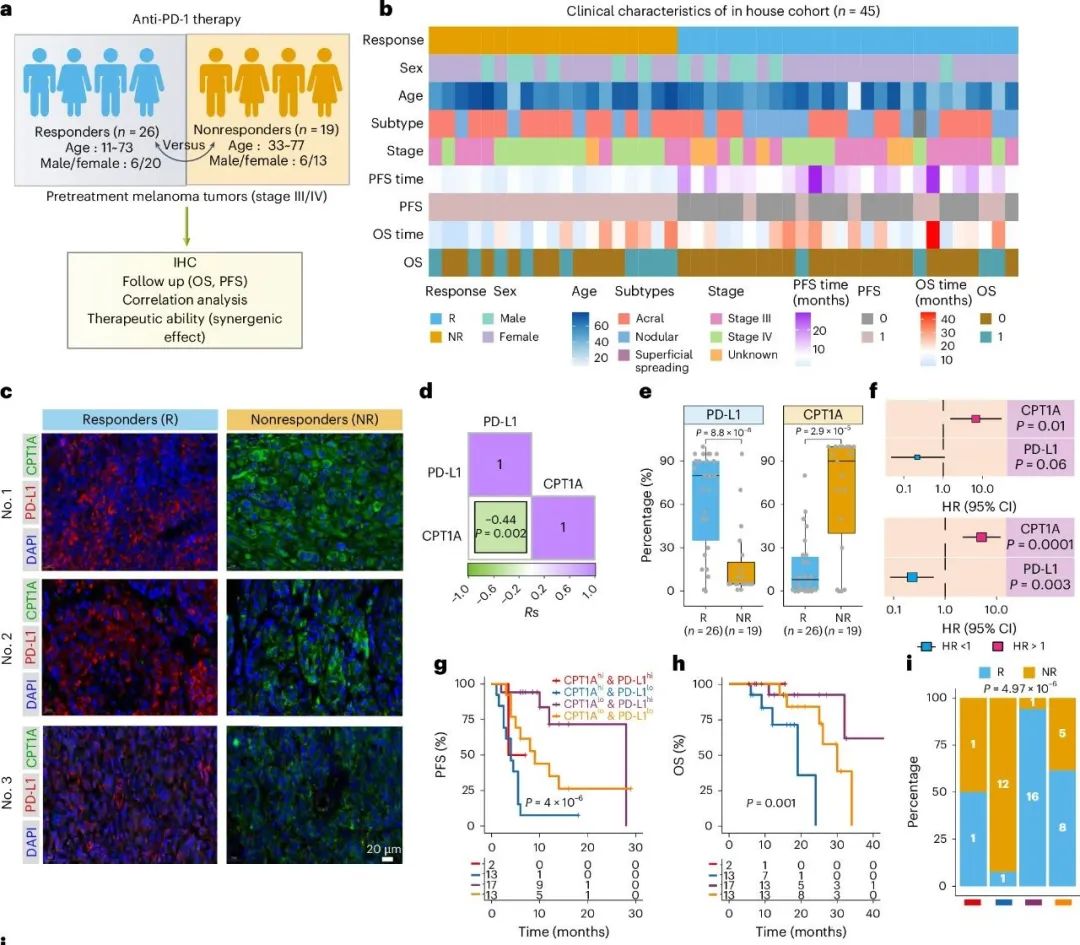
黑色素瘤患者CPT1A及PD-L1表达水平与免疫治疗效果的关联
参考文献:
[1] Liang L, Kuang X, He Y, et al. Alterations in PD-L1 succinylation shape anti-tumor immune responses in melanoma[J]. Nature Genetics, 2025.
[2]Liu Z, Wang R, Wang Y, et al. Targeting succinylation-mediated metabolic reprogramming as a potential approach for cancer therapy[J]. Biomedicine Pharmacotherapy, 2023, 168: 115713.
[3]Zheng Z, Xiao P, Kuang J, et al. Unlocking the Hidden Potential of Cancer Therapy Targeting Lysine Succinylation[J]. Journal of Cancer, 2025, 16(3): 821-834.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature Medicine:这个基因突变,会导致肥胖,但能抵御心脏病 (2025-10-19)
- 《柳叶刀》子刊:艾扬格瑜伽,增加跌倒风险!随机对照试验结果显示,与坐姿瑜伽相比,艾扬格瑜伽与老年人跌倒风险增加33%相关 (2025-10-19)
- 《自然·神经科学》:中国科学家揭示深脑刺激治疗帕金森病的神经机制,并发现更安全、成本更低的替代方法! (2025-10-19)
- 2025年槲皮素哪个牌子效果最好?2025年十大槲皮素清肺品牌排行榜,清肺护肺哪个好? (2025-10-19)
- 赛诺菲胰岛素原料药项目启动,助力北京打造全球医药健康产业高地 (2025-10-18)
- Nature Medicine:首次人体实验,PD-1单抗治疗艾滋病 (2025-10-18)
- 百年药企参天公司旗下维生素B12滴眼液参天玫瑰®焕新上市 (2025-10-17)
- 神经元只负责“干活”?Nature:星形胶质细胞才是记忆“保存总监”,双重认证锁死重要记忆 (2025-10-17)
- 赛诺菲胰岛素原料药项目启动,助力北京打造全球医药健康产业高地 (2025-10-17)
- Nat Cell Biol:结肠癌也“分地段”?科学家找到决定癌症位置的“源头细胞” (2025-10-17)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















