mRNA疫苗出手:只需一剂,即可抵抗HPV相关肿瘤,效果优于DNA或重组蛋白疫苗 |
 |
来源:生物世界 2023-03-16 13:20
这项研究在广泛的对比实验中证明了三种不同的mRNA疫苗的免疫原性和治疗效果,其表现均优于基于DNA和蛋白质的常规的gDE7疫苗。这些研究数据支持在临床试验中进一步评估这些mRNA疫苗宫颈癌,是最常见的妇科恶性肿瘤之一。临床研究表明人乳头瘤病毒(HPV)感染,特别是高危型HPV的持续感染,是引起子宫颈癌前病变和宫颈癌的重要原因。开发和接种HPV疫苗对降低宫颈癌发病率十分重要。
真实世界数据也表明,HPV疫苗接种大幅降低了宫颈癌发病率。例如,英国的HPV疫苗免费接种计划几乎完全消除了1995年9月1日以后出生的女性的宫颈癌。
此外,HPV感染不仅仅会导致女性宫颈癌,还会导致生殖器疣、肛门癌等男女皆可患病的疾病,HPV6和HPV11导致了约90%的生殖器疣,HPV16和HPV18导致了约70%的宫颈癌和肛门癌。因此,不少国家同时对男性和女性接种HPV疫苗。
新冠大流行以来,mRNA疫苗大放异彩,获得了空前的发展。这种新型疫苗形式的巨大潜力也推动科学家们开发针对其他传染病以及癌症的强效mRNA疫苗。
近日,圣保罗大学、宾夕法尼亚大学、Acuitas公司、BioNTech公司的研究人员合作,在Science Translation Medicine期刊发表了题为:Single immunizations of self-amplifying or non-replicating mRNA-LNP vaccines control HPV-associated tumors in mice的研究论文。
该研究在HPV诱发的小鼠肿瘤模型中测试了三种不同的HPV mRNA疫苗的原性和治疗效果。结果显示,单剂HPV mRNA疫苗就能诱导强烈的CD8+ T细胞反应,发挥强大的抗肿瘤功效,其表现要优于HPV重组蛋白疫苗和HPV DNA疫苗。

mRNA疫苗可以分为非复制型mRNA(nr-mRNA)疫苗和自复制型mRNA(sa-mRNA)疫苗。nr-mRNA疫苗编码抗原的表达水平会随时间流逝而不断降低。相比之下,sa-mRNA添加了来自甲病毒的复制酶序列,在进入细胞后可以自我复制,从而延长表达抗原的时间,也降低使用剂量。
此外,nr-mRNA疫苗还可以划分为两种。一种是由未修饰的mRNA构成,具有高度促炎症性,这些强烈的炎症反应可能有利于CD8+ T细胞的激活,而CD8+ T细胞在抗肿瘤反应中起关键作用,但强烈的炎症反应也可能导致不良事件。另一种是由修饰过的mRNA构成,能降低炎症反应,还能增强mRNA翻译效率。
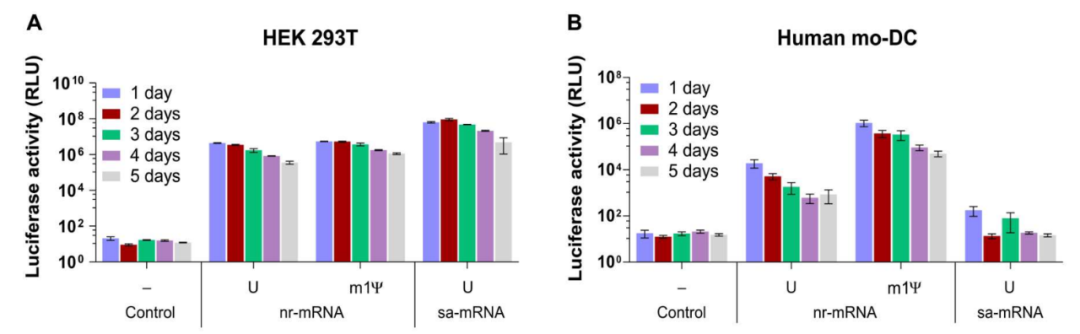
三种mRNA疫苗(sa-mRNA、未修饰的nr-mRNA、修饰的nr-mRNA)的翻译效率比较
这三种mRNA疫苗平台(sa-mRNA、未修饰nr-mRNA和修饰nr-mRNA)已在动物模型中进行了广泛的测试,并发现可以诱导针对各种病原体和肿瘤类型的有效免疫应答。值得一提的是,mRNA疫苗已在临床前研究中成功治疗HPV相关肿瘤。此外,正在进行的针对HPV-16头颈部鳞状细胞癌的1/2期临床试验也是使用mRNA编码的抗CD40进行治疗(NCT03418480)。
在这项最新研究中,研究团队使用这三种mRNA疫苗平台,制备了编码1型单纯疱疹病毒(HSV-1)糖蛋白D(gD)和HPV-16 E7癌蛋白(E7)融合的嵌合蛋白的mRNA疫苗,同样使用脂质纳米颗粒(LNP)进行递送。紧接着,在已被广泛研究的实验性HPV相关肿瘤模型的基础上,研究小组对三种编码相同靶抗原的mRNA疫苗的诱导免疫反应和治疗效果进行了详细的比较分析。
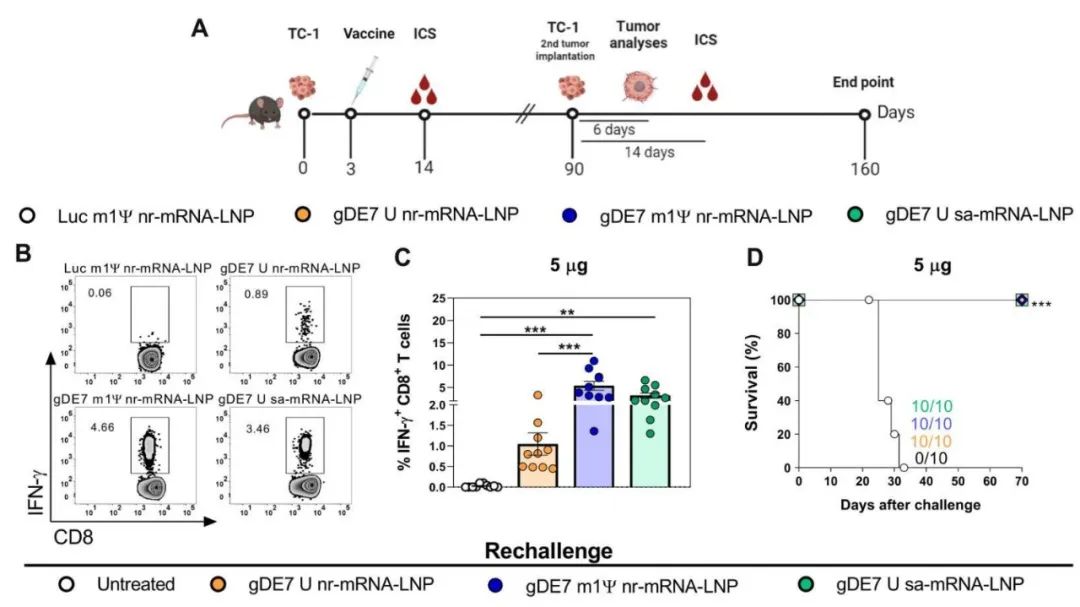
三种mRNA疫苗均具有强大的抗肿瘤效果
研究结果表明,三种gDE7 mRNA疫苗中的任何一种,在单次、低剂量接种后,都能诱导E7特异性CD8+ T细胞的激活,产生能够预防肿瘤复发的记忆T细胞反应,并根除不同生长阶段的皮下肿瘤,甚至即使是在生长晚期也能控制肿瘤进展。

gDE7 mRNA-LNP单次免疫即可诱导强烈的e7特异性细胞毒性CD8+ T细胞反应
更重要的是,在接种单剂量gDE7 mRNA-LNP疫苗后,就可以在两种不同的原位小鼠肿瘤模型中诱导了有效的肿瘤保护。最后,比较研究表明,三种gDE7 mRNA-LNP疫苗在免疫原性和抗肿瘤效果等方面均优于gDE7 DNA疫苗和gDE7重组蛋白疫苗,并显著提高了肿瘤小鼠模型的生存率。
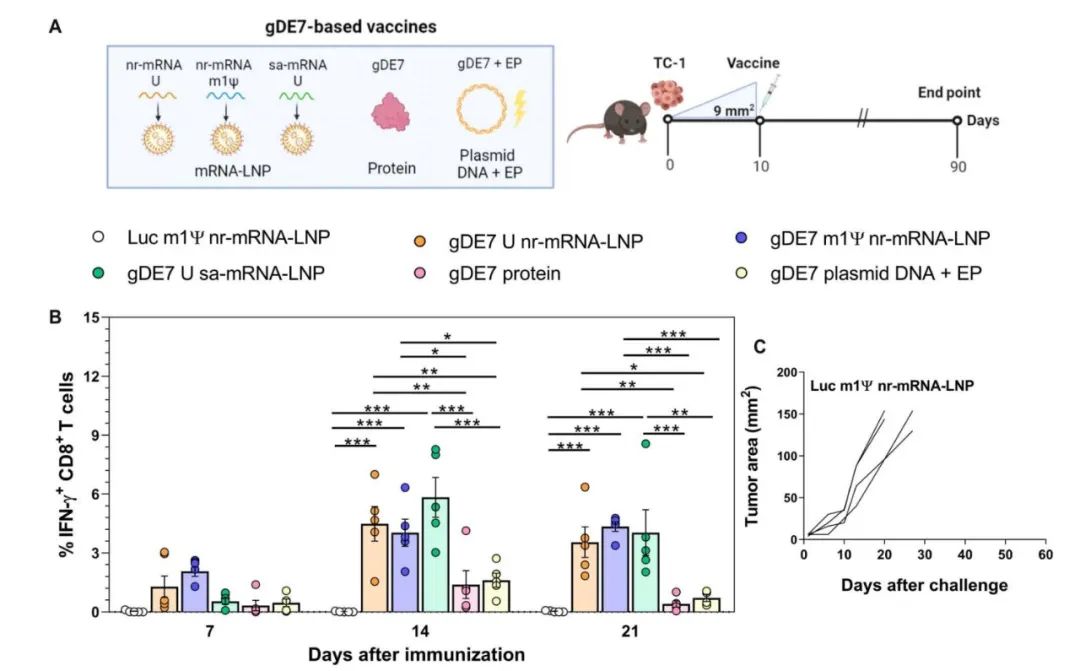
gDE7 mRNA-LNP疫苗、gDE7 DNA疫苗和gDE7重组蛋白疫苗的免疫原性和抗肿瘤疗效的比较
总而言之,这项研究在广泛的对比实验中证明了三种不同的mRNA疫苗的免疫原性和治疗效果,其表现均优于基于DNA和蛋白质的常规的gDE7疫苗。这些研究数据支持在临床试验中进一步评估这些mRNA疫苗,为抗肿瘤mRNA疫苗的临床应用开辟了令人兴奋的前景。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- Nature Genetics:我们沿用20年的小鼠参考基因组,究竟错过了什么?一份T2T图谱的完整答案 (2025-10-26)
- 情感传染!南方医科大学最新论文登上Science封面 (2025-10-26)
- Nature Biotechnology:数据基准与算法创新的双轮驱动——DeepSomatic研究定义的基因组学发现新范式 (2025-10-25)
- Nature:当饥饿遇上荷尔蒙——大脑如何权衡母爱与生存? (2025-10-25)
- 加科思药业在AACR-NCI-EORTC国际大会公布泛KRAS抑制剂(JAB-23E73)临床前数据 (2025-10-24)
- 《柳叶刀》:减肥神药,暗藏护心秘法!迄今最大规模临床试验证实,司美格鲁肽的心脏保护作用与基线肥胖和体重减轻无关,或有独特保护机制 (2025-10-24)
- Cell子刊:脂肪细胞脂解,激活上皮干细胞,促进毛发再生 (2025-10-24)
- AJPCP:线粒体钾通道调节棕色脂肪组织的产热,为新的肥胖治疗铺平道路 (2025-10-24)
- 生育力下降别只怪卵子!Science:卵巢里的神经、胶质细胞才是“隐形操控者” (2025-10-24)
- Science:泛素介导的线粒体自噬调节线粒体DNA突变的遗传 (2025-10-24)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















