Cancer Res:武汉大学的研究者们揭示了一种增强子在癌症疾病中的作用机制 |
 |
来源:100医药网 2024-03-22 15:00
该研究揭示了BRD4调控转录的KDM5C介导机制,为将BETi纳入与KDM5C抑制剂联合治疗以提高治疗效果提供了理论依据。基因表达程序决定细胞命运,转录失调可导致多种疾病。最近,增强子破坏越来越多地被认为是一种疾病驱动机制,包括人类癌症。转录因子(TFs)、辅助因子和染色质调节因子参与维持增强子的活性状态;然而,调控协调的分子机制在很大程度上仍然不清楚。

图片来源:
近日,来自武汉大学的研究者们在Cancer Res杂志上发表了题为 KDM5C-mediated recruitment of BRD4 to chromatin regulates enhancer activation and BET inhibitor sensitivity 的文章,该研究揭示了BRD4调控转录的KDM5C介导机制,为将BETi纳入与KDM5C抑制剂联合治疗以提高治疗效果提供了理论依据。
BET家族成员BRD4是一种含溴结构域的蛋白,在驱动癌基因表达中起重要作用。鉴于BET抑制剂在各种癌症类型的致癌网络调节中的关键作用,其临床应用一直受到剂量限制性毒性和耐药性的阻碍。了解BRD4活性的机制和识别预测性生物标志物可以促进BETis的成功临床应用。
在这里,研究者发现KDM5C和BRD4协同维持的生长。在机制上,KDM5C与BRD4相互作用并刺激BRD4增强子的募集。此外,BRD4 c -末端与KDM5C的结合刺激了KDM5C的H3K4去甲基化酶活性。kdm5c相关BRD4和h3k4me /3的丰度决定了许多癌基因的转录激活。
值得注意的是,在肿瘤细胞系和患者来源的类器官模型中,KDM5C的耗损或药理降解显著降低了BRD4染色质的富集,并显著提高了BETi在多种癌症类型中的疗效。此外,在异种移植小鼠模型中,靶向KDM5C与BETi联合抑制肿瘤生长。
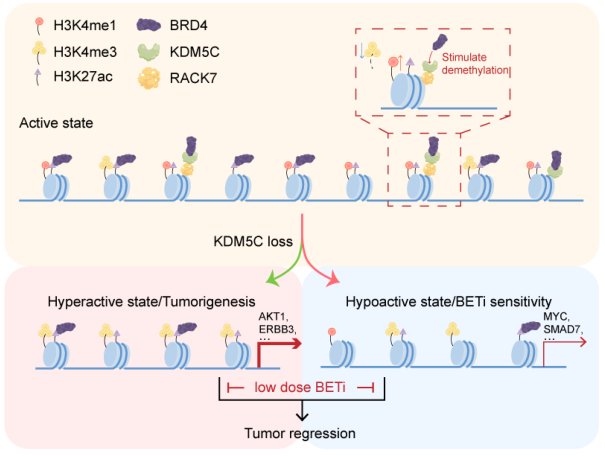
kdm5c介导的BRD4募集和组蛋白去甲基化模型维持增强子的活性状态
图片来源:
总之,本研究证明了KDM5C招募BRD4为活性增强子元件,并表现出更高的组蛋白去甲基化酶活性,以维持活性增强子状态并调节基因表达模式。这些发现为开发新的癌症联合疗法提供了线索。( 100yiyao.com)
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 重庆市规范部门西医类医疗服务价钱名目及 医保付出政策 (2025-10-28)
- 脊髓损伤患者的康复新曙光!Biomaterials证实通道图案化胶原支架培育功能类器官,高效修复脊髓损伤 (2025-10-28)
- Cell:RAEFISH技术为研究复杂组织中的RNA活性提供了更大、更好的窗口 (2025-10-27)
- 关于举办“损容性皮肤病及医美”稳态管理创新人才高级培训班的通知 (2025-10-27)
- 东北林业大学,首次发表Science论文 (2025-10-27)
- 雷浪潮:建设生养敌对型社会 推进老有所养、老有所为 (2025-10-27)
- 第八届中国医疗东西立异守业年夜赛总决赛在津启幕 (2025-10-27)
- 三阴性乳腺癌迎“破局者”!J Hematol Oncol:现货 CAR-NKT 细胞三重绞杀肿瘤,成本直降90% (2025-10-27)
- Nature子刊:多发性硬化症与独特的口腔微生物组相关联 (2025-10-27)
- Oncogene:帕博西尼和泰拉格司他组合使用有望治疗结直肠癌 (2025-10-27)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















