FDA接受辉瑞/礼来潜在“first |
 |
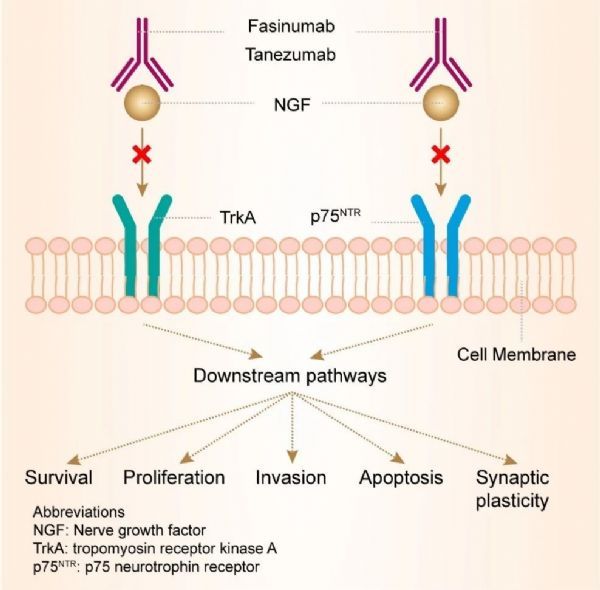
日前,(Pfizer)和(Eli Lilly and Company)公司联合宣布,美国接受其皮下注射止痛药tanezumab的生物制品许可申请(BLA),治疗因中重度骨关节炎(OA)而引起慢性疼痛的患者。Tanezumab是一款人源化的因子(NGF)单克隆抗体。
由于骨骼两端具有保护功能的软骨磨损而导致的OA,是一种进展型的关节疾病。OA最主要的症状之一是慢性疼痛,可能在关节运动时或运动后发生,同时也会限制患者的运动能力。在美国,OA影响了大约2700万人,其中1100万为中重度OA患者。这些OA患者急需一款安全的新型疗法来帮助他们管理疼痛。
Tanezumab是一款人源化因子单克隆抗体,也是首款得到快速通道资格的NGF抑制剂,它具有可以选择性结合并抑制NGF的功能。在人体出现因受伤、炎症引起的疼痛或慢性疼痛时,NGF的水平也会相应上升。因此,通过选择性抑制NGF,tanezumab可能有助于阻断肌肉、皮肤和器官产生的疼痛信号进入脊髓和大脑。
由于tanezumab这一新作用机制与阿片类药物和包括非甾体类抗炎药(NSAIDs)在内的其它镇痛药完全不同,在至今为止的试验中从未出现过任何成瘾、滥用或依赖的风险。Tanezumab的研究目前主要针对OA疼痛、重度慢性腰疼(CLBP)以及由于癌症骨转移引起的疼痛这三类疼痛的治疗。
该项BLA的递交是基于39项1至3期的积极数据,这些试验评估了tanezumab在治疗18000例患者中的疗效与安全性,其中包括3项评估中重度OA患者的3期试验。在其中一项为期24周的3期临床研究中,tanezumab达到了试验的所有主要终点,它的治疗使膝关节或髋关节中重度OA疼痛患者感受的疼痛和身体功能达到统计学意义上的显着改善。在另一项为期16周的3期临床研究中,超过一半患者的疼痛程度获得了50%及以上的减轻。
“接受tanezumab的上市申请是一项重要的里程碑,”辉瑞全球产品开发团队负责人Ken Verburg博士说:“近十多年来,没有治疗这种使人衰弱的OA疗法出现。因此,这些患者迫切需要创新疗法出现。其它止痛药对中重度OA导致的慢性疼痛的治疗没有使患者达到很好的缓解。如果获得批准,tanezumab将成为治疗这些患者的first-in-class疗法。”
“OA患者面临巨大的身体疼痛负担,几乎在生活的每个方面都受到影响。这种疼痛会影响他们参与日常活动的能力,同时对患者心理也产生重大影响,”生物医学总裁Patrik Jonsson先生说:“我们期待与紧密合作,将tanezumab尽快带给中重度OA患者。”(100yiyao.com)
医药网新闻
- 相关报道
-
- Cell Death and Disease:类器官模型揭示 ULBP2 CAR-T 细胞对胃癌的杀伤作用 (2025-08-12)
- Cell子刊:华人团队开发新型微针贴片,促进心肌梗塞后的心脏修复 (2025-08-12)
- 颜宁团队发表最新PNAS论文:助力心脏病及抗癫痫/镇痛药物精准设计 (2025-08-12)
- STTT:湖北工业大学团队发现“癌王”进展新机制和治疗新靶点! (2025-08-12)
- Nature Neuroscience:宋洪军/明国莉/周毅团队揭示人类海马新生未成熟神经元的独特演化规律 (2025-08-12)
- 第十一届马凡病友大会:以爱为翼,让健康与希望接力传递 (2025-08-11)
- Nature子刊:邹强/崔心刚/倪志宇/高强团队发现,饮食来源的半乳糖具有抗癌作用 (2025-08-11)
- 海南封关在即:外泌体产业迎来新机遇 (2025-08-11)
- 激活大脑“清洁工”!Nat Aging:ACE 蛋白让小胶质细胞重获“噬”斑能力,或可逆转阿尔茨海默病? (2025-08-11)
- 数十年前的诺奖级发现,正在挽救这类癌症患者生命 (2025-08-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















