研究揭示杀虫真菌侵染结构附着胞分化形成的表观遗传机制及调控通路 |
 |
3月26日,中国科学院分子植物科学卓越创新中心昆虫发育与进化生物学重点实验室王四宝研究组与中国科学院上海营养与健康研究所魏刚研究组合作在国际学术期刊《科学进展》(Science Advances)上在线发表了题为Coordinated regulation of infection-related morphogenesis by the KMT2-Cre1-Hyd4 regulatory pathway to facilitate fungal infection 的研究论文。该研究揭示了杀虫真菌通过表观KMT2-Cre1-Hyd4通路调控真菌侵染结构——附着胞的发育分化和杀蚊毒力的分子机制。
蚊虫是疟疾、革登热等多种疾病的传播媒介。蚊虫控制是阻断蚊媒传染病的重要措施。有别于和病毒等杀虫微生物需要通过消化道侵染昆虫,杀虫真菌以穿透体壁的入侵方式感染昆虫,能够更高效地杀死抗药性蚊虫,显着降低蚊媒疾病的传播,具有环境友好、持续控制、不易产生抗性的特点,因而在蚊虫生物防治和阻断疾病传播上具有巨大的优势,被认为是最有潜力的下一代生物杀蚊剂之一。在入侵寄主体壁的过程中,杀虫真菌产生一种重要的特殊侵染结构——附着胞,附着胞通过分化成侵染钉以及分泌一系列降解昆虫体壁的胞外酶等方式来穿透体壁。因此,附着胞的分化形成对于真菌成功侵染寄主蚊虫至关重要。然而,人们对附着胞分化形成的调控机制知之甚少。
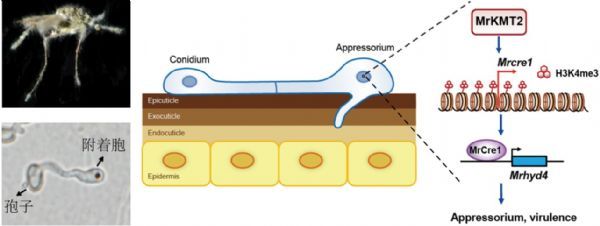
本研究基于前期真菌与蚊虫互作过程中的基因表达谱分析(Science China Life Sciences, 2017),鉴定到一个在绿僵菌早期侵染蚊虫体壁时特异上调表达的表观遗传调控因子——组蛋白赖氨酸甲基转移酶基因kmt2。研究表明KMT2催化组蛋白H3第4位赖氨酸甲基化(H3K4me3)修饰,在真菌侵染蚊虫体壁阶段发挥重要的调控作用。敲除kmt2基因显着减少真菌附着胞的形成,并显着降低杀蚊毒力。转录组测序(RNA-seq)研究发现,经昆虫体壁诱导后,依赖于MrKMT2的差异表达基因主要参与脂类、碳水化合物的代谢和转运。利用染色质免疫共沉淀结合二代测序(ChIP-seq)技术,分析H3K4me3在野生型(WT)和敲除菌株(ΔMrkmt2)中的染色质分布情况,发现KMT2介导的H3K4me3修饰主要与基因转录激活相关。通过对WT和突变体在体壁诱导条件下的ChIP-seq和RNA-seq的关联分析,结合学验证和表型测定,发现受昆虫体壁诱导表达的KMT2通过将H3K4me3标记富集于转录因子Cre1基因位点染色质区域进而转录激活cre1的表达,上调表达的Cre1再通过转录激活疏水蛋白基因hyd4来调控真菌附着胞的分化形成,从而完整地揭示了由KMT2-Cre1-Hyd4协同调控附着胞发育分化的机制和调控通路(如图)。
该研究深入揭示了杀虫真菌附着胞分化的分子调控机制,不仅为虫生真菌与寄主昆虫相互作用提供新机制,而且为高效杀蚊真菌改良提供新的靶点和改造策略。(100yiyao.com)
医药网新闻
- 相关报道
-
- Cell Death and Disease:类器官模型揭示 ULBP2 CAR-T 细胞对胃癌的杀伤作用 (2025-08-12)
- Cell子刊:华人团队开发新型微针贴片,促进心肌梗塞后的心脏修复 (2025-08-12)
- 颜宁团队发表最新PNAS论文:助力心脏病及抗癫痫/镇痛药物精准设计 (2025-08-12)
- STTT:湖北工业大学团队发现“癌王”进展新机制和治疗新靶点! (2025-08-12)
- Nature Neuroscience:宋洪军/明国莉/周毅团队揭示人类海马新生未成熟神经元的独特演化规律 (2025-08-12)
- 第十一届马凡病友大会:以爱为翼,让健康与希望接力传递 (2025-08-11)
- Nature子刊:邹强/崔心刚/倪志宇/高强团队发现,饮食来源的半乳糖具有抗癌作用 (2025-08-11)
- 海南封关在即:外泌体产业迎来新机遇 (2025-08-11)
- 激活大脑“清洁工”!Nat Aging:ACE 蛋白让小胶质细胞重获“噬”斑能力,或可逆转阿尔茨海默病? (2025-08-11)
- 数十年前的诺奖级发现,正在挽救这类癌症患者生命 (2025-08-11)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















