西美利14个一类新药和5个主要品种的首本! |
 |
近日,simcere宣布与上海药物研究所等就新冠肺炎候选药物SIM0417系列的全球开发、生产和商业化达成项目合作。在创新转型最前沿的simcere,2021H1创新药营收增长约57%,占营收比重约58%,成为以创新药业务为主的医药公司。目前公司在研创新药物项目近60个,14个1类新药处于临床应用及以上阶段,其中4个已上市。在仿制药方面,有15个品种被高估(6个为首次),5个品种被首次仿制,其中超过90亿美元的品种被专门报道用于生产。
创新药销售占比近60%,医保助推1类新药放量
Simcere,致力于快速向研发转型;d和创新驱动,已成为以创新药物业务为主的医药公司,是众多传统医药公司创新转型的典型代表之一。
中期业绩报告显示,2021年,H1希姆切雷实现营收约21.2亿元,同比增长10.1%,其中创新药营收约12.2亿元,同比增长56.8%,占总营收的57.6%。净利润约5.55亿元,较去年同期增长约200.2%。
simcere创新药物收入占总收入的比例
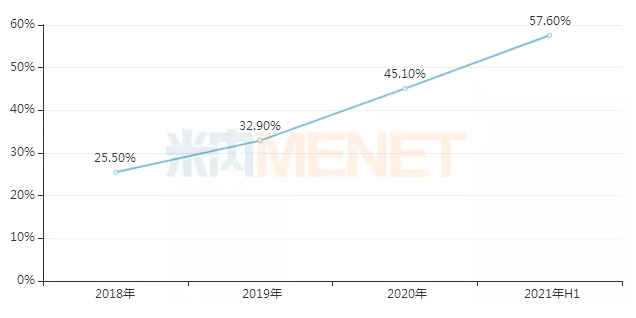
来源:上市公司公告
近年来,simcere创新药物的收入逐年增长。得益于一类新药依达拉奉右美沙芬注射液收入的快速增长,2021年H1公司创新药销售额再创新高,达57.6%。
研发。d .对希姆切雷的投资(单位:亿元)
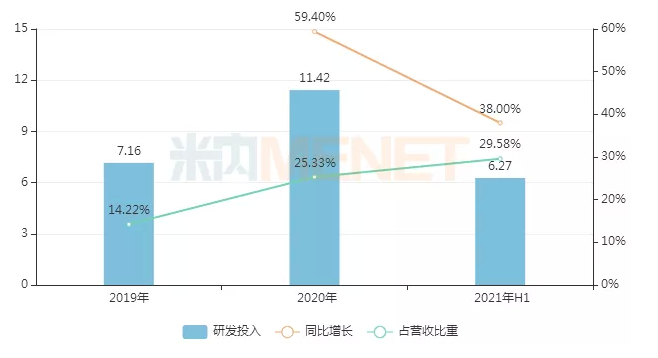
来源:上市公司公告
2021年,H1希姆切雷投入研发资金约6.27亿元;d、较去年同期增长38%,占营收的29.6%。近年来,研发;simcere的d强度逐年提升,从2018年的9.9%提升至2021年H1的29.6%,可见公司向研发快速转型的决心和速度;创新。
目前已有4种创新药物获批在simcere上市,分别是依达拉奉右美沙芬注射液、重组人血管内皮抑素注射液、Iramod片剂和Abbasip注射液。
依达拉奉右美沙芬醇注射液于2020年7月获批,是近5年来全球唯一获批的卒中新药。上市不到半年,经协商被纳入国家医保乙类。米内网数据显示,2021H1年该产品在中国城市公立、县级公立医院、城市社区中心、乡镇卫生院(简称中国公立医疗机构)的终端销售额超过2亿元。
2020年获批的还有从simcere引进的创新药Abbasip注射液,这是国内首个也是唯一一个获批的CTLA4-Fc融合蛋白,也是目前唯一获批的T细胞选择性共刺激免疫调节剂,用于治疗类风湿关节炎。该产品参加了2021年医保谈判。据报道,simcere只用了25分钟就完成了谈判。
同样用于类风湿性关节炎的1类新药——伊拉莫德片,是世界上第一个上市的药物,也是中国唯一上市的药物。是B类国家医疗保险产品。2020年,中国城市实体在中国公立医疗机构和医院终端的销售总额超过10亿元,同比增长54.3%。目前该产品在二期临床有治疗干燥综合征的新适应症。
重组人内皮抑素注射液是目前国内外唯一获批上市的内皮抑素,也是国内首个抗血管生成靶向药物。该产品已纳入医疗保险多年。2020年,中国城市公立医疗机构和实体药店销售总额超过10亿元。对于该产品,simcere正在积极拓展新的适应症,其中恶性胸腹水的适应症正在进行III期临床试验。
完善的销售和促销体系叠加医保量,西米赛创新药收入增加
药店正在部分研究创新药物。
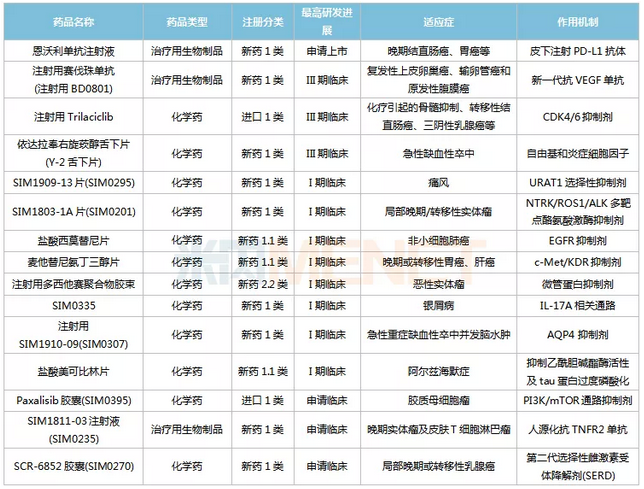
来源:Minenet中国药物临床试验宣传库
在抗肿瘤领域,与西迪、康宁杰瑞合作的恩沃利单抗已提交NDA,近期进入行政审批阶段,有望成为全球首个可皮下注射的PD-L1单抗。与美国Apexigen合作的Sevazhumab属于新一代重组人源化抗血管内皮生长因子(VEGF)单克隆抗体,抗肿瘤作用更强,目前正在进行III期临床试验。Trilaciclib是与美国G1公司合作的CDK4/6抑制剂,具有全面的骨髓保护作用,目前正在进行三期临床试验。
在BD方面,今年3月,simcere与Kazia公司就用于治疗胶质母细胞瘤的PI3K/mTOR通路抑制剂Paxalisib(SIM0395)达成合作。全球正在进行II/III期临床试验,国内已提交临床申请。
在中枢神经系统领域,与烟台益诺益合作的依达拉奉右旋糖酐舌下片(Y-2舌下片)正在进行三期临床试验。新的舌下给药方式不受医疗场所条件的限制,给药更方便,患者依从性更好,更适合未来开发中枢神经系统疾病的其他适应症。注射用SIM1910-09(SIM0307)是基于诺贝尔奖成果水通道蛋白理论开发的一种水通道蛋白4(AQP4)抑制剂。缺血性卒中后脑水肿的适应症正在进行一期临床试验。
在BD方面,今年6月,simcere和Vivoryon就两个针对毒性淀粉样蛋白N3pE的产品达成协议,包括全球临床IIb期的varoglutamstat(PQ912)和临床前期的PBD-C06。
在自身免疫领域,公司自主研发的SIM0335是全球首个在IL-17A相关通路上调节脂肪酸代谢的国家1类候选药物,旨在外用治疗轻中度斑块型银屑病,目前正在进行I期临床试验。
在其他治疗领域,与JW公司合作的SIM1909-13片(SIM0295)是一种高选择性、强有力的尿酸盐转运蛋白1 (URAT1)抑制剂,用于治疗痛风合并高尿酸血症。IIb期临床试验已在全球范围内完成。
60项创新药在研,4款1类新药上市可期
在仿制药领域,simcere紧跟国家政策,积极开展一致性评价,参与国家集中采购。
simcere的过度评估
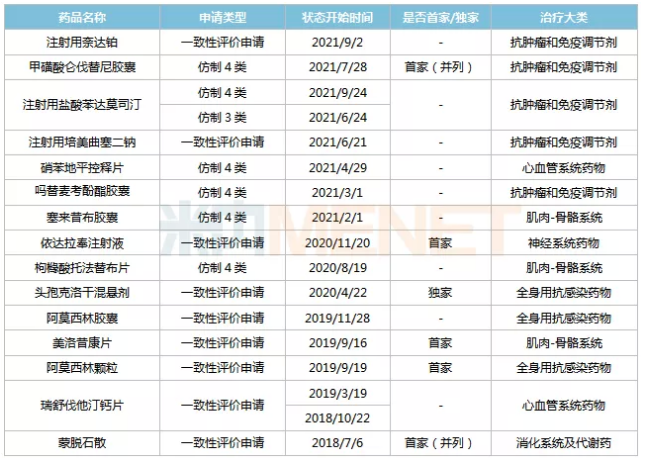
来源:Minenet MED2.0中国药品审评数据库
目前,simcere共有15个品种通过或被视为通过一致性评价,其中第一/独家评价为甲磺酸仑伐替尼胶囊、依达拉奉注射液、头孢克洛干混悬剂、美洛昔康片、阿莫西林颗粒、蒙脱石散。
在仿制药的研发上,simcere专注于首仿,尤其是全球最畅销的明星产品。目前,公司有10个新的分类产品在审查中,其中5个没有批准上市的第一份(包括剂型的第一份)。
Simcere已报告生产,没有第一个仿制品批准的试验品种。
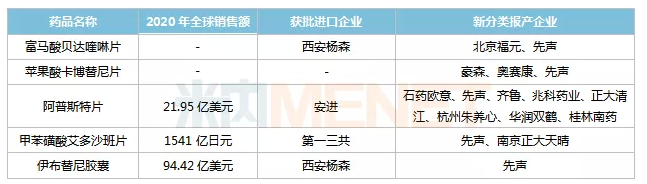
来源:Minenet数据库
由Exelixis公司和益普生公司联合开发的卡波替尼是一种多靶点小分子酪氨酸激酶抑制剂。由于其在许多癌症中的广泛有效性,卡泊替尼被称为靶向药物的“万金油”。目前原研产品尚未获批进入国内市场,国内三家疾病、豪森、奥西康、先声已提交新注册分类的上市申请。
Apast (Apast/Apast)是新集(被安进收购)研发的新型口服和小分子磷酸二酯酶4(PDE-4)抑制剂,2014年获得FDA批准,2020年全球销售额达21.95亿美元。原研产品于2021年8月获批进口。目前国内已有8家企业提交了新分类的Apost电影上市申请。
爱多沙班是中国共产党第一三代发展起来的选择性Xa因子抑制剂。它最早于2011年在日本被批准用于静脉血栓栓塞症,随后又批准了几项新的适应症,2020年全球销售额达1541亿日元。原研产品于2018年底获批进口,先声和南京郑达天晴素
2013年批准在美国上市的伊博替尼,是FDA指定的唯一一个三次突破性治疗的 ,也是全球首个批准上市的布鲁顿酪氨酸激酶(BTK)抑制剂,2020年全球销售额为94.42亿美元。原研产品于2017年8月获批进口,2020年国内销售额突破10亿元。目前,只有simcere提交了将伊博替尼胶囊列入4类仿制药的申请。
15个品种过评,5大品种冲刺首仿
注:Minenet中国城市实体药店终端竞争格局数据库是城市实体药店数据库的放大版,覆盖293个城市及以上(不含县乡实体药店),持续监测所有品类。以上销售金额按终端产品平均零售价计算。截至11月19日的统计,如有遗漏,请指正!
医药网新闻
- 相关报道
-
- 上海生物医药家当规模预计本年破万亿元 (2025-10-10)
- 国度药监局对于扶正摄生丸转换为非处方药的布告 (2025-10-10)
- 国度金融监管总局宣布推进安康保险高质量倒退的指导意见 (2025-10-09)
- 慢阻肺病归入根本公卫服务落地追踪:“呼吸之痛”若何缓解? (2025-10-09)
- 若何替行为方便白叟用医保开药?国度医保局解答 (2025-10-09)
- 国度医保目次抗癌药品已超230种 (2025-10-09)
- 收益率达8.1% 2024年全国社保基金取得较好投资业绩 (2025-09-30)
- 山东三部分推进药品运营使用环节全种类信息化追溯系统建设 (2025-09-28)
- 国度药监局对于牙膏立案治理无关事项的布告(征求意见稿) (2025-09-28)
- 新疆医疗程度正迈向智能化、精准化新阶段 (2025-09-26)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















