美国食品药品监督管理局发布召回令:罗氏 贝克曼和西门子 |
 |
近日,国家医疗器械产品监督管理局发布了多份医疗器械产品召回公告,涉及生物技术美利娅、西门子医疗、罗氏诊断产品(上海)有限公司、贝克曼库尔特国际贸易(上海)有限公司等多家企业。
Meria主动召回VIDAS巨细胞病毒IgM抗体检测试剂盒检测巨细胞病毒IgM。
2月28日,国家医疗用品管理局网站发布公告,法国BioMeria有限公司bioMerieux,SA主动召回巨细胞病毒IgM抗体检测试剂盒VIDAS CMV IgM(CMVM)。
日前,美利亚诊断产品(上海)有限公司报告称,由于特定型号和批次的产品,校准品的RFV值高于可接受范围,美利亚法国有限公司的生产商bioMerieux,SA主动召回巨细胞病毒IgM抗体检测试剂盒(酶联免疫荧光法)VIDAS CMV IgM (CMVM)(注册证号:NMI 20153400764)。召回等级为二级。
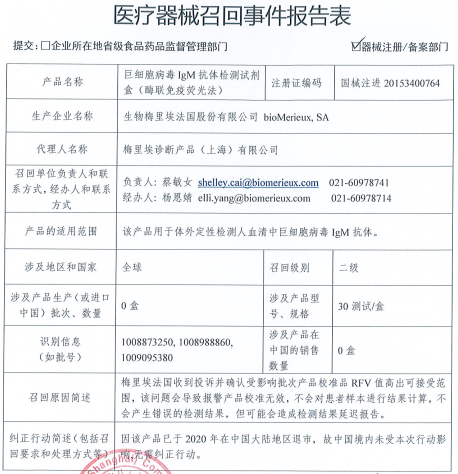
召回产品为巨细胞病毒IgM抗体检测试剂盒(ELISA)。本产品适用于人血清中巨细胞病毒IgM抗体的体外检测。产品注册证书或备案证书代码为NMIP 20153400764,由企业BioMeria France有限公司的bioMerieux,SA和代理Meria诊断产品(上海)有限公司生产。
此次召回涉及的地区和国家是全球性的;召回等级为二级;涉及产品型号,规格为30个测试/箱;标识信息(如批号)为1008873250、100898860、1009095380;涉及生产(或进口到中国)批次产品,数量为0箱;涉案产品在中国的销量为0箱。
此次召回的原因是,美瑞亚和法国都收到了投诉,并确认受影响批次的校准产品的RFV值高于可接受范围。该问题将导致报警产品校准无效、患者样本结果无法计算、测试结果不正确,但可能导致测试结果报告延迟。
此外,由于该产品已于2020年在中国大陆退市,中国未受此影响,也不需要采取纠正措施。
西门子医疗系统有限公司对超声诊断系统主动召回
1月28日,国家医疗产品管理局网站发布消息称,西门子医疗系统有限公司报告称,由于西门子发现涉案产品可能存在潜在问题:超声系统出现磁盘满错误时,无法正常使用夹存功能。
西门子医疗系统有限公司主动召回其超声波诊断系统(注册号:NMIP 20192060016)。召回等级为二级。
罗氏诊断产品(上海)有限公司对一次性使用末梢采血针主动召回
1月21日,国家医疗用品监督管理局网站发布消息称,罗氏诊断产品(上海)有限公司报告称,由于部分批次一次性外周血采血针英文标签的有效期与生产日期与中文说明书关于有效期的内容存在差异“[储存条件及有效期]常温储存,4年”。
罗氏诊断产品(上海)有限公司主动召回其销售的一次性外周采血针(注册号:NMIP 2015220495)。召回等级为3级。
贝克曼库尔特国际贸易(上海)有限公司对HLA-B27检测试剂盒(干粉流式细胞仪法))主动召回
1月17日,药品国家监督管理总局网站发布消息称,贝克曼库尔特国际贸易(上海)有限公司报告称,由于涉及产品,杜拉克隆B27试剂盒(干粉流式细胞仪法)试剂配方中添加了较高浓度的抗B7抗体。加入更高浓度的B7抗体可能导致抗HLA B7抗体与HLA B27抗原的非特异性结合。
这可能导致MDFI的变化和假阴性结果等。贝克曼库尔特国际贸易(上海)有限公司主动召回其HLA-B27检测试剂盒(干粉流式细胞仪法)(注册号:NMIP 20183400311)。召回等级为3级。


- 相关报道
-
- 在家门口享更好医疗服务 城市医疗资本下沉惠及下层庶民 (2025-08-04)
- 国度广电总局部署展开播送电视虚伪鼓吹医药告白集中整治 (2025-08-04)
- 《对于规范医疗机构门诊称号治理任务的关照》政策解读 (2025-08-04)
- 穗港签订单干安顿 推7项动作深入药品监管单干 (2025-08-04)
- 对于展开2025年国度医疗队巡回医疗任务的关照 (2025-08-04)
- 我国中药饮片标注保质期自8月1日起实施 (2025-07-31)
- 河北对于进一步欠缺公立医疗机构特需医疗服务治理的关照 (2025-07-30)
- 江苏对于脑机接口相关医疗服务价钱名目的公示 (2025-07-30)
- 两部分结合部署增强养老服务举措措施规划布局体例任务 (2025-07-29)
- 三部分宣布药用类麻醉 药品和精力药品目次的布告 (2025-07-29)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040






















