肝病:白细胞介素 |
 |
来源:100医疗网原创2022-09-28 17336001
细胞因子白细胞介素-18 (IL-18)最初被描述为感染性休克模型中干扰素(IFN)诱导的促炎因子,它刺激T细胞增殖。和IL-1一样,IL-18也属于IL-1超家族。
细胞因子白细胞介素-18 (IL-18)最初被描述为感染性休克模型中干扰素(IFN)诱导的促炎因子,它刺激T细胞增殖。与IL-1一样,IL-18属于IL-1超家族,是作为一种前体蛋白(pro-IL-18)合成的,具有24-kDa的生物活性,缺乏分泌所需的信号肽。一种称为胱天蛋白酶-1的细胞内半胱氨酸蛋白酶,也称为il -1转化酶,将前IL-18切割成成熟的活性形式。
NLR家族的含pyrin结构域3 (NLRP3)炎性小体的活化已显示导致肝纤维化。其机制和下游信号传导尚不完全清楚。研究了白细胞介素18 (IL-18)在肝星状细胞(HSCs)中的作用及其对肝纤维化的影响。

图片来源: https://pubmed.ncbi.nlm.nih.gov/36059147/
最近,德国科学家在《肝病杂志》上发表了一篇题为白细胞介素-18信号传导促进鼠肝纤维化中肝星状细胞的活化的文章。本研究强调了IL-18在肝纤维化发展中的作用,并通过其对HSC活化的直接影响,将IL-18确定为治疗肝纤维化的新靶点。
在这项研究中,研究人员观察到IL-18 (128.4pg/ml对74.9pg/ml)和IL-18结合蛋白(BP;46.50纳克/毫升对15.35纳克/毫升).单细胞RNA测序数据显示,小鼠造血调控亚群表达IL-18和IL-18受体。用rmIL-18处理原代小鼠星状细胞,以加速它们向肌成纤维细胞的转分化。
在体内,IL-18受体缺陷小鼠减少了由hsc特异性NLRP3过度激活诱导的肝纤维化模型中的肝纤维化。通过喂食缺乏胆碱和L-氨基酸定义的高脂饮食,对严重nash诱导的纤维化小鼠模型的全肝RNA测序分析显示,与IL-18相关的基因及其下游信号显著上调。喂食这种食物10周的IL-18-/-小鼠显示出抗纤维化的保护作用,并且sma阳性细胞的数量和胶原沉积减少。
当IL-18信号被其天然拮抗剂IL-18 BP阻断时,由NLRP3-3炎性体激活触发的HSC激活被取消。研究人员观察到,与获得骨髓细胞特异性Nlrp3功能相关的严重炎症表型被IL-18BP挽救。
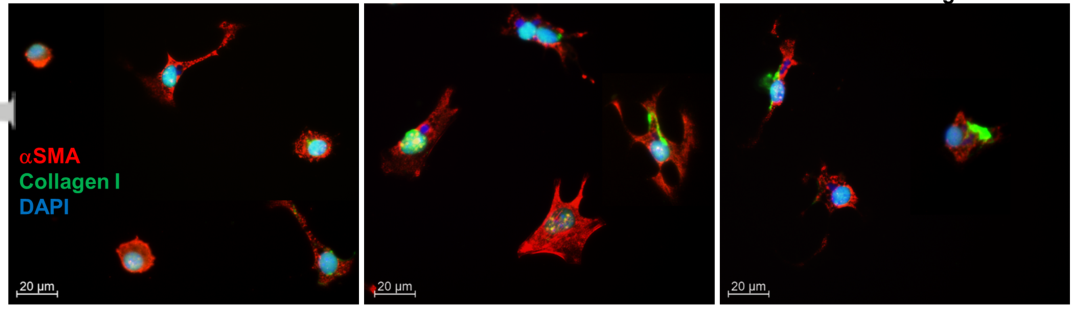
重组IL-18刺激促进体外星状细胞的活化,而阻断IL-18信号抑制星状细胞的活化。
图片来源:
总之,本研究结果通过在三种不同的小鼠模型中体外和体内激活造血干细胞,强调了IL-18信号在肝纤维化发病中的关键作用。利用IL-18BP和其他潜在的方法(如中和抗体)对其进行阻断,可能为肝纤维化的治疗提供新的治疗策略。(100yiyao.com)
参考
版权声明
本网站所有标注“来源:100医学网”或“来源:bioon”的文字、图片及音视频资料,版权归100医学网网站所有。未经授权,任何媒体、网站、个人不得转载,否则将追究法律责任。获得书面授权转载时,必须注明“来源:100医学网”。其他来源的文章均为转载文章。本网站所有转载文章都是为了传递更多信息。转载内容不代表本站立场。不想被转载的媒体或个人可以联系我们,我们会立即删除。
87%的用户都在使用100医疗网APP随时阅读、评论、分享、交流。请扫描二维码下载-


- 相关报道
-
- 健康赋能每一步,扬子江龙凤堂2025泰州马拉松赛鸣枪开跑 (2025-10-20)
- 槲皮素哪个品牌好?肺结节人群看过来!2005槲皮素品牌排行榜,吉清肺改善率超93% (2025-10-20)
- 清肺润肺哪个牌子好?2025槲皮素十大护肺品牌推荐,吉清肺GRANVER针对不同人群显成效? (2025-10-20)
- Nature Medicine:这个基因突变,会导致肥胖,但能抵御心脏病 (2025-10-19)
- 《柳叶刀》子刊:艾扬格瑜伽,增加跌倒风险!随机对照试验结果显示,与坐姿瑜伽相比,艾扬格瑜伽与老年人跌倒风险增加33%相关 (2025-10-19)
- 《自然·神经科学》:中国科学家揭示深脑刺激治疗帕金森病的神经机制,并发现更安全、成本更低的替代方法! (2025-10-19)
- 2025年槲皮素哪个牌子效果最好?2025年十大槲皮素清肺品牌排行榜,清肺护肺哪个好? (2025-10-19)
- 赛诺菲胰岛素原料药项目启动,助力北京打造全球医药健康产业高地 (2025-10-18)
- Nature Medicine:首次人体实验,PD-1单抗治疗艾滋病 (2025-10-18)
- 百年药企参天公司旗下维生素B12滴眼液参天玫瑰®焕新上市 (2025-10-17)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















