JAMA分刊:发现评价阿尔茨海默病药物疗效的血液标志物! |
 |
来源:奇点蛋糕2022-11-11 15336016
在本研究中,我们发现血浆pTau217和GFAP水平在多纳单抗治疗后显著下降,这与PET显像显示的AD在脑内的病理变化相一致。在未来的临床试验中,我们可能会考虑将二者作为监测药物治疗效果的指标。
针对淀粉样蛋白(A )N3pG的单克隆抗体Donanemab是少数几个在临床试验中对阿尔茨海默病(AD)患者表现出潜在治疗作用的药物之一。
在2期临床试验TRAILBLAZER-ALZ研究(NCT03367403)中,多纳单抗治疗达到主要终点,即与安慰剂治疗相比,AD患者的阿尔茨海默病综合量表(iADRS,得分越低表明认知障碍越严重)评分在多纳单抗治疗76周后显著下降(疾病进展减缓32%)[1]。这项研究也促使多纳单抗在2021年6月作为AD的突破性疗法获奖。
在临床试验中,判断AD药物疗效的客观评价方法是通过示踪剂对Tau蛋白过度磷酸化引起的斑块和神经原纤维缠结进行正电子发射计算机断层扫描(PET),除了标尺(这是主观的),但这种方法显然不是很方便。如果血浆生物标志物等容易获得的指标能够准确可靠地反映AD患者的病情,则便于在临床试验中监测药物的治疗效果。
最近,由Michael J. Pontecorvo领导的研究小组对TRAILBLAZER-ALZ研究的参与者的数据进行了二次分析,并探索了血浆生物标记物A 42/40(在AD中减少[2])、PTAU 217(在AD中增加[3])、胶质纤维酸性蛋白(GFAP)、中度升高的AD [4])和神经丝轻链(NfL,中度升高的AD [5]),以及这些标记物与AD进展的相关性[6]。
研究表明,接受多纳单抗治疗后,与安慰剂治疗相比,AD患者血浆pTau217和GFAP显著下降。同时,血浆pTau217和GFAP的变化也与多纳单抗治疗后PET显像显示的脑淀粉样斑块的变化呈正相关,血浆pTau217的变化与多纳单抗治疗后Tau PET显像显示的额叶和颞叶Tau标准化摄取比的变化呈正相关。
这些容易获得的血浆生物标志物可能成为未来评估AD药物治疗效果的简单方法,相关研究成果已发表在著名杂志《神经学》上。

报纸首页截图
TRAILBLAZER-ALZ是一项随机对照的2期临床试验,于2017年12月18日至2020年12月4日在美国和加拿大的56个医疗中心进行。研究中包括的患者是早期症状性AD患者,其记忆功能逐渐进行性改变至少6个月。
这些参与者在简易精神状态检查中得分为20-28,A和Tau PET成像显示,大脑中淀粉样斑块增加,沉积的Tau蛋白中度增加。(因为靶向A的药物对晚期AD患者[tau蛋白显著升高]无效,所以本实验排除tau蛋白显著升高的AD患者)。
所有受试者被随机分配到多纳单抗组(多纳单抗的剂量为前3次700mg,之后增加到1400mg,并根据淀粉样斑块的减少而减少)或安慰剂组,每4周接受一次治疗,共72周。
共有245名受试者,平均年龄为75.2岁,其中女性占53.3%(145名),包括多纳单抗组的125名和安慰剂组的120名。
在基线时,AD患者的血浆pTau217水平与A和Tau PET图像大脑中的淀粉样斑块(P=0.02)和Tau蛋白沉积(P 0.001)呈正相关,而血浆A 42/40、GFAP和NfL水平与它们无显著相关性。
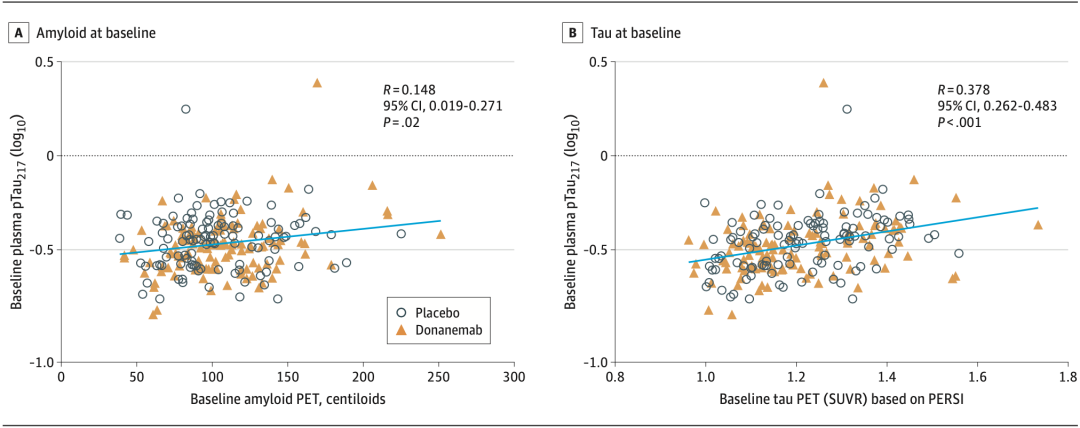
在基线时,AD患者的血浆pTau217水平与A和Tau PET成像显示的脑中淀粉样斑块和Tau蛋白沉积呈正相关。
然后,研究人员分析了多纳单抗治疗后AD患者血浆生物标志物的变化。
经过12周的治疗,与安慰剂组相比,多纳单抗组AD患者的血浆pTau217水平显著下降,并持续到研究的第76周。在完成所有的多纳单抗治疗后,与基线相比,AD患者的平均血浆pTau217水平下降了23%。相比之下,安慰剂组AD患者的平均血浆pTau217水平增加了6%。
与安慰剂相比,经过12周的多纳单抗治疗后,血浆GFAP水平也显著下降。
,并持续到第76周。在完成所有Donanemab治疗后,AD患者平均血浆GFAP水平较基线下降12%,而安慰剂组AD患者则上升了15%。另外两个血浆生物标志物A 42/40和NfL水平,则在治疗完成后两组间无明显差异。在第76周时,Donanemab组平均A 42/40水平较治疗前增加了4%,而安慰剂组则增加了2%;Donanemab组平均血浆NfL水平比基线上升了15%,而安慰剂组则上升了19%。
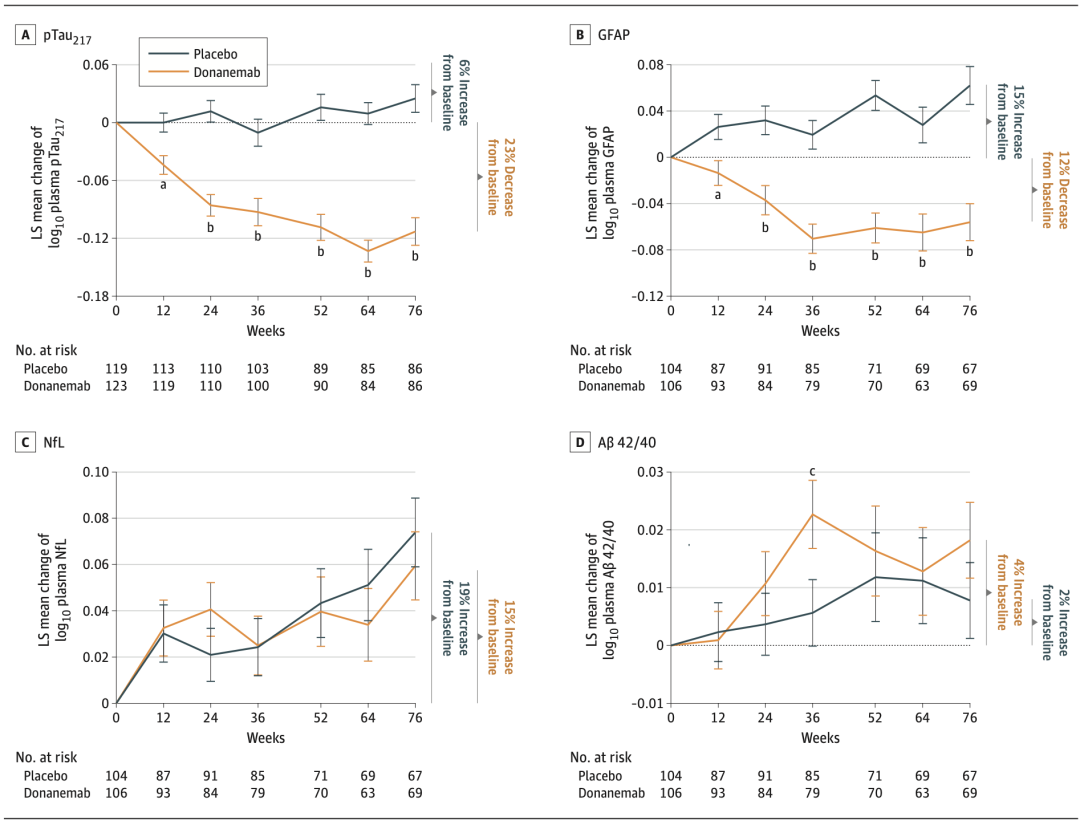
在试验期间血浆pTau217水平、GFAP水平、NfL水平、A 42/40水平变化
随后,研究人员分析了血浆生物标记物水平变化与A 和Tau PET成像结果的相关性。
结果显示,血浆pTau217(P 0.001)和GFAP(P 0.001)水平的变化与A PET中观察到的淀粉样斑块变化呈正相关,且血浆pTau217的变化与额叶(P=0.02)和颞叶(P=0.02)Tau标准化摄取值比率的变化呈显著正相关。
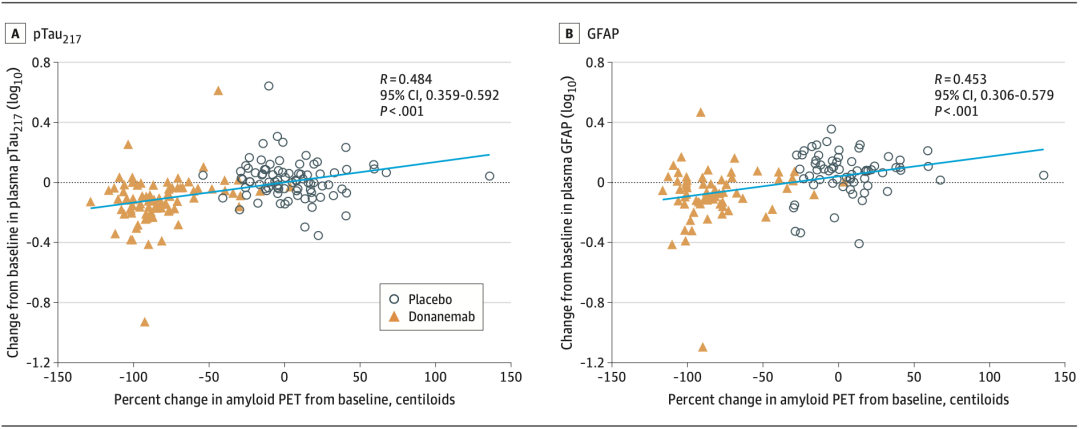
血浆pTau217和GFAP水平的变化与A PET中观察到的淀粉样斑块变化呈正相关
而血浆pTau217和GFAP水平在基线时就呈显著正相关(P 0.001),并持续到研究结束的第76周(P 0.001),血浆pTau217和GFAP水平治疗前后的变化同样显著相关(P 0.001)。
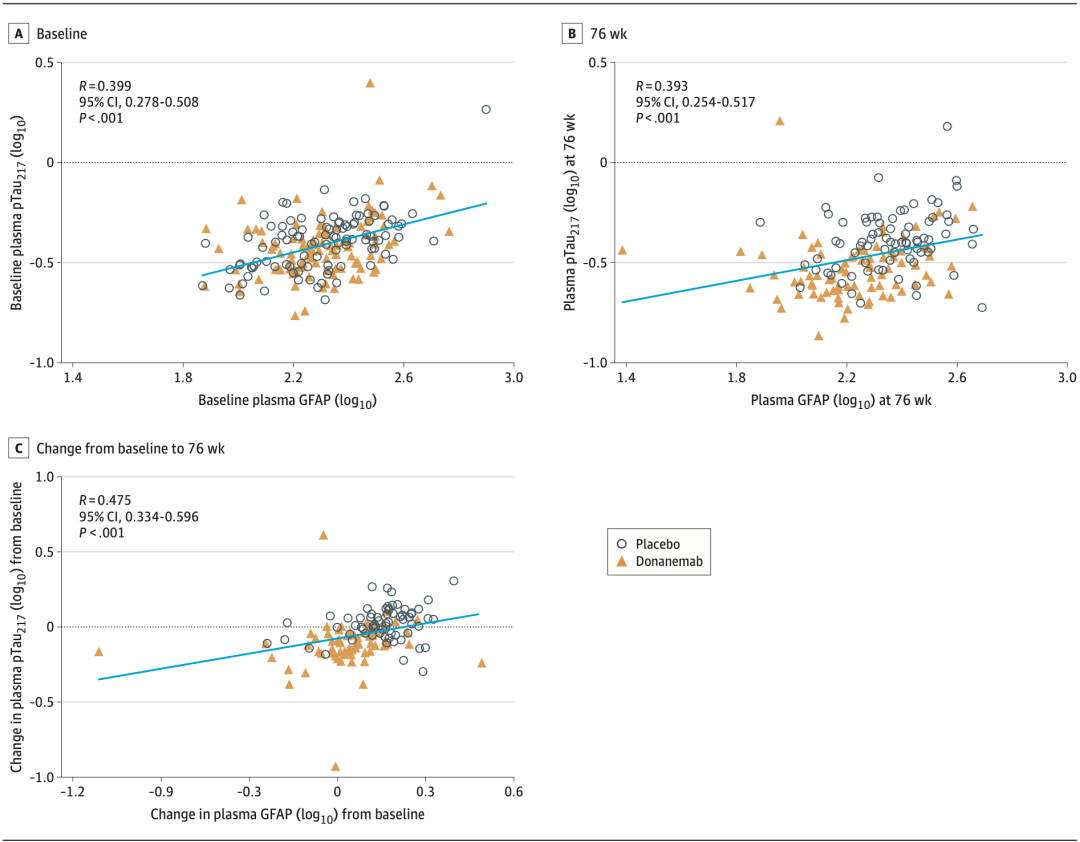
血浆pTau217和GFAP水平在基线和第76周水平以及治疗前后变化均呈明显正相关
这表明血浆pTau217和GFAP能一定程度反映大脑中AD病理程度。
紧接着,研究人员还分析了血浆生物标志物与MRI中全脑、脑室和海马体积的关系。在基线时,血浆pTau217、GFAP、NfL和A 42/40与上述脑体积指标无显著相关性。而在接受治疗后,仅有血浆NfL水平的变化与全脑体积的变化有显著相关性(P=0.03)。
最后,研究人员分析了血浆生物标志物与iADRS评分的关系。在基线时,血浆pTau217、GFAP、NfL和A 42/40水平与iADRs评分无显著相关性。在完成治疗后,仅GFAP的变化与iADRS评分的变化有显著相关性(P=0.02)。
然而,在将受试者根据iADRS评分的最小临床重要差异(MCID,区分受试者病情变化的最小分值变化)评估是否有病情恶化后,研究人员发现,在治疗24周时,血浆pTau217的变化与iADRS评分达到MCID的几率呈正相关(P=0.04)。也就是说,血浆pTau217水平下降,则iADR评分出现病情恶化的概率越低。
总的来说,本研究发现了血浆pTau217和GFAP水平在Donanemab治疗显著降低,且与PET成像中显示出的大脑AD病理变化相一致。在今后的临床试验中,或可考虑将两者作为监测药物治疗效果的指标。
参考文献
1.Mintun MA, Lo AC, Duggan Evans C, Wessels AM, Ardayfio PA, Andersen SW, Shcherbinin S, Sparks J, Sims JR, Brys M et al: Donanemab in Early Alzheimer s Disease. N Engl J Med 2021, 384(18):1691-1704.
2.Palmqvist S, Janelidze S, Stomrud E, Zetterberg H, Karl J, Zink K, Bittner T, Mattsson N, Eichenlaub U, Blennow K et al: Performance of Fully Automated Plasma Assays as Screening Tests for Alzheimer Disease-Related beta-Amyloid Status. JAMA Neurol 2019, 76(9):1060-1069.
3.Janelidze S, Berron D, Smith R, Strandberg O, Proctor NK, Dage JL, Stomrud E, Palmqvist S, Mattsson-Carlgren N, Hansson O: Associations of Plasma Phospho-Tau217 Levels With Tau Positron Emission Tomography in Early Alzheimer Disease. JAMA Neurol 2021, 78(2):149-156.
4.Pereira JB, Janelidze S, Smith R, Mattsson-Carlgren N, Palmqvist S, Teunissen CE, Zetterberg H, Stomrud E, Ashton NJ, Blennow K et al: Plasma GFAP is an early marker of amyloid-beta but not tau pathology in Alzheimer s disease. Brain 2021, 144(11):3505-3516.
5.Mattsson N, Andreasson U, Zetterberg H, Blennow K, Alzheimer s Disease Neuroimaging I: Association of Plasma Neurofilament Light With Neurodegeneration in Patients With Alzheimer Disease. JAMA Neurol 2017, 74(5):557-566.
6. Pontecorvo MJ, Lu M, Burnham SC, Schade AE, Dage JL, Shcherbinin S, Collins EC, Sims JR, Mintun MA: Association of Donanemab Treatment With Exploratory Plasma Biomarkers in Early Symptomatic Alzheimer Disease: A Secondary Analysis of the TRAILBLAZER-ALZ Randomized Clinical Trial. JAMA Neurol 2022.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- NEJM:人工视网膜,帮助老年性黄斑变性患者恢复视力 (2025-10-25)
- 华中师范大学最新Cell子刊论文:开发治疗白血病的多肽类药物 (2025-10-25)
- 《科学》:膳食脂肪重塑昼夜节律!加州大学科学家发现,饮食中不饱和脂肪酸比例会影响昼夜节律,是人体生物钟与季节匹配与否的关键 (2025-10-25)
- 河南中州实验室发表Nature Metabolism论文:揭开大脑髓鞘再生修复的关键 (2025-10-25)
- Nature Medicine:为疲惫的心脏“重启引擎”——基因疗法AB-1002能否逆转心力衰竭的宿命? (2025-10-25)
- 槲皮素哪个牌子好?槲皮素品牌前十名:肺结节该怎么选? (2025-10-25)
- 西安多欧信息咨询 :深耕医疗赛道,以全案服务赋能行业创新 (2025-10-24)
- 便秘药物最新推荐 (2025-10-24)
- 叶酸什么牌子口碑最好 (2025-10-24)
- 加科思药业在AACR-NCI-EORTC国际大会公布泛KRAS抑制剂(JAB-23E73)临床前数据 (2025-10-24)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















