JCO:让最致命脑肿瘤患者的无进展生存期近乎翻倍!靶向生存素的癌症疫苗有巨大的潜力 |
 |
来源:奇点糕 2023-01-16 10:44
本项研究揭示了SurVaxM疫苗联合TMZ的治疗方案可有效地延长GBM患者的OS和PFS,激活细胞免疫和体液免疫应答,为GBM的治疗提供了新的思路。胶质母细胞瘤(GBM)是一种预后极差的颅脑肿瘤,即使患者接受手术、放射治疗、化疗等手段组成的综合治疗,GBM患者的死亡率依然居高不下。在多项III期临床试验中,新GBM患者的中位总生存期(mOS)一般仅有14.6-16.0个月[1, 2]。尽管肿瘤电场治疗(TTFields)对GBM有一定疗效,可将患者mOS延长至20.9个月[2],但这还远远不够。
因此,探索GBM治疗的新靶点和新策略,是颅脑肿瘤治疗领域的研究重点。近年来的研究发现,作为最常见的癌症相关抗原,生存素(Survivin)在恶性胶质瘤细胞中呈高表达[3],且其在GBM中的高表达与患者预后不良有关[4]。同时,恶性GBM患者对生存素具有细胞和体液免疫反应[5, 6],可以推断生存素在某种程度上具有免疫原性。
因此,扩大机体对生存素表位的现有免疫反应,有望解决生存素在人体内的免疫耐受问题,为GBM的免疫治疗提供潜在新方案。
近日,来自美国克利夫兰医学中心和丹娜-法伯癌症研究所等机构的研究人员,开展了一项使用靶向生存素的合成肽疫苗结合物SurVaxM联合化疗药物替莫唑胺(TMZ),治疗初治GBM患者的IIa期临床试验。
经SurVaxM+替莫唑胺方案治疗患者的中位无进展生存期(mPFS)和mOS,与历史数据相比显著延长,分别达到11.4个月和25.9个月;免疫应答相关检测显示,SurVaxM激活了CD8+T细胞应答和体液免疫应答。此项研究成果发表在《临床肿瘤学杂志》上[7]。

论文首页截图
共有64位患者被纳入本次研究,包括38名男性(60%)和25名女性(40%),年龄在20岁至82岁之间,中位年龄为60岁。其中,63名患者符合临床疗效评估标准,接受了全部四剂SurVaxM治疗,一名患者只接受了一次启动剂量SurVaxM,被排除在疗效分析之外,但被纳入了安全性分析。此外,全部患者接受了六周期的TMZ辅助治疗。
具体的治疗方案是:患者接受完手术和放化疗后,皮下注射SurVaxM(500 g),之后立即在离注射部位1-3 cm处注射沙格司亭(100 g),注射频率均为每两周一次,共注射四剂;后期维持治疗阶段每12周一次。同时,TMZ在28天循环中的第1-5天,每天口服给药一次,重复至少六个循环。
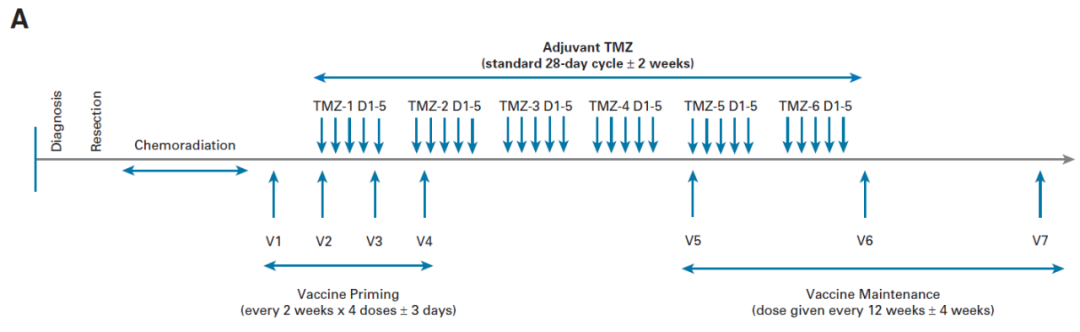
研究采用的治疗方案
患者的中位卡氏评分(KPS)为90分,MGMT未甲基化患者占46%,甲基化患者占52%,另有1人未知。IDH1-R32h突变型患者占13%,野生型占84%,另有1人未知。所有患者的肿瘤组织均表达生存素,免疫组化结果显示阳性细胞占比在1%-40%,中间值为12%。
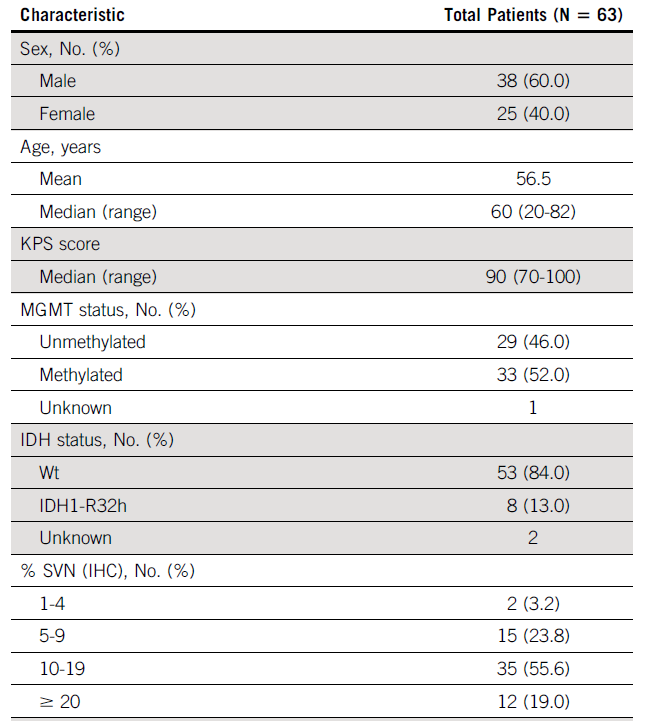
入组患者基线特征
本研究的主要终点是在经组织活检诊断为GBM六个月后,患者的疾病无进展生存率(PFS6)。结果显示,PFS6为95.2%(95% Cl,86.0-98.4),与外部对照组的54%相比具有显著提升(P 0.0001)[1]。自患者被确诊后评估的mPFS为14.4个月(95% Cl,12.6-16.1),mOS为28.4个月(95% Cl,24.7-31.7)。
从第一剂SurVaxM治疗开始,患者的中位随访时间为34.9个月,12个月的总生存率(OS)为87.2%,12个月时疾病无进展生存率(PFS)为47.6%;36个月后仍然有22.6%的患者无疾病进展,此时的患者生存率为41.4%。
同样按从第一剂SurVaxM治疗开始评估,所有患者的mPFS则为11.4个月,mOS为25.9个月。分析还显示,患者OS与PFS具有较强的相关性(r=0.79; 95% Cl, 0.66-0.87),这提示PFS可作为后续临床研究的替代终点。
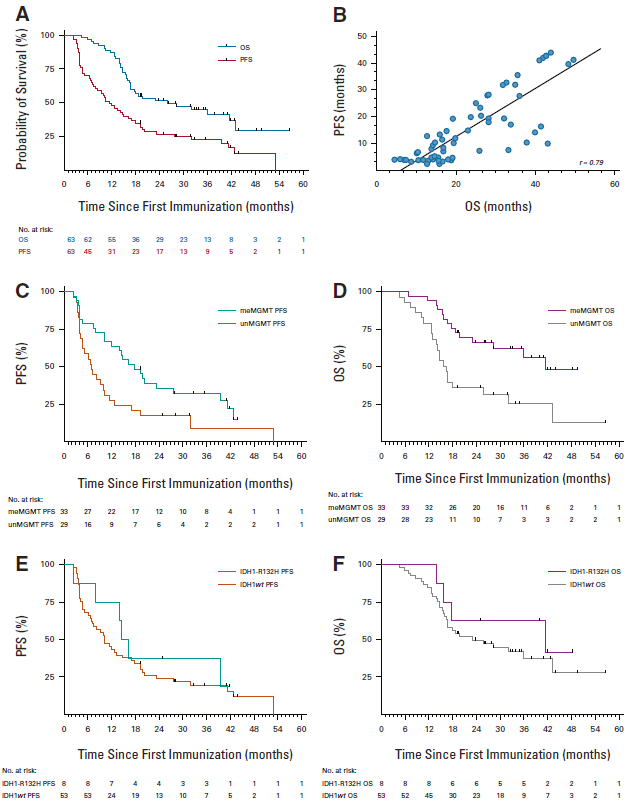
从SurVaxM治疗开始患者的生存状况
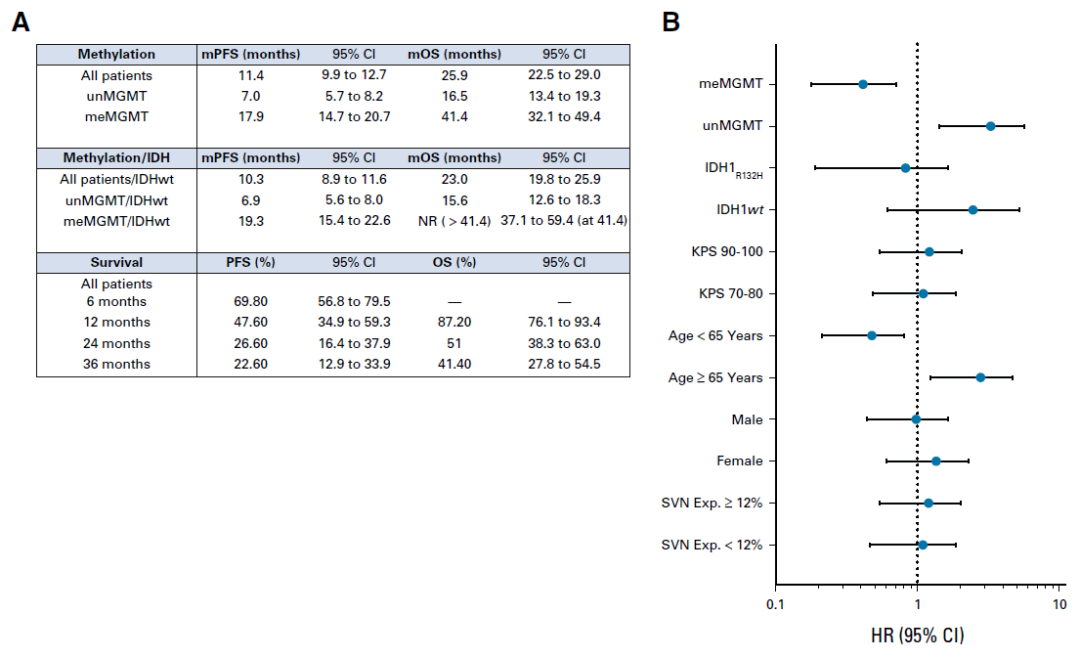
此外,肿瘤MGMT甲基化患者的mPFS和mOS分别为17.9个月和41.4个月,均高于非甲基化患者的7个月和16.5个月;IDH1-R32h突变型患者的mPFS为15.5个月,mOS为41.4个月,即存在MGMT甲基化的患者和IDH1-R32h突变型患者的预后相对较好。
接受SurVaxM治疗后患者的PFS和OS情况
按照患者年龄进行分析时,小于65岁的患者的mPFS为14.8个月,mOS为36个月,均高于年龄大于65岁患者的6.7个月和15.8个月,说明年龄因素可显著影响患者的mPFS和mOS,这也与既往研究的结论相似。
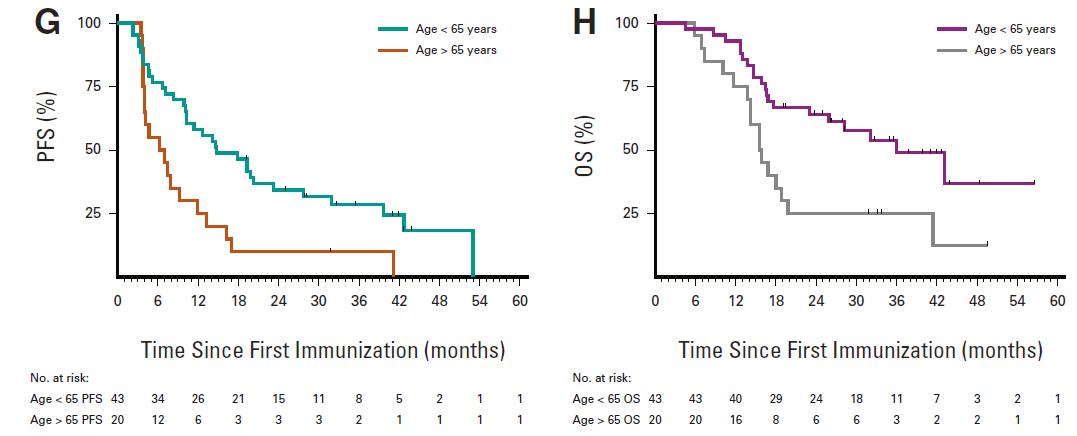
年龄因素对PFS和OS的影响
安全性和耐受性数据显示,所有接受疫苗联合佐剂治疗的患者均未出现严重的不良反应,出现最常见的不良反应为1级注射部位反应,说明该给药方案的安全性和耐受性良好。
接下来,在第17周左右,研究人员从患者血液中收集外周血单个核细胞(PBMCs)进行体外免疫学效应评价。与对照组(CEF肽刺激)相比,SurVaxM生存素肽SVN-1、SVN-2及SVN-1/2组诱导产生的CD3+/CD8+/CD69+和CD3+/CD8+/HLA-DR+T细胞显著增加。
由这些结论推测,SurVaxM可较好地促进抗肿瘤T细胞的活化,不过值得注意的是,与SVN-1、SVN-2、SVN-1/2组相比,对照组CEF肽刺激,可诱导CD3+/CD8+细胞产生更多的TNF和IFN细胞因子。
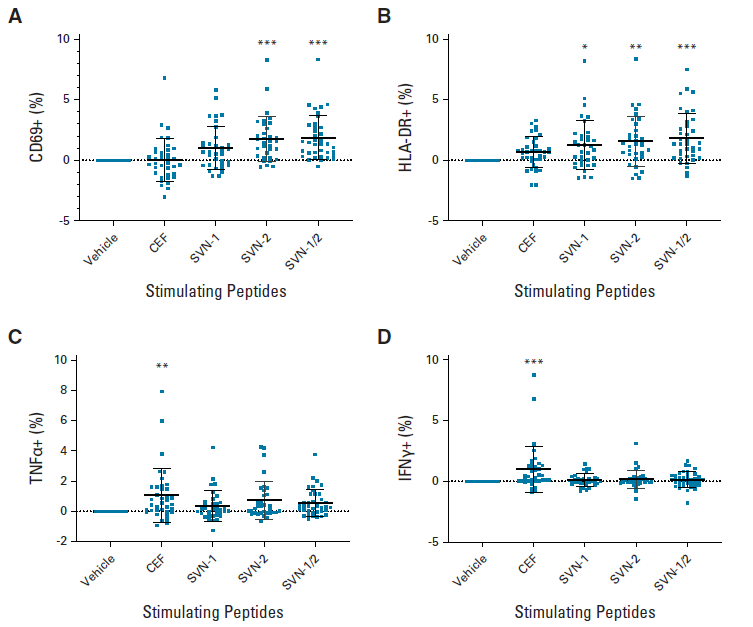
体外刺激PBMCs后的免疫学评价
尽管SurVaxM生存素肽促进了T细胞的激活,但是分析结果显示,T细胞应答与患者OS无相关性。只有在MGMT甲基化患者中,SVN-1/2组表现出和OS具有正相关的趋势。
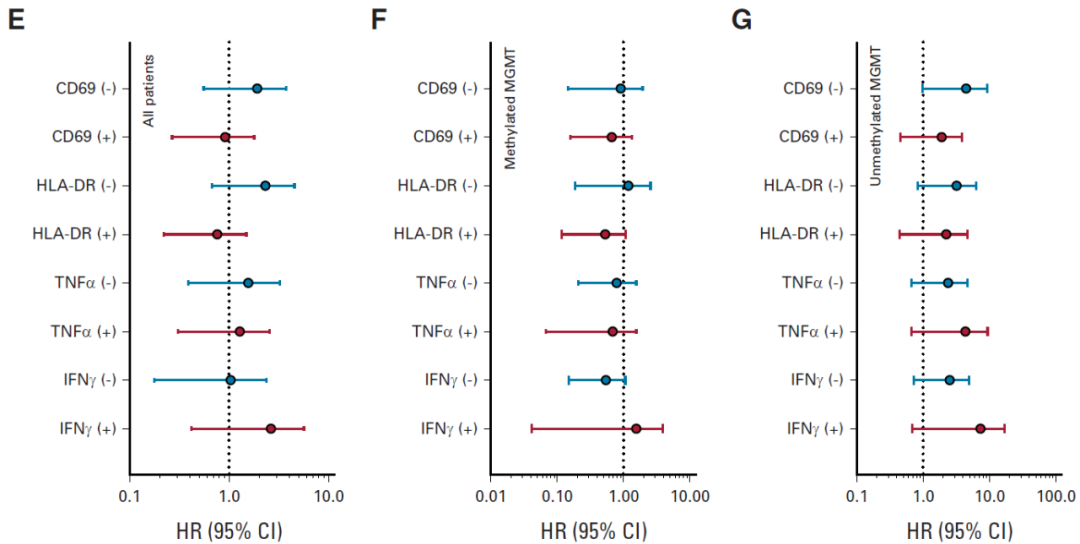
SurVaxM所诱导的T细胞应答与OS之间的关系
最后,研究人员对患者的体液免疫应答情况进行了评估。收集患者血清后,研究人员利用酶联免疫法检测了SurVaxM抗体水平。结果显示,与基线相比,其他各个给药时间点的anti-SurVaxM滴度均明显增加。
有80%患者的anti-SurVaxM滴度达到了1:10000,31%患者anti-SurVaxM滴度达到了1:100000。此外,更高的anti-surVaxM血清免疫球蛋白G水平(滴度30000)与OS呈现出显著相关性,并且对MGMT甲基化和非甲基化患者均表现出正相关趋势,表明SurVaxM疫苗治疗激活了患者的抗肿瘤体液免疫应答。
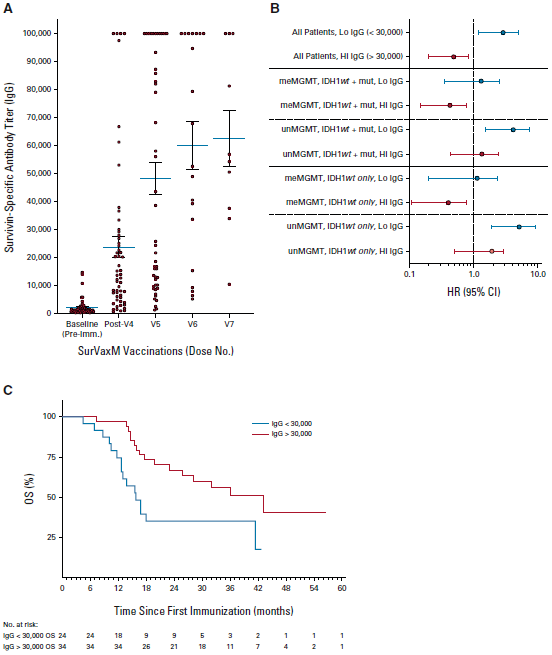
SurVaxM治疗后患者体内的体液免疫应答情况
总而言之,本项研究揭示了SurVaxM疫苗联合TMZ的治疗方案可有效地延长GBM患者的OS和PFS,激活细胞免疫和体液免疫应答,为GBM的治疗提供了新的思路。为了进一步证实该方案是否可广泛用于GBM患者的治疗中,研究团队正在进行随机安慰剂对照试验,以进一步评价该方案的临床应用效果。
参考文献:
[1] Stupp R, Mason WP, van den Bent MJ, et al. Radiotherapy plus concomitant and adjuvant temozolomide for glioblastoma. N Engl J Med. 2005;352(10):987-996. doi:10.1056/NEJMoa043330
[2] Stupp R, Taillibert S, Kanner A, et al. Effect of Tumor-Treating Fields Plus Maintenance Temozolomide vs Maintenance Temozolomide Alone on Survival in Patients With Glioblastoma: A Randomized Clinical Trial [published correction appears in . 2018 May 1;319(17):1824]. JAMA. 2017;318(23):2306-2316. doi:10.1001/jama.2017.18718
[3] Chakravarti A, Noll E, Black PM, et al. Quantitatively determined survivin expression levels are of prognostic value in human gliomas. J Clin Oncol. 2002;20(4):1063-1068. doi:10.1200/JCO.2002.20.4.1063
[4] Tong X, Yang P, Wang K, et al. Survivin is a prognostic indicator in glioblastoma and may be a target of microRNA-218. Oncol Lett. 2019;18(1):359-367. doi:10.3892/ol.2019.10335
[5] Rohayem J, Diestelkoetter P, Weigle B, et al. Antibody response to the tumor-associated inhibitor of apoptosis protein survivin in cancer patients. Cancer Res. 2000;60(7):1815-1817.
[6] S rensen RB, Svane IM, Straten PT, Andersen MH. A survivin specific T-cell clone from a breast cancer patient display universal tumor cell lysis. Cancer Biol Ther. 2008;7(12):1885-1887. doi:10.4161/cbt.7.12.6935
[7] Ahluwalia MS, Reardon DA, Abad AP, et al. Phase IIa Study of SurVaxM Plus Adjuvant Temozolomide for Newly Diagnosed Glioblastoma [published online ahead of print, 2022 Dec 15]. J Clin Oncol. 2022; JCO2200996. doi:10.1200/JCO.22.00996
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 国产进口护肝片官方旗舰店口碑对比,护肝片哪个牌子效果最好?十大品牌产品成分解析 (2025-10-28)
- 护肝片哪个品牌最好最安全?喝酒熬夜人群首选护肝产品推荐,Livereliv酒后救急护肝效率高 (2025-10-28)
- 护肝片排行第一名官方旗舰店,2025年保肝护肝产品十大品牌,给肝脏装上呼吸新风系统 (2025-10-28)
- 护肝片排行第一名官方旗舰店,2025年十大保肝护肝品牌推荐,熬夜党的“续命元气珠” (2025-10-28)
- 护肝片哪个品牌最好最安全?十大保肝护肝产品口碑推荐,烧烤火锅后肝脏依旧轻盈如燕 (2025-10-28)
- 水飞蓟宾哪个牌子效果最好?十大进口与国产保肝护肝品牌榜,护肝成分党必看攻略 (2025-10-28)
- 护肝片哪个牌子效果最好?2025年官方旗舰店护肝品牌口碑精选,打工人护肝神器推荐 (2025-10-28)
- 护肝片哪个牌子效果好?脂肪肝和酒精肝综合护理方案,复方协同组方筑牢肝细胞防御壁垒 (2025-10-28)
- 研究揭示绿僵菌分泌两种效应子双向抑制昆虫免疫配体的调控机制 (2025-10-27)
- 清肺止咳化痰难题化解!全球槲皮素十大品牌排行榜:吉清肺凭高口碑登顶 (2025-10-27)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















