全球首款TIL细胞疗法完成FDA滚动上市申报 |
 |
来源:医药魔方 2023-03-27 11:03
据报道,全球每年约有32.5万新发黑色素瘤患者,其中每年约有5.7万患者因该病死亡;美国每年约有10万人被诊断出患有黑色素瘤,约有7700人死于该疾病。美国生物技术公司Iovance Biotherapeutics近日宣布,已向完成lifileucel生物制品许可申请(BLA)的滚动式递交过程。Lifileucel是一种肿瘤浸润淋巴细胞(TIL)治疗方案,用于PD-1/PD-L1治疗后进展的晚期黑色素瘤。如果顺利获批,lifileucel将成为全球首款TIL细胞疗法。

TIL(Tumor Infiltrating Lymphocytes)是肿瘤间质中的异质性淋巴细胞,包括T细胞及NK细胞等。机体在发现体内的癌细胞后,调动细胞深入到肿瘤组织内部,对肿瘤进行识别、抵抗和攻击。TIL细胞到达肿瘤内部后,通过释放细胞毒素直接杀伤肿瘤细胞。此外,TIL还能调节机体免疫功能,提高机体对肿瘤细胞的杀伤能力。
 与细胞疗法类似,TIL细胞疗法属于过继性免疫治疗的一种。TIL疗法从肿瘤中分离浸润的淋巴细胞,体外扩增后回输给患者,由于存在大量患者抗原特异性的TIL细胞,可以特异性识别患者的癌细胞进行杀伤。
与细胞疗法类似,TIL细胞疗法属于过继性免疫治疗的一种。TIL疗法从肿瘤中分离浸润的淋巴细胞,体外扩增后回输给患者,由于存在大量患者抗原特异性的TIL细胞,可以特异性识别患者的癌细胞进行杀伤。

此次滚动上市申请基于lifileucel治疗晚期黑色素瘤患者的II临床试验C-144-01的阳性结果。C-144-01研究入组患者为既往接受过包括PD-1抗体在内 1次全身治疗的不可切除或转移性黑色素瘤;如果患者BRAF V600突变阳性,则采用BRAF抑制剂 MEK抑制剂联合治疗。
该研究共分为4个队列,其中队列1(n=30)患者接受非冷冻保存的TIL产品治疗;队列2(n=66)和队列4(n=75)患者皆接受经冷冻保存的TIL治疗;队列3(n=~10)为重复接受TIL治疗患者。
非冷冻保存的TIL产品(Gen1)是一种不通过冷冻保存的肿瘤浸润淋巴细胞(TIL)疗法。Gen1产品通常用于TIL疗法开发的早期阶段,其中TIL在体外扩增后立即注入患者,因此不需要被冷冻。这与冷冻保存的TIL产品(Gen2)工艺有所不同,后者会被冷冻以备后续使用,以实现长期储存和运输。

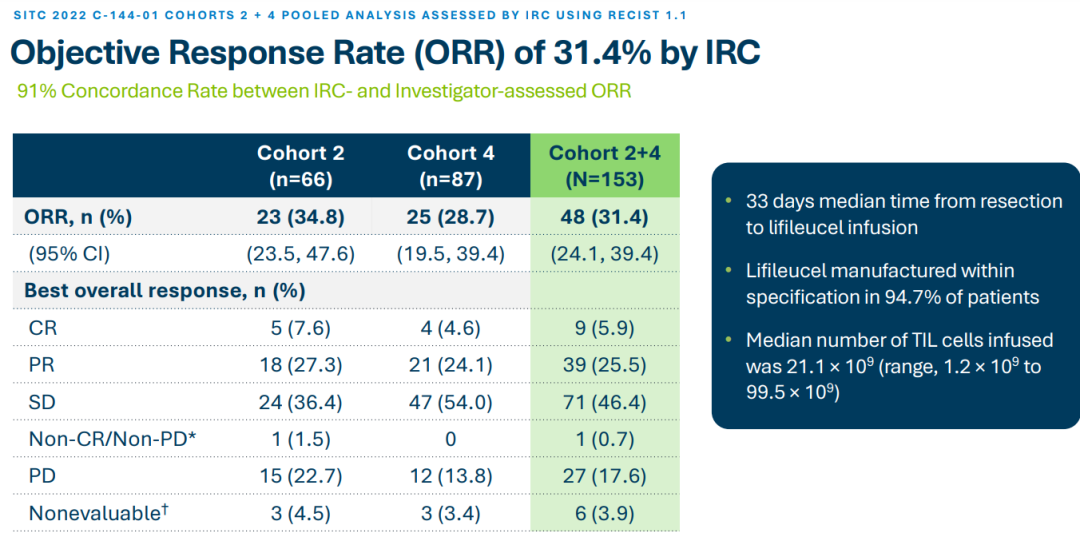
研究结果显示,经过独立影像学委员会(IRC)评估,队列2的客观缓解率(ORR)为34.8%;队列4的ORR为28.7%;队列2+4的总ORR为31.4%。
Iovance还就lifileucel的III期注册试验(研究代号TILVANCE-301)设计方案与FDA达成一致,该试验是将lifileucel与K药联合用于一线晚期黑色素瘤的试验,不仅旨在全面支持lifileucel获批用于治疗PD-1单抗进展后的黑色素瘤患者,同时也是为了支持lifileucel与K药联合用于一线晚期黑色素瘤治疗方案的注册申请。
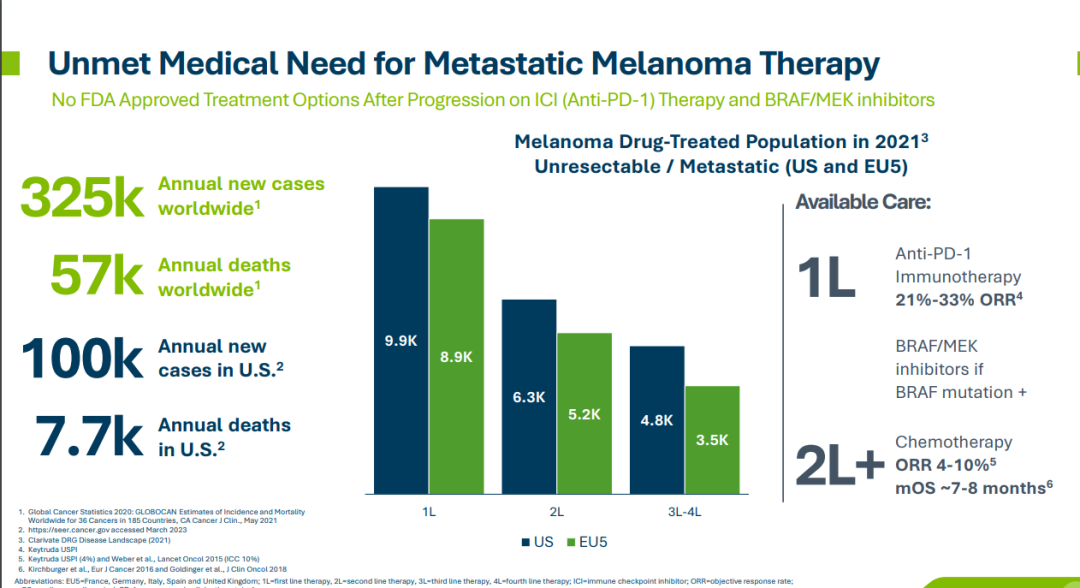
据报道,全球每年约有32.5万新发黑色素瘤患者,其中每年约有5.7万患者因该病死亡;美国每年约有10万人被出患有黑色素瘤,约有7700人死于该疾病。如果获得FDA的批准,lifileucel将成为一种在晚期黑色素瘤治疗中的全新选择。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 警惕“超级大肠杆菌”!它堵死肠道细胞“自我牺牲路”,新研究破解抗耐药密码 (2025-10-27)
- Nature Genetics:我们沿用20年的小鼠参考基因组,究竟错过了什么?一份T2T图谱的完整答案 (2025-10-26)
- 情感传染!南方医科大学最新论文登上Science封面 (2025-10-26)
- Nature Biotechnology:数据基准与算法创新的双轮驱动——DeepSomatic研究定义的基因组学发现新范式 (2025-10-25)
- Nature:当饥饿遇上荷尔蒙——大脑如何权衡母爱与生存? (2025-10-25)
- 加科思药业在AACR-NCI-EORTC国际大会公布泛KRAS抑制剂(JAB-23E73)临床前数据 (2025-10-24)
- 《柳叶刀》:减肥神药,暗藏护心秘法!迄今最大规模临床试验证实,司美格鲁肽的心脏保护作用与基线肥胖和体重减轻无关,或有独特保护机制 (2025-10-24)
- Cell子刊:脂肪细胞脂解,激活上皮干细胞,促进毛发再生 (2025-10-24)
- AJPCP:线粒体钾通道调节棕色脂肪组织的产热,为新的肥胖治疗铺平道路 (2025-10-24)
- 生育力下降别只怪卵子!Science:卵巢里的神经、胶质细胞才是“隐形操控者” (2025-10-24)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















