Nat Commun:发现鳞状细胞癌免疫逃避的新机制为改进免疫疗法提供了可能 |
 |
来源:100医药网 2024-05-31 13:06
在人类 SCC 患者中,TP63 的表达与 CD8+ T 细胞的浸润和活化呈负相关。重要的是,下调 TP63 能显著提高 PD-1 mAb 在 SCC 小鼠模型中的抗肿瘤免疫治疗效果。在一项新的研究中,来自中国科学院合肥物质科学研究院、中国科学技术大学和美国南加州大学的研究人员揭示了主调控转录因子 TP63在促进逃避和影响鳞癌免疫疗法疗效方面的肿瘤外源性功能。相关研究结果近期发表在Nature Communications期刊上,论文标题为 Reciprocal inhibition between TP63 and STAT1 regulates anti-tumor immune response through interferon- signaling in squamous cancer 。论文通讯作者为中国科学院合肥物质科学研究院的蒋焱熠(Jiang Yanyi)博士和南加州大学的Lin Dechen博士。

诸如抗PD-1/PD-L1抗体之类的免疫疗法大大改善了部分晚期鳞状(SCC)患者的治疗效果。然而,低反应率和抗药性也很常见。目前仍不清楚哪些患者能从免疫疗法中获益最多,也不清楚如何设计合理的组合免疫疗法策略,部分原因是SCC逃避的分子机制仍未明确。
这项研究首先对 1077 份 SCC 患者样本和 112 个细胞系进行了无偏见的高通量分析。通过分析,这些作者发现干扰素 / (IFN / )信号传导是受TP63抑制最显著的途径,而TP63通常在SCC中特异性过度表达。通过整合scRNA-seq、流式细胞术、体内同源小鼠模型和体外共培养数据,他们发现CD8+ T细胞是受TP63调控的主要细胞类型。抑制TP63会导致更多的CD8+ T细胞浸润,并增强对肿瘤的杀伤力。
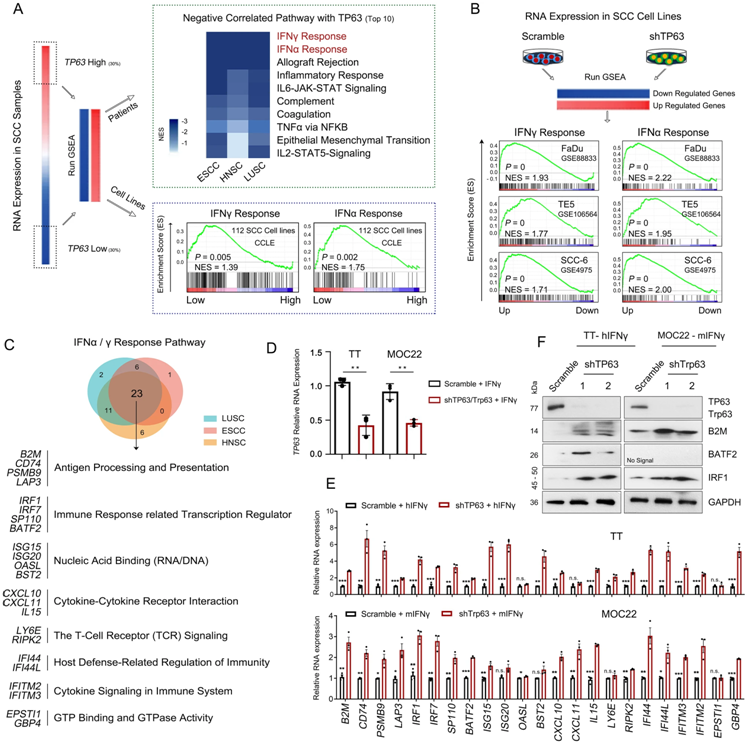
图片来自Nature Communications, 2024, doi:10.1038/s41467-024-46785-9
在人类 SCC 患者中,TP63 的表达与 CD8+ T 细胞的浸润和活化呈负相关。重要的是,下调 TP63 能显著提高 PD-1 mAb 在 SCC 小鼠模型中的抗肿瘤免疫治疗效果。
从机理上讲,这些作者发现,TP63和STAT1通过共同占据和共同调控各自的启动子和增强子,从而相互抑制,调控IFN 信号传导。STAT1和TP63之间的相对表达决定了IFN 信号传导的强度,而IFN 信号传导通过调节CD8+ T细胞的活性来决定免疫反应。
Jiang博士说, 我们的发现为了解SCC细胞如何逃避免疫监视提供了新的视角,并表明靶向IFN -TP63/STAT1轴是提高SCC抗肿瘤免疫治疗效果的一种潜在策略。 (100yiyao.com)
参考资料:
Yuan Jiang et al. . Nature Communications, 2024, doi:10.1038/s41467-024-46785-9.
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 当AI赶上医疗,会碰撞出怎么的聪明火花? (2025-10-28)
- 吉林做好2026年城乡住民根本医疗保险参保缴费任务 (2025-10-28)
- 重庆市医药推销平台药品挂网规定(试行) (2025-10-28)
- 2025年槲皮素十大护肺品牌口碑榜:槲皮素哪个牌子好? (2025-10-28)
- 国产进口护肝片官方旗舰店口碑对比,护肝片哪个牌子效果最好?十大品牌产品成分解析 (2025-10-28)
- 护肝片哪个品牌最好最安全?喝酒熬夜人群首选护肝产品推荐,Livereliv酒后救急护肝效率高 (2025-10-28)
- 护肝片排行第一名官方旗舰店,2025年保肝护肝产品十大品牌,给肝脏装上呼吸新风系统 (2025-10-28)
- 护肝片排行第一名官方旗舰店,2025年十大保肝护肝品牌推荐,熬夜党的“续命元气珠” (2025-10-28)
- 护肝片哪个品牌最好最安全?十大保肝护肝产品口碑推荐,烧烤火锅后肝脏依旧轻盈如燕 (2025-10-28)
- 水飞蓟宾哪个牌子效果最好?十大进口与国产保肝护肝品牌榜,护肝成分党必看攻略 (2025-10-28)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















