Nat Commun:足细胞OTUD5通过去泛素化TAK1,减轻足细胞炎症和损伤,减轻糖尿病肾病 |
 |
来源:100医药网 2024-07-21 15:53
本研究观察到OTUD5在HG/ pa刺激足细胞和糖尿病肾组织中下调。足细胞特异性Otud5敲除显著加重糖尿病小鼠足细胞损伤和DKD。肾病(DKD)是一种常见的疾病,是终末期肾脏疾病进展的主要原因。DKD的特征是蛋白尿增加,肾小球滤过减少,肾小球基底膜增厚,系膜基质积聚,足细胞损伤加重。足细胞是排列在肾小球基底膜(GBM)外表面的高度分化的上皮细胞,对维持GBM的完整性至关重要。
足细胞数量或密度的减少导致膜破坏并促进蛋白尿。因此,通常将足细胞损伤程度作为评价DKD进展的指标。此外,足细胞炎症的积累与足细胞损伤的加重有关。确定足细胞损伤调控的关键蛋白可能为DKD治疗提供策略和靶点,具有重要的临床意义。
泛素化/去泛素化作为一种翻译后修饰,在调节蛋白质的稳定性、定位和功能,参与多种疾病的病理生理中起着至关重要的作用。去泛素化酶(DUBs)通过去除底物蛋白中的泛素分子,负向调节动态可逆的泛素化过程。目前关于DUBs对肾功能调节的研究主要集中在和肾纤维化方面。例如,肾小管上皮细胞中USP11的缺失通过促进EGFR14的降解来改善肾纤维化小鼠模型的肾功能。
OTUD1和USP22可促进肾小管上皮细胞的纤维化和损伤。此外,USP13通过去泛素化ZHX217促进透明细胞肾的肿瘤发生。然而,很少有研究探讨DKD中DUBs与足细胞损伤之间的关系。考虑到足细胞功能在DN中的重要性,研究者对高浓度葡萄糖和棕榈酸(HG/PA)条件下的足细胞进行了RNA测序(RNA-seq)分析,发现足细胞中可能与dkd相关的DUB,卵巢肿瘤去泛素酶5 (OTUD5)。
OTUD5是一种半胱氨酸蛋白酶,属于OTU蛋白家族。它包含两个高度保守的结构域:催化OTU结构域和泛素相互作用基序(UIM)结构域。最近的研究已经证明OTUD5在介导先天和炎症发展中的关键作用。此外,OTUD5在各种癌症中的作用也逐渐被发现,例如在肝细胞癌和非小细胞中,OTUD5通过去除TRIM25和肿瘤蛋白P5321的泛素化而发挥致癌作用。然而,OTUD5在足细胞中的作用仍然未知。

图片来源:
近日,来自温州医科大学第一附属医院的研究者们在Nat Commun杂志上发表了题为 Podocyte OTUD5 alleviates diabetic kidney disease through deubiquitinating TAK1 and reducing podocyte inflammation and injury 的文章,该研究表明足细胞OTUD5通过去泛素化TAK1,减轻足细胞炎症和损伤,减轻糖尿病肾病,扩大了对糖尿病肾病发病机制的理解。
最近的研究表明足细胞损伤在糖尿病肾病(DKD)的发展中起着至关重要的作用,蛋白质的去泛素化修饰广泛参与疾病的发生和发展。
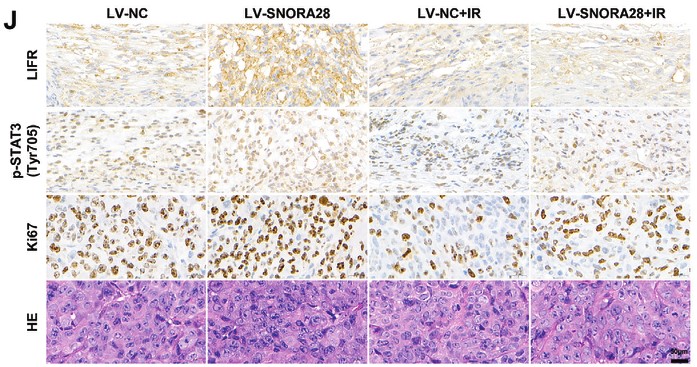
OTUD5作为足细胞炎症和损伤调节因子的鉴定
图片来源:
本文研究了脱泛素化酶OTUD5在足细胞损伤和DKD中的作用机制。RNA-seq分析显示,HG/ pa刺激足细胞中OTUD5的表达显著降低。在1型和2型糖尿病小鼠中,足细胞特异性Otud5敲除加剧足细胞损伤和DKD。此外,avv9介导的OTUD5在足细胞中的过表达显示出对DKD的治疗作用。
质谱和共免疫沉淀实验显示,炎症调节蛋白TAK1是足细胞中OTUD5的底物。在机制上,OTUD5通过其活性位点C224在K158位点去泛素化k63连接的TAK1,随后阻止TAK1的磷酸化并减少足细胞的下游炎症反应。本研究结果表明,OTUD5- tak1轴与足细胞炎症和损伤有关,并突出了OTUD5作为DKD治疗靶点的潜力。
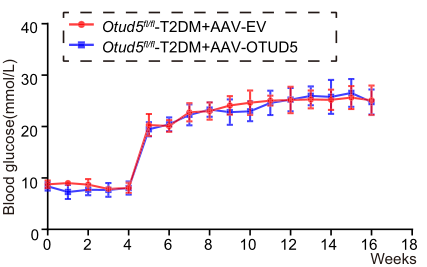
足细胞特异性过表达OTUD5可减轻T2DM小鼠足细胞损伤和DKD
图片来源:
综上所述,本研究观察到OTUD5在HG/ pa刺激足细胞和糖尿病肾组织中下调。足细胞特异性Otud5敲除显著加重糖尿病小鼠足细胞损伤和DKD。相反,OTUD5在足细胞中的过表达可改善T2DM小鼠足细胞损伤和DKD。在机制上,研究者证明OTUD5直接与TAK1相互作用,并通过其活性位点C224减少k63连接的TAK1残基K158的多泛素化,随后抑制TAK1介导的炎症反应和足细胞损伤。最后,研究者在体内验证了OTUD5-TAK1轴通过抑制TAK1调控足细胞损伤和DKD的作用。本研究报道了OTUD5在足细胞损伤中的作用,扩大了对DKD发病机制的理解。( 100yiyao.com)
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载-> 医药网新闻
医药网新闻

- 相关报道
-
- 颠覆“一胖毁所有”!最新研究:带这种“肥胖基因”缺陷,胖却血脂低、心血管风险降,大脑才是幕后调度官 (2025-10-22)
- Nat Commun:癌细胞也有“作战指挥室”?科学家用纳米炸弹把它炸了! (2025-10-22)
- Cell:黑色素瘤细胞表面的凹陷是肿瘤杀伤热点 (2025-10-22)
- 致敬世界传统医药日,扬子江药业“上新”非遗工艺“中药之冠” (2025-10-22)
- Cell:“细胞风暴”过境,熄灭中枢神经的“燎原之火”——CAR-T疗法为进展性多发性硬化带来新曙光 (2025-10-22)
- Nature Biotechnology:微缩战场!在毫米级芯片上,我们能否洞悉CAR-T细胞与实体瘤的生死对决? (2025-10-22)
- 《自然》:哺乳还有这种好处!科学家发现,生育和哺乳会促进CD8阳性T细胞在乳腺中的积累,可降低乳腺癌风险,尤其是三阴性乳腺癌 (2025-10-22)
- 槲皮素哪个牌子好?2025年十大槲皮素品牌深度解析:肺结节选购指南 (2025-10-22)
- 从结构性洗牌中突围:顾连医疗的十年,与一场康复行业的分化赛跑 (2025-10-22)
- 循证为基,人文为怀:苏州明基医院代谢与减重中心的高质量发展之道 (2025-10-22)
- 视频新闻
-
- 图片新闻
-
医药网免责声明:
- 本公司对医药网上刊登之所有信息不声明或保证其内容之正确性或可靠性;您于此接受并承认信赖任何信息所生之风险应自行承担。本公司,有权但无此义务,改善或更正所刊登信息任何部分之错误或疏失。
- 凡本网注明"来源:XXX(非医药网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。本网转载其他媒体之稿件,意在为公众提供免费服务。如稿件版权单位或个人不想在本网发布,可与本网联系,本网视情况可立即将其撤除。联系QQ:896150040





















